Clear Sky Science · de
Ein molekular definiertes basalo‑präfrontal‑thalamisches Schaltkreis reguliert sensorische und affektive Dimensionen von Schmerz bei männlichen Mäusen
Warum dieser Hirnkreis für Schmerz wichtig ist
Schmerz ist mehr als ein scharfer Stich oder dumpfer Schmerz; er trägt auch eine emotionale Last und kann unsere Stimmung und unser Verhalten über Jahre verändern. Viele Patienten mit chronischen Schmerzen finden wenig Linderung durch gängige Medikamente und haben häufig mit schweren Nebenwirkungen zu kämpfen. Diese Studie an männlichen Mäusen enthüllt einen präzise definierten Hirnkreis, der dem Gehirn ermöglicht, Schmerz sowohl in seiner Stärke als auch in seiner emotionalen Belastung hoch- oder herunterzudrehen. Durch Kartierung und Kontrolle dieses Pfades weist die Arbeit auf neue, gezieltere Wege hin, chronische Schmerzen zu lindern, ohne sich ausschließlich auf klassische Schmerzmittel zu stützen.
Eine verborgene Autobahn vom Denkzentrum zum Schmerz-Hub
Die Forschenden konzentrierten sich auf den medialen präfrontalen Kortex, eine vordere Gehirnregion, die an Entscheidungsfindung, Emotion und Schmerzregulation beteiligt ist, sowie auf den Thalamus, ein tief gelegenes Relaiszentrum, das sowohl die Intensität als auch die Unangenehmheit von Schmerz mitprägt. Sie entdeckten, dass eine spezifische Zellgruppe im medialen präfrontalen Kortex, markiert durch das Gen Foxp2, einen wichtigen Ausgangspfad zum Thalamus bildet. Diese Zellen liegen überwiegend in der tiefsten Schicht des Kortex und senden lange Fasern zu bestimmten thalamischen Kernen, während sie andere übliche Ziele des präfrontalen Kortex weitgehend auslassen. Mit Hilfe von Tracing‑Methoden und Ganzhirnkartierung zeigte das Team, dass diese Foxp2‑markierten Neurone starke Verbindungen zu drei thalamischen Regionen haben, die bekanntermaßen die Schmerzverarbeitung beeinflussen: dem parataenialen Nukleus, dem mediodorsalen Thalamus und dem ventromedialen Thalamus. 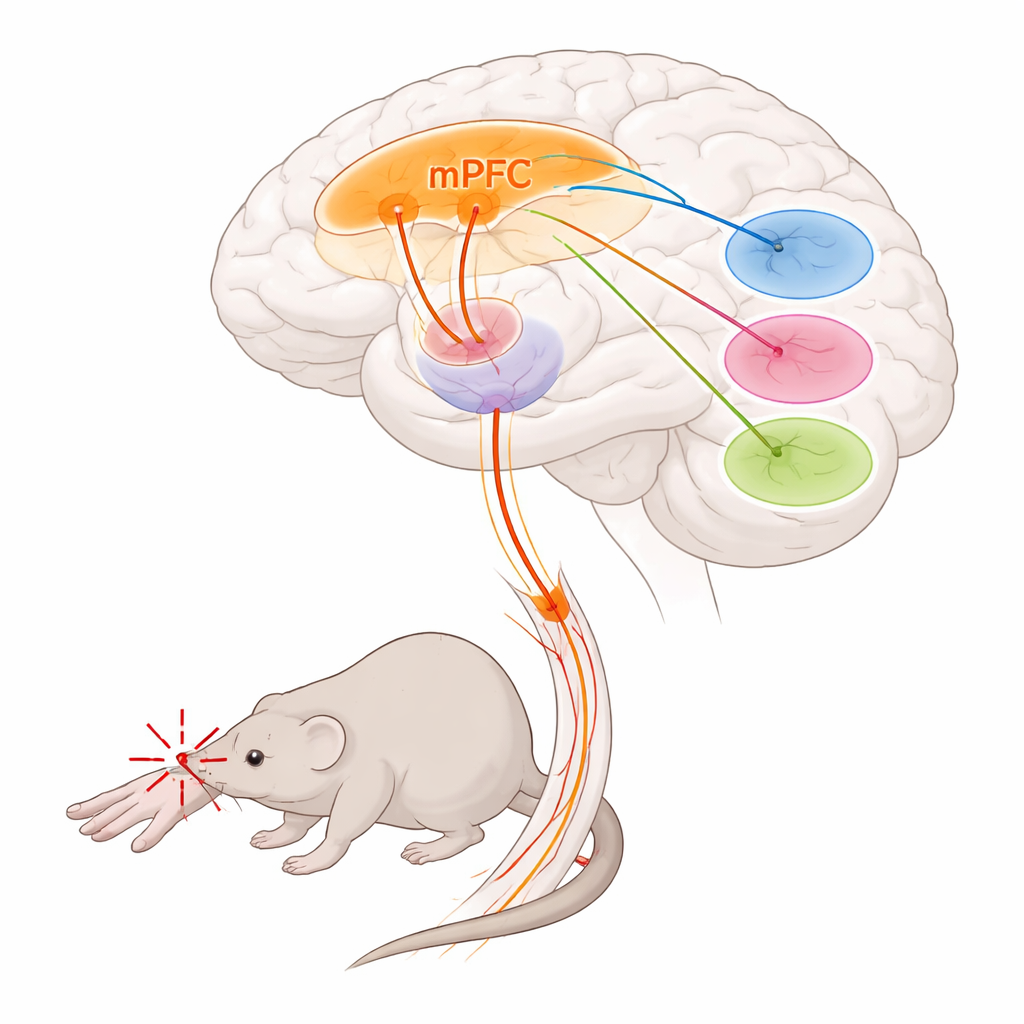
Wenn Schmerz einsetzt, fährt ein wichtiges Kontrollzentrum herunter
Um zu sehen, wie sich dieser Pfad bei Schmerz verhält, setzten die Wissenschaftler kleine Linsen über dem medialen präfrontalen Kortex ein und zeichneten die Aktivität einzelner Foxp2‑markierter Neurone in wachen Mäusen auf. Bei kurzen mechanischen Stichen, chemisch induziertem Schmerz durch Formalin und langanhaltendem entzündlichem Schmerz stellten diese Zellen durchgehend eine Verringerung ihrer Aktivität fest: Die meisten zeigten während schmerzhafter Episoden und in den Tagen nach entzündlicher Schädigung weniger Aktivitätsausbrüche. Dieses Abschalten war nicht subtil; unter manchen Bedingungen wurden mehr als ein Drittel bis nahezu die Hälfte der Zellen deutlich inaktiv. Die Befunde deuten darauf hin, dass akute und chronische Schmerzzustände zum Teil die Stilllegung eines natürlichen präfrontalen Bremssystems widerspiegeln könnten, das sonst helfen würde, Schmerz in Schach zu halten.
Das Schaltkreis‑An- und Ausschalten verändert Schmerz
Das Team fragte dann, ob dieses Herunterfahren nur eine Folge von Schmerz oder ein treibender Faktor dafür ist. Mit genetischen Werkzeugen blockierten sie entweder langfristig das Output der Foxp2‑markierten Neurone oder steigerten kurzzeitig deren Aktivität. Anhaltende Inaktivierung machte Mäuse empfindlicher gegenüber Berührung und Hitze, was darauf hinweist, dass dieser Pfad normalerweise eingehende Schmerzsignale dämpft. Im Gegensatz dazu erhöhte kurzfristige Aktivierung die Schwelle für schmerzhafte Reize, reduzierte das späte Lecken im Formalin‑Test (ein Maß für anhaltenden, entzündlichen Schmerz) und ließ Mäuse Umgebungen bevorzugen, in denen der Schaltkreis aktiviert worden war — ein Hinweis auf Erleichterung von der emotionalen Last des Schmerzes. Durch gezielte Bestrahlung spezifischer Astbereiche des Pfads zeigten die Forschenden, dass Projektionen zum parataenialen Thalamus sowohl die physische Sensitivität als auch die Bewältigungsreaktionen reduzieren, während Projektionen zum mediodorsalen und ventromedialen Thalamus vor allem die emotionalen und verhaltensbezogenen Dimensionen modulieren. Zusammen offenbaren diese Ergebnisse ein fein aufgespaltenes Verdrahtungsschema, in dem verschiedene Äste derselben präfrontalen Population unterschiedliche Facetten der Schmerzerfahrung steuern.
Chemische Feinabstimmung: ein cholinerges Plus für Schmerzlinderung
Was steuert diese präfrontalen schmerzlindernden Neurone? Tracing‑Experimente deckten starke Eingänge aus einer cholinergen Region des basalen Vorderhirns auf, dem horizontalen Diagonalband. Viele der Zellen, die Signale aus diesem Gebiet zu den Foxp2‑markierten Neuronen senden, verwenden Acetylcholin, einen Botenstoff, der an Aufmerksamkeit und Erregung beteiligt ist. Die Aktivierung dieser cholinergen Projektion verringerte die mechanische Sensitivität und die Bewältigungsverhalten und linderte entzündliche Hypersensitivität, obwohl sie den negativen emotionalen Ton des Schmerzes nicht deutlich veränderte. Auf der Empfängerseite fanden sich in Foxp2‑markierten Neuronen vermehrt eine bestimmte Art von Acetylcholinrezeptor, bekannt als α4β2‑nikotinischer Rezeptor. Die direkte Verabreichung eines selektiven α4β2‑Agonisten in den medialen präfrontalen Kortex machte Mäuse weniger empfindlich gegenüber schmerzhafter Hitze und Berührung, selbst bei chronischen Entzündungszuständen, und erhöhte die Aktivität in Foxp2‑markierten Neuronen. Die Blockade dieser Neurone aufgehob die Wirkung des Medikaments, was zeigt, dass dieser Rezeptor Schmerzen gezielt lindert, indem er genau diesen Zelltyp erregt. 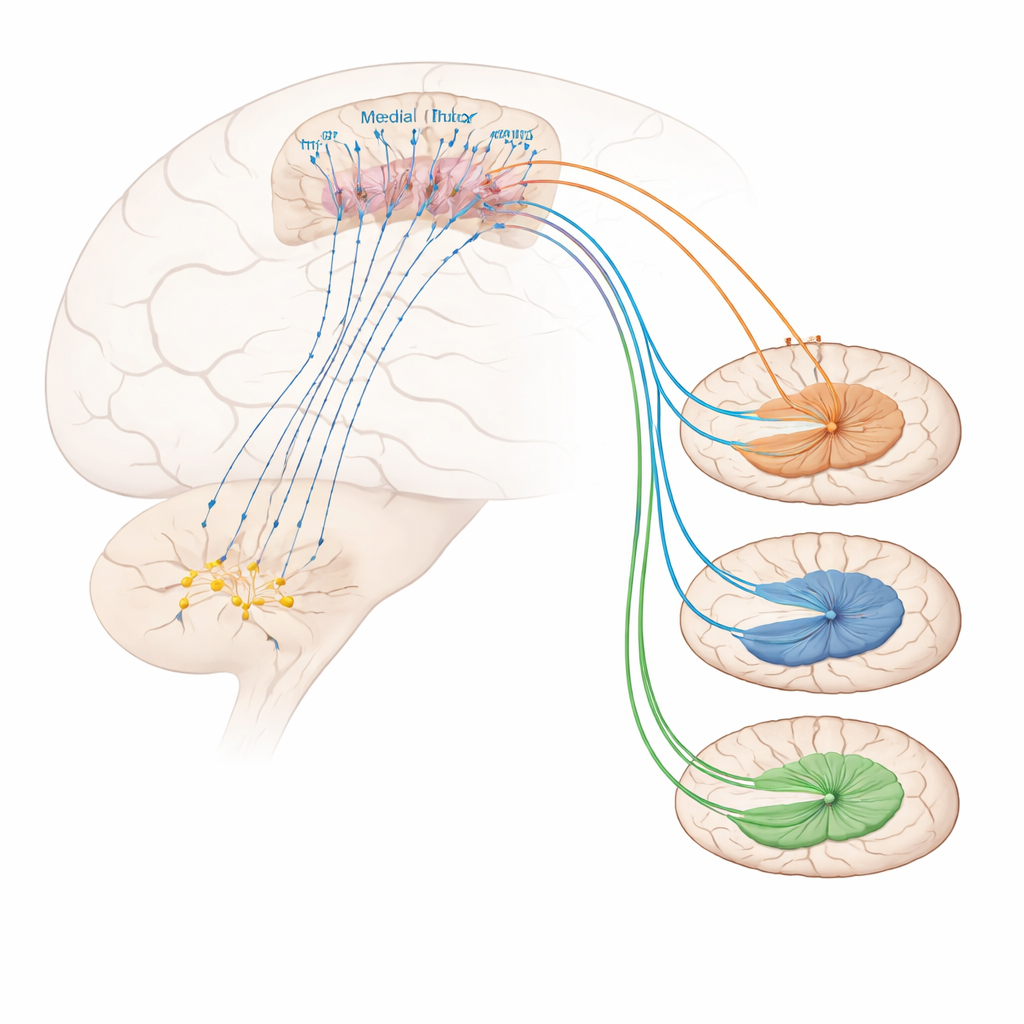
Was das für zukünftige Schmerzbehandlungen bedeutet
Anschaulich identifiziert die Studie einen präzisen Dreischrittpfad: eine cholinerge "Starter"‑Region im basalen Vorderhirn, eine spezialisierte Gruppe von Kontrollzellen im medialen präfrontalen Kortex und distinkte Relaiszentren im Thalamus, die getrennt steuern, wie stark Schmerz sich anfühlt, wie sehr er emotional belastet und wie wir darauf reagieren. Es scheint, dass Schmerz diesen Kreis herunterregelt; seine Reaktivierung, entweder durch direkte Stimulation oder durch gezielte Ansprache seiner Acetylcholinrezeptoren, verringert sowohl das Stechen als auch die Belastung durch entzündlichen Schmerz bei männlichen Mäusen. Obwohl noch viel Arbeit nötig ist, um diese Befunde auf den Menschen und auf andere Formen chronischer Schmerzen zu übertragen, heben die Ergebnisse eine vielversprechende Strategie hervor: Statt alle Empfindung zu betäuben, könnten zukünftige Therapien die eigenen schmerzhemmenden Kreise des Gehirns wiederherstellen oder feinabstimmen, um eine effektivere und möglicherweise sicherere Langzeitbehandlung zu ermöglichen.
Zitation: Xie, G., Liu, Y., Qi, X. et al. A molecularly defined basalo-prefrontal-thalamic circuit regulates sensory and affective dimensions of pain in male mice. Nat Commun 17, 2134 (2026). https://doi.org/10.1038/s41467-026-69001-2
Schlüsselwörter: chronischer Schmerz, medialer präfrontaler Kortex, Thalamus, cholinerges Signal, nikotinische Rezeptoren