Clear Sky Science · de
Ingenieurmäßige Herstellung synthetischer Zellen mit intramembranen Domänen, die unterschiedliche Bilayer‑Asymmetrien aufweisen
Warum winzige synthetische Bläschen wichtig sind
Jede lebende Zelle ist von einer Membran umhüllt, die sich wie eine intelligente, flexible Haut verhält. Diese Haut ist nicht einheitlich: Innen- und Außenseite und sogar verschiedene Bereiche auf der Oberfläche können sehr unterschiedliche Zusammensetzungen und Formen aufweisen. Diese Unterschiede helfen Zellen, Signale zu senden, Proteine zu binden und sich sogar zu teilen. Dennoch war es bemerkenswert schwierig, einfache, kontrollierbare Modellmembranen zu bauen, die diese Komplexität einfangen. Diese Studie stellt eine praktikable Methode vor, um zellgroße „synthetische Zellen“ herzustellen, deren Membranen sowohl in der Blattdicke asymmetrisch als auch lateral in unterschiedliche Regionen gemustert sind — ein Weg zu realistischeren Zellnachbildungen und zum Studium, wie Membranmuster Abschnürung und Teilung antreiben. 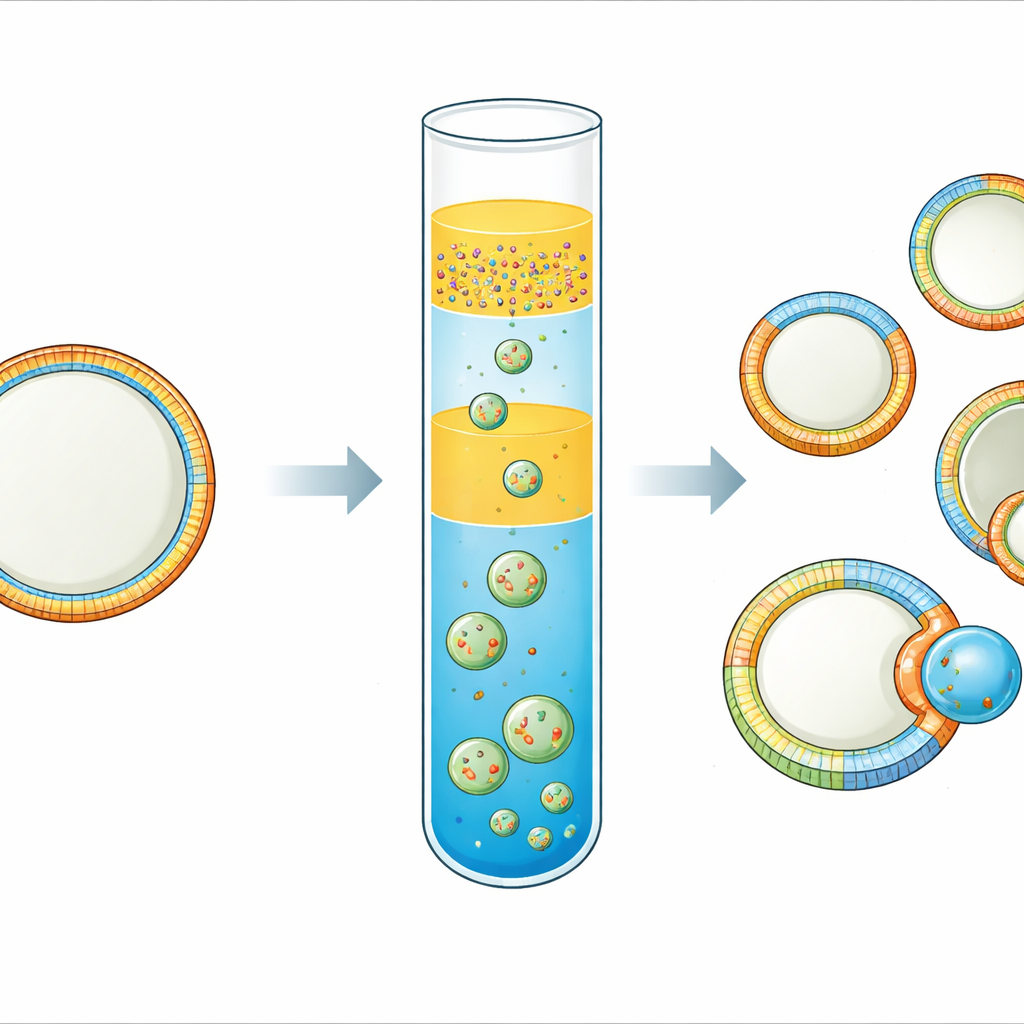
Bessere Zellnachbildungen bauen
Echte Zellmembranen sind asymmetrisch: Die Innenseite ist reich an negativ geladenen Lipiden, die Signalmoleküfte rekrutieren, während die Außenseite andere Lipide trägt, die die Zell–Zell‑Erkennung vermitteln. Viele Laborverfahren können riesige Vesikel erzeugen — hohle Kugeln aus fettähnlichen Molekülen —, doch ihre beiden Blattseiten sind meist gleich, und das Innere ist schwer zugänglich. Andere Ansätze, die Asymmetrie erzeugen, erfordern oft komplexe Geräte, spezielle Lipide oder führen dazu, dass die Vesikel an einer Oberfläche haften bleiben. Die Autoren wollten freistehende, zellgroße Vesikel schaffen, die hohe Einkapselung von Biomolekülen mit robuster, einstellbarer Asymmetrie kombinieren, die eher der einer lebenden Zelle ähnelt.
Ein Drei‑Schichten‑Rezept für asymmetrische Membranen
Das Team verfeinerte eine „inverted emulsion“-Technik, bei der winzige Wassertropfen, die mit Lipiden beschichtet sind, durch eine Öl‑Wasser‑Grenzfläche getrieben werden, um Vesikel zu bilden. Ihre zentrale Innovation ist eine dreischichtige Ölkonfiguration. Unten befindet sich ein Öl, das die Lipide für die äußere Blattseite enthält. Darüber legen sie eine dünne Zwischenölschicht ohne Lipide, und darauf eine Emulsion von Wassertropfen in einem zweiten Öl, das die Lipide für die innere Blattseite trägt. Während eines kurzen Zentrifugationsschritts fallen die Tropfen durch die Zwischen‑ und die untere Schicht, nehmen eine zweite Lipidschicht auf und schließen sich zu Vesikeln. Die Wahl von zwei Ölen mit unterschiedlicher Dichte und die Einfügung der Zwischenlage begrenzen das Mischen zwischen den Lipidpools stark, sodass die innere und äußere Blattseite unterschiedliche Zusammensetzungen beibehalten.
Nachprüfen, dass die beiden Seiten verschieden bleiben
Um zu verifizieren, dass die Blattseiten tatsächlich unterschiedlich waren, nutzten die Forscher chemische und proteinbasierte Nachweismethoden. In einer Versuchsreihe fügten sie ein fluoreszierendes Lipid nur einer Blattseite hinzu und setzten die Vesikel dann einer Chemikalie in der Außenlösung aus, die die Fluoreszenz löscht, aber die Membran nicht passieren kann. War das fluoreszierende Lipid außen, sank das Signal fast vollständig; war es innen, änderte sich kaum etwas — ein Beleg dafür, dass die markierten Lipide größtenteils dort blieben, wo beabsichtigt. In einer zweiten Experimentserie platzierten sie Lipide, die spezifische Proteine binden (etwa biotinmarkierte Lipide für Streptavidin oder spezielle Kopfgruppen für His‑markierte grün fluoreszierende Proteine), ebenfalls nur auf einer Blattseite. Zugefügte Proteine in der entgegengesetzten Kompartiment (innen oder außen) banden nur, wenn ihr passendes Lipid auf derselben Membranseite lag, was sowohl eine starke Asymmetrie als auch erhaltene Proteinfunktion bestätigte.
Rafts erzeugen und Membranen bei der Abschnürung beobachten
Echte Zellmembranen enthalten auch „Rafts“: winzige Bereiche, die in bestimmten Lipiden wie Cholesterin und Sphingomyelin angereichert sind, Proteine zusammenziehen und die Form beeinflussen können. Solche Phasentrennung mit der inverted emulsion‑Methode zu erreichen, war schwierig, weil Cholesterin dazu tendierte, im Öl gelöst zu bleiben statt in die Membran überzugehen. Durch die Verwendung von Squalen in der unteren Ölschicht, das Cholesterin weniger stark hält als Standard‑Mineralöl, konnten die Autoren reproduzierbar Vesikel herstellen, deren Membranen in koexistierende flüssig‑geordnete und flüssig‑ungeordnete Regionen aufspalteten — ähnlich den Rafts. Sie kombinierten dieses laterale Muster mit Blattasymmetrie: Eine Domäne trug einen inneren Blattliganden, der innen Streptavidin bindet, während eine andere Domäne Glykolipide trug, die außen das Choleratoxin binden. 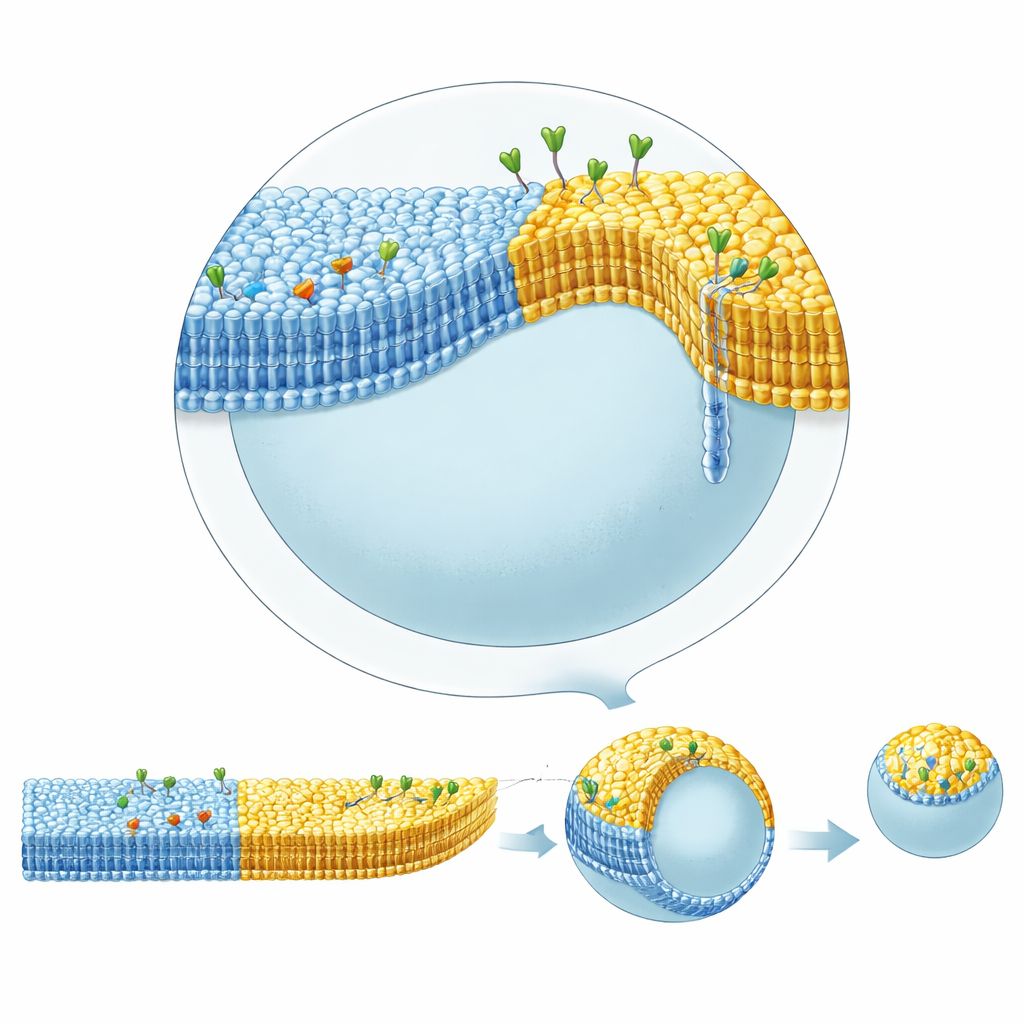
Wie Proteine und Muster Formänderungen antreiben
Diese komplexen Vesikel zeigten eindrückliche Formdynamik. Wenn Choleratoxin an Glykolipide in der geordneten Domäne auf der Außenseite band, wölbte sich diese Domäne nach außen zu einer gekrümmten Ausstülpung, verbunden durch einen engen Hals, und konnte bei leichter osmotischer Entleerung vollständig als Tochtervesikel abknopfen. Diese Abschnürung benötigte keine energieübertragenden Moleküle wie ATP oder spezialisierte Teilungsmaschinerie; sie entstand allein aus dem Zusammenwirken von Lipidzusammensetzung, Domänengrenzen und asymmetrischer Proteinbindung. Durch Erhöhung der Menge an innen gebundenem Streptavidin in der ungeordneten Domäne konnte das Team das nach außen gerichtete Biegen der geordneten Domäne entgegenwirken und allmählich eine kugeligere Form wiederherstellen. Detaillierte geometrische Analysen der Vesikelkonturen zeigten, dass die Membrankrümmung an der Grenze zwischen Domänen sprunghaft wechselt und dass die engen Hälse beim Abschnüren Kräften von mindestens einigen zehn Pikonewton standhalten müssen — eine Quantifizierung, wie Domänenstruktur und Proteindichte Membranen mechanisch formen können.
Was das für zukünftige synthetische Zellen bedeutet
Einfach gesagt haben die Autoren ein Rezept entwickelt, um weiche, zellgroße Bläschen herzustellen, deren Hüllen ähnlich wie echte Zellmembranen zweigeteilt und gemustert sind. Da die Methode relativ einfach ist, mit vielen verschiedenen Lipiden funktioniert und es erlaubt, Proteine und andere große Moleküle einzuschließen, ebnet sie den Weg zum Aufbau lebensechterer künstlicher Zellen von Grund auf. Solche synthetischen Zellen könnten Wissenschaftlern helfen, zu entschlüsseln, wie Membranmuster Signalübertragung, Transport und Teilung steuern, und sie könnten schließlich als intelligente Wirkstoffträger dienen, die im Körper auf Abruf ihre Form ändern oder sich teilen.
Zitation: Yandrapalli, N., Seemann, T., Lipowsky, R. et al. Engineering synthetic cells with intramembrane domains possessing distinct bilayer asymmetries. Nat Commun 17, 2620 (2026). https://doi.org/10.1038/s41467-026-68997-x
Schlüsselwörter: synthetische Zellen, Lipidmembranen, Membranasymmetrie, Phasentrennung, Membranabschnürung