Clear Sky Science · de
Nanodiscs für Virus-Glykoproteine als Plattform zur Impfstoffanalyse
Virusproteine als messbare Ziele
Moderne Impfstoffe stützen sich zunehmend auf präzise entworfene Versionen der Proteine, die die Oberfläche von Viren zieren. Diese Proteine sind die Hauptziele schützender Antikörper, lassen sich in ihrer natürlichen, membranverankerten Form aber nur schwer untersuchen. Dieser Artikel beschreibt eine neue Laborplattform, die vollständige virale Oberflächenproteine in winzige, flache Lipidpartikel — sogenannte Nanodiscs — einbettet. Dieses System erlaubt Forschern zu messen, wie gut Impfstoffkandidaten reale Viren nachahmen, wie Antikörper an sie binden und wie sich Impfstoffe zur besseren Schutzwirkung umgestalten lassen.
Warum die Rekonstruktion der Virusoberfläche zählt
Viele der wichtigsten viralen Proteine sind in eine fettige Membran verankert, so wie auch auf einem tatsächlichen Virus. Traditionelle Laborverfahren schneiden den Membrananteil ab, um diese Proteine in Lösung leichter herzustellen und zu reinigen. Dieser Kniff entfernt jedoch Bereiche in der Nähe der Membran, die besonders wertvolle Antikörperziele enthalten — etwa ein Segment des HIV, das als membrane-proximal external region (MPER) bekannt ist. Diese nahe der Membran liegenden Regionen können anders aussehen und sich anders verhalten, wenn sie nicht in einer realistischen Lipidumgebung eingebettet sind, sodass lösliche Proteinfragmente ein unvollständiges oder irreführendes Bild davon liefern können, wie ein Impfstoff im Körper wirken wird.
Aufbau einer vielseitigen Nanodisc-Plattform
Die Forschenden entwickelten einen schlanken Fünf-Tage-Workflow, um vollständige virale Oberflächenproteine aus menschlichen Zellen zu gewinnen, ihre natürlichen Membran durchspannenden Segmente intakt zu halten und sie in kontrollierte Lipidscheiben zurückzusetzen. Zunächst exprimierten sie gentechnisch veränderte HIV‑ und Ebola‑Glykoproteine auf Zelloberflächen, extrahierten sie dann schonend mit Detergenzien und fingen sie auf einer Aufreinigungsmatrix ein. Während die Proteine noch gebunden waren, mischten sie definierte Lipide und ein gürtelähnliches Gerüstprotein bei, das sich selbst zu einer kleinen, scheibenförmigen Membran zusammenlagert. Beim Entfernen des Detergens setzten sich die viralen Proteine in diese Nanodiscs. Die resultierenden Präparate waren hochrein, monatelang im Kühlschrank stabil und trugen Glykanschichten, die denen nativer viraler Spitzen sehr ähnlich waren. 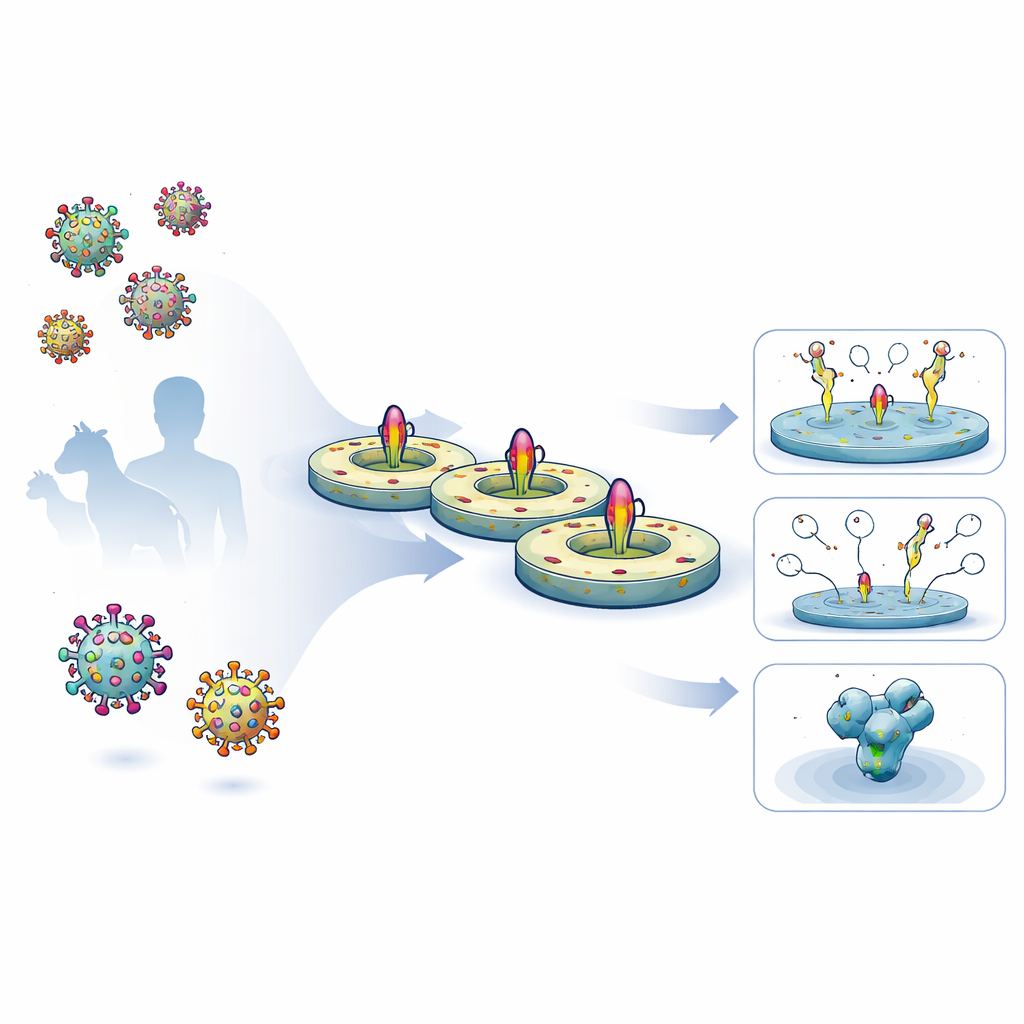
Antikörperbindung und Immunantworten messen
Mit den in Nanodiscs eingebetteten Proteinen testete das Team, wie gut verschiedene Antikörper unter mehreren Oberflächenplasmonresonanz-(SPR-)Setups binden, einer Technik zur Echtzeitverfolgung von Bindungen. Mit HIV‑Nanodiscs, die so gestaltet waren, dass sie die MPER‑Region exponieren, zeigten sie, dass ein potenter breit neutralisierender Antikörper namens 10E8 etwa 70‑mal stärker an das neu entwickelte Konstrukt gebunden war als an ein früheres Design — hauptsächlich weil er deutlich langsamer dissoziierte. Kontrollmutationen, die die MPER‑Region störten, eliminierten die Bindung von 10E8 vollständig, was bestätigt, dass die Plattform empfindlich anzeigt, wie Designänderungen Schlüssel‑Epitopen beeinflussen. Dieselben Nanodiscs dienten als Sonden in der Durchflusszytometrie, wo sie halfen, B‑Zellen aus immunisierten Mäusen und Affen herauszufischen, die die voll transmembrane Form des HIV‑Proteins erkannten, einschließlich Teilen, die in standardmäßigen löslichen Sonden fehlen. 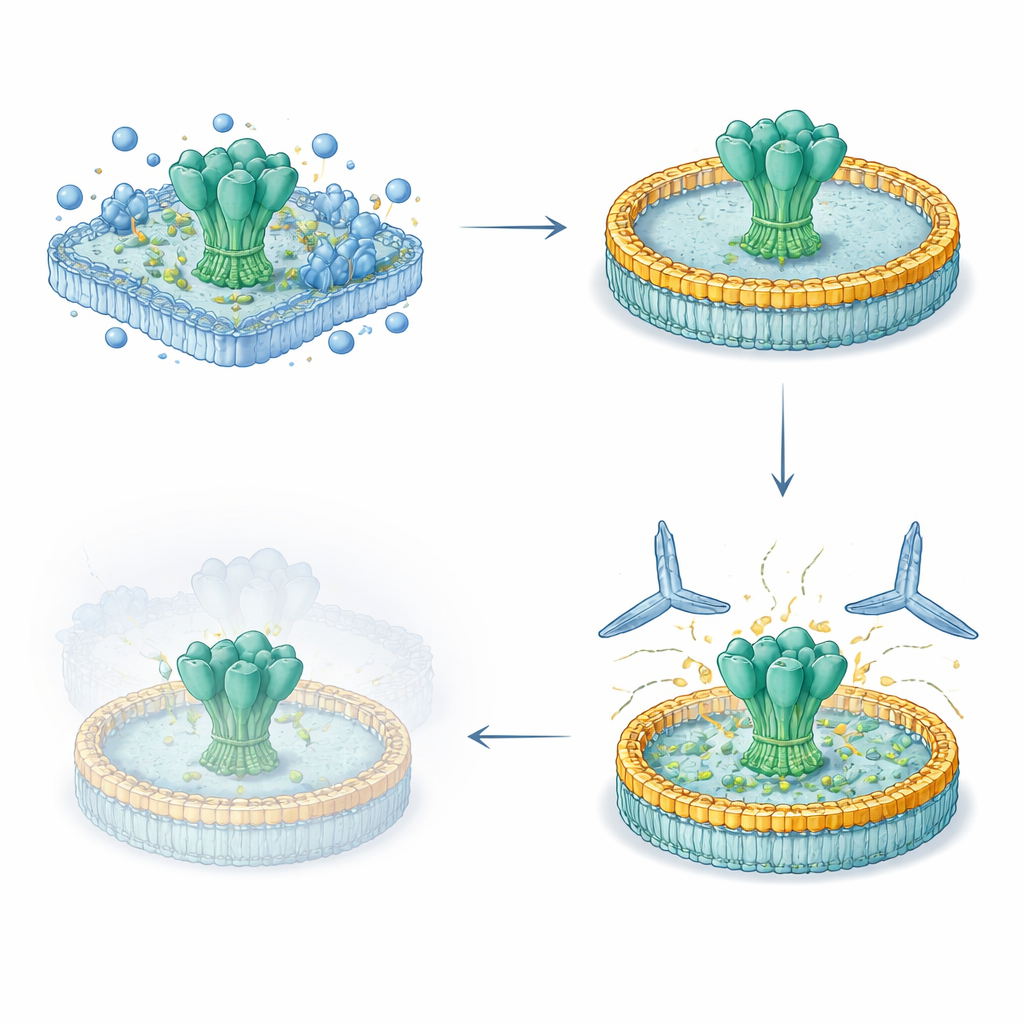
Das vollständige Ziel in atomarer Detailauflösung sehen
Um genau zu verstehen, wie Antikörper die MPER in ihrer nativen Umgebung erkennen, nutzten die Autorinnen und Autoren kryogene Elektronenmikroskopie, um die konstruierten HIV‑Nanodiscs gebunden an drei verschiedene breit neutralisierende Antikörper zu untersuchen. Sie erhielten eine 3,5‑Å‑Struktur eines Antikörpers, 10E8, der das MPER‑Segment engagiert, während der Rest der HIV‑Spitze weiterhin in der Lipidscheibe verankert war. Dies offenbarte ein durchgehendes Netzwerk von Kontakten zwischen 10E8 sowohl und dem MPER als auch benachbarten Teilen des äußeren Proteins, einschließlich einer tiefen Tasche an der Schnittstelle zwischen zwei Untereinheiten. Im Vergleich zu früheren Aufnahmen von 10E8, die nur an ein kurzes Peptid gebunden waren, zeigte das Team, dass die Membranumgebung und die vollständige Spike‑Form zusätzliche Kontakte und dynamische Bewegungen ermöglichen, die in einfacheren Modellen unsichtbar blieben, und dass bestimmte Aminosäuren im Virus stark beeinflussen, wie leicht 10E8 es neutralisieren kann.
Breite Einsatzmöglichkeiten für klügere Impfstoffe
Praktisch gesehen bietet diese Nanodisc‑Plattform Impfstoffdesignern ein Mittel, transmembrane Impfstoffkandidaten mit denselben leistungsfähigen analytischen Werkzeugen zu bewerten, die bislang vorwiegend für lösliche Proteinfragmente verwendet wurden. Sie funktioniert für verschiedene Viren, unterstützt detaillierte Bindungsmessungen, ermöglicht präzises Sortieren und Sequenzieren von impfstoffinduzierten B‑Zellen und liefert hochaufgelöste Strukturen, die realistische membrannahe Epitope einfangen. Für eine allgemeine Leserschaft lautet die Schlussfolgerung: Forschende verfügen jetzt über ein lebensnäheres Testfeld für virale Oberflächenproteine, das zeigt, welche Impfstoffdesigns wirklich wie das echte Virus aussehen und sich so verhalten — und wie man sie für stärkere, breitere Antikörperantworten optimiert. Das sollte die Entwicklung der nächsten Impfstoffgenerationen nicht nur gegen HIV, sondern gegen viele andere umhüllte Viren beschleunigen.
Zitation: Rantalainen, K., Liguori, A., Ozorowski, G. et al. Virus glycoprotein nanodisc platform for vaccine analytics. Nat Commun 17, 2561 (2026). https://doi.org/10.1038/s41467-026-68985-1
Schlüsselwörter: Nanodiscs, HIV-Impfstoffe, virale Glykoproteine, breit neutralisierende Antikörper, cryo-EM