Clear Sky Science · de
Radikale Footprinting in vollständigem Säugetierblut
Proteine in echtem Blut bei der Arbeit beobachten
Proteine in unserem Blut verändern laufend ihre Form, während sie lebenswichtige Aufgaben erfüllen, etwa Infektionen bekämpfen, Eisen transportieren und auf Krankheit reagieren. Bisher funktionierten die meisten Werkzeuge zur Untersuchung dieser feinen Formänderungen nur in vereinfachten Laborproben oder isolierten Zellen. Diese Studie zeigt erstmals, dass Wissenschaftler Proteinstrukturen direkt in intaktem Säugetierblut lesen können und damit einen Weg eröffnet haben, Krankheitsprozesse so zu beobachten, wie sie tatsächlich im Körper ablaufen.
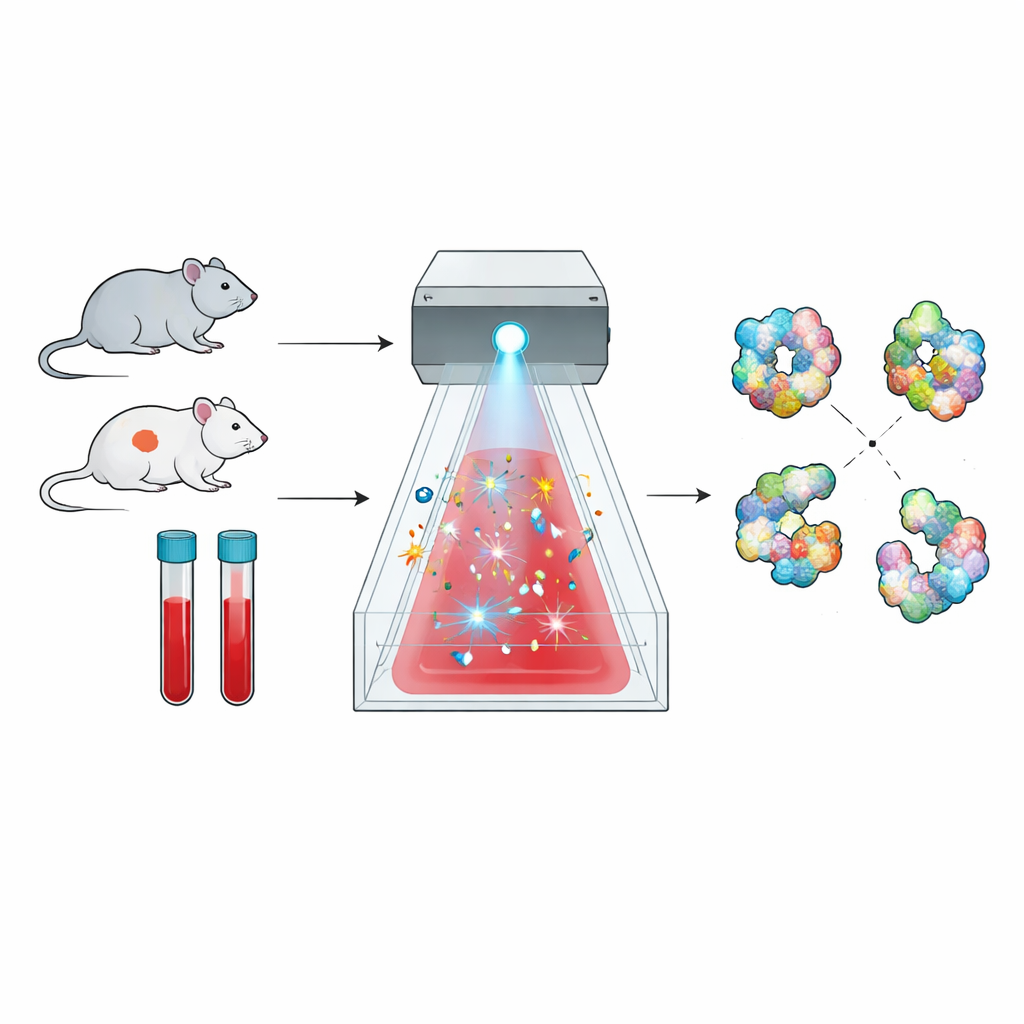
Eine neue Methode, Proteinformen zu kartieren
Proteine sind keine starren Kügelchen; sie falten sich zu komplexen dreidimensionalen Formen, und diese Formen bestimmen ihre Funktion. Das hier untersuchte Verfahren, radikales Protein-Footprinting, nutzt genau dieses Prinzip. Kurze Blitze hochreaktiver Moleküle wirken wie ein chemischer „Kamerablitz“ und treffen nur die Bereiche eines Proteins, die zur umgebenden Flüssigkeit hin exponiert sind. Anschließend wird Massenspektrometrie eingesetzt, um nachzuzählen, wo diese chemischen Treffer stattgefunden haben, und so eine Art Oberflächenkarte bzw. Fußabdruck der Proteinstruktur zu erstellen. Unterschiede im Fußabdruck zwischen gesunden und erkrankten Zuständen zeigen feine Verschiebungen in der Faltung des Proteins oder in seiner Interaktion mit Partnern.
Die Technik im ganzen Blut anwendbar machen
Die direkte Anwendung dieses Ansatzes auf Blut war lange eine Herausforderung. Blut absorbiert stark ultraviolettes Licht und ist voll von Enzymen wie Katalase, die die üblichen radikalbildenden Chemikalien schnell zerstören, bevor sie die Proteine markieren können. Die Forschenden lösten das Problem, indem sie auf Natriumpersulfat umstiegen, das durch einen intensiven breitbandigen Lichtblitz in potente Sulfatradikale gespalten werden kann. Mit einem kommerziellen System namens FOX zeigten sie, dass Persulfat zuverlässig aktiviert werden kann und dass eine integrierte Dosimetrie-Anzeige verfolgt, wie viele Radikale erzeugt werden, sodass die „Exposition“ jeder Probe genau kontrolliert werden kann.
Zellen schützen und gleichzeitig Details erfassen
Weil die Methode Proteine in einem Zustand untersuchen soll, der ihrer natürlichen Umgebung nahekommt, war es entscheidend, dass die Blutzellen selbst nicht zerstört werden. Tests an Mausblut zeigten, dass die Zugabe konzentrierten Persulfats nur geringe, reversible Veränderungen der Form roter Blutkörperchen verursachte und weniger als zwei Prozent Zellruptur auftraten — vergleichbar mit einfachen Kochsalzlösungen. Das Team entwickelte außerdem eine verbesserte „Quench“-Mischung, die verbleibende reaktive Spezies schnell auffängt und so schädliche Nebenreaktionen nach dem Blitz verhindert. Zusammen erlaubten diese Verfeinerungen, Proteine in intaktem Mausblut zu markieren, dabei die Zellstruktur zu erhalten und das Hintergrundrauschen sehr niedrig zu halten.
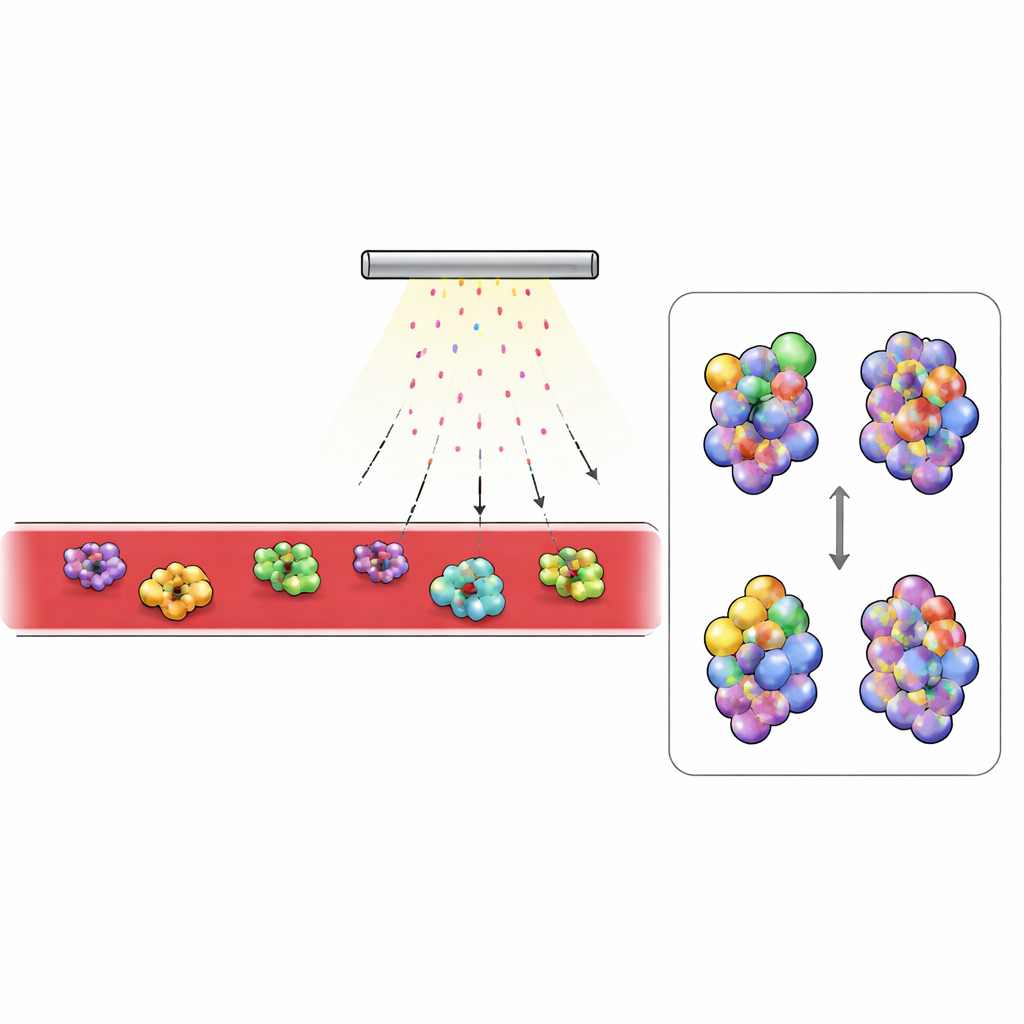
Was sich im diabetischen Blut verändert
Mit dieser Plattform verglichen die Forschenden Blut von gesunden Mäusen und von einem gängigen Modell für Typ-2-Diabetes. Sie konzentrierten sich auf die am häufigsten nachgewiesenen Proteine, insbesondere solche, die außerhalb der Zellen zirkulieren. Extrazelluläre Proteine zeigten deutlich stärkere Markierung als solche innerhalb der Zellen, was die begrenzte Penetration von Persulfat in Zellinnenräume widerspiegelt. Zwei Blutproteine hoben sich hervor: Komplement C3, ein Schlüsselbestandteil des Immunsystems, und Transferrin, das Eisen transportiert. Bei diabetischen Mäusen waren Bereiche von C3, die beim Umschalten in die aktive Form vergraben werden, weniger markiert, während normalerweise verborgene Regionen stärker exponiert waren. Dieses Muster stimmte mit der bekannten strukturellen Veränderung überein, wenn C3 in sein aktives Fragment C3b umgewandelt wird, und Bluttests bestätigten, dass diabetische Tiere deutlich mehr aktiviertes C3 aufwiesen. Bei Transferrin waren Bereiche in der Nähe der Eisenbindungsstelle in diabetischem Blut stärker geschützt, was zu dem Bild passt, dass das Protein mehr Eisen trägt. Unabhängige Messungen zeigten erhöhtes Serum-Eisen und einen größeren Anteil eisenbesetzter Transferrin-Moleküle bei den diabetischen Mäusen.
Warum das für Gesundheit und Medizin wichtig ist
Für Nichtfachleute lautet die Kernbotschaft, dass die Autorinnen und Autoren eine Methode entwickelt haben, um die Formen vieler Proteine gleichzeitig direkt im echten Blut „zu ertasten“ und diese Formmuster zu nutzen, um Rückschlüsse darauf zu ziehen, wie Krankheiten die Biochemie des Körpers verändern. In diesem Mausmodell des Typ-2-Diabetes offenbart die Methode eine überaktive Komplement-Signalisierung und stärkere Eisenbeladung von Transferrin — Veränderungen, die klassische Tests übersehen oder nur indirekt erfassen könnten. Da der Ansatz mit kleinen Blutmengen funktioniert und eine standardisierte Lichtquelle verwendet, könnte er künftig helfen, frühe strukturelle Warnzeichen von Krankheiten zu identifizieren, die Verteilung von Biopharmazeutika im Blut zu verfolgen und die Entwicklung wirksamerer Therapien zu unterstützen.
Zitation: Zhao, M., Tobin, L., Misra, S.K. et al. Radical footprinting in mammalian whole blood. Nat Commun 17, 2470 (2026). https://doi.org/10.1038/s41467-026-68982-4
Schlüsselwörter: strukturelle Proteomik, Blutproteine, Typ-2-Diabetes, Komplementsystem, Eisenstoffwechsel