Clear Sky Science · de
Koacervat-Tropfen als pH-regionalisierte Protocellen
Warum winzige Tropfen für die Chemie des Lebens wichtig sind
In unseren Zellen müssen zahllose chemische Reaktionen mit genau der richtigen Geschwindigkeit und unter genau den richtigen Bedingungen ablaufen, damit wir leben. Eine der wichtigsten dieser Bedingungen ist die Säurestärke, meist beschrieben durch den pH‑Wert. Doch einige der geschäftigsten ‚Arbeitsplätze‘ der Zelle, die membranlosen Organellen, besitzen keine umgebende Membran oder Pumpen zur Festlegung ihres pH. Diese Studie untersucht, wie einfache, tropfenartige Strukturen aus kurzen Peptiden diese Organellen nachahmen, eigene winzige pH‑Zonen erzeugen und komplexe Reaktionen wie DNA‑Kopieren und Proteinsynthese steuern können — und liefert damit Hinweise sowohl für die moderne Zellbiologie als auch dafür, wie frühe Protocellen auf der Erde funktioniert haben könnten.
Versteckte pH‑Zonen im Kontrollzentrum der Zelle
Die Autor:innen beginnen mit dem Nukleolus, einem großen, tropfenartigen Kompartiment im Zellkern, das beim Aufbau von Ribosomen, den Proteinfabriken der Zelle, hilft. Mit einem fluoreszierenden Farbstoff, der seine Farbe pH‑abhängig ändert, maßen sie die Säure im Nukleolus und im umliegenden Nukleoplasma in verschiedenen Zelltypen. Sie fanden, dass der Nukleolus konstant geringfügig saurer ist als seine Umgebung und damit einen eingebauten pH‑Unterschied über diese unsichtbare Grenze hinweg zeigt. Behandelten sie Zellen mit Wirkstoffen, die die Aktivität oder Struktur des Nukleolus stören, verringerte oder verschwand dieser pH‑Kontrast, was die lokale Säure nicht auf Membranpumpen, sondern auf das Vorhandensein und die Integrität der tropfenartigen Struktur selbst zurückführt.
Synthetische Tropfen bauen, die Säure spalten
Um diesen Effekt unter kontrollierten Bedingungen zu untersuchen, bauten die Forschenden ein künstliches System 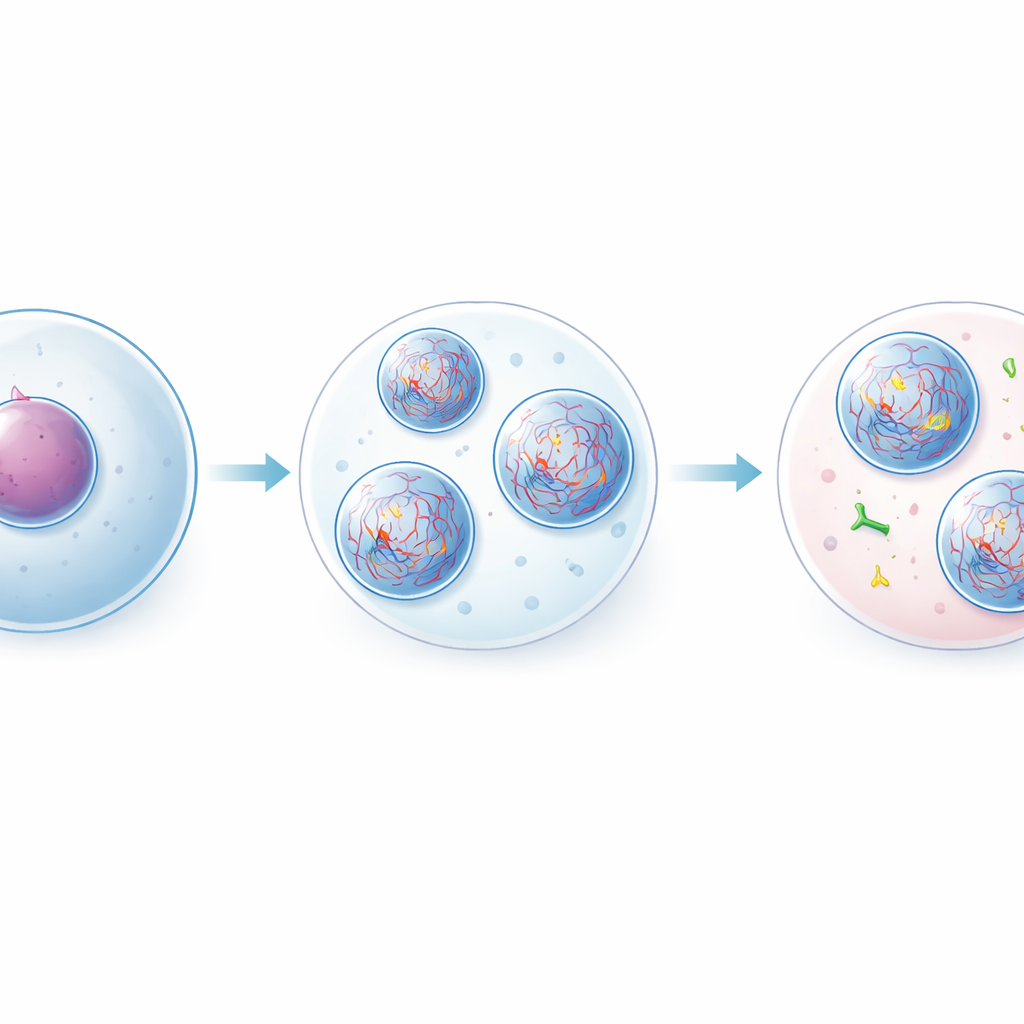
Tropfen in miniaturisierte Reaktoren verwandeln
Als Nächstes luden die Forschenden diese Peptidtropfen mit echten Enzymen, die bei ihrer Tätigkeit natürlich den pH verändern. Ein Enzym, Glucoseoxidase, wandelt Zucker in eine Säure um und senkt so den pH. Ein anderes, Urease, spaltet Harnstoff zu basischen Produkten und hebt den pH. Die Enzyme konzentrierten sich spontan in den Tropfen aufgrund attraktiver, ladungsbasierter Wechselwirkungen mit den Peptidketten. Wurden ihre Substrate zugegeben, veränderte sich das pH im Inneren der Tropfen stärker als in der umgebenden Lösung, und dieser Einstellbereich ließ sich durch Anpassung der Tropfenzusammensetzung und des Salzgehalts erweitern oder verengen. Trotz der dichten Umgebung blieben die Enzyme aktiv, wenn auch ihre Geschwindigkeit und scheinbare Substrataffinität sich von der in einfacher Lösung unterschieden — ein Spiegelbild der speziellen Mikroumgebung in jedem Tropfen.
Reaktionskaskaden durch lokale Säure programmieren
Mit kontrollierbaren pH‑Zonen untersuchten die Autor:innen, ob eine Reaktion in einem Tropfen eine andere hoch- oder herunterregeln kann 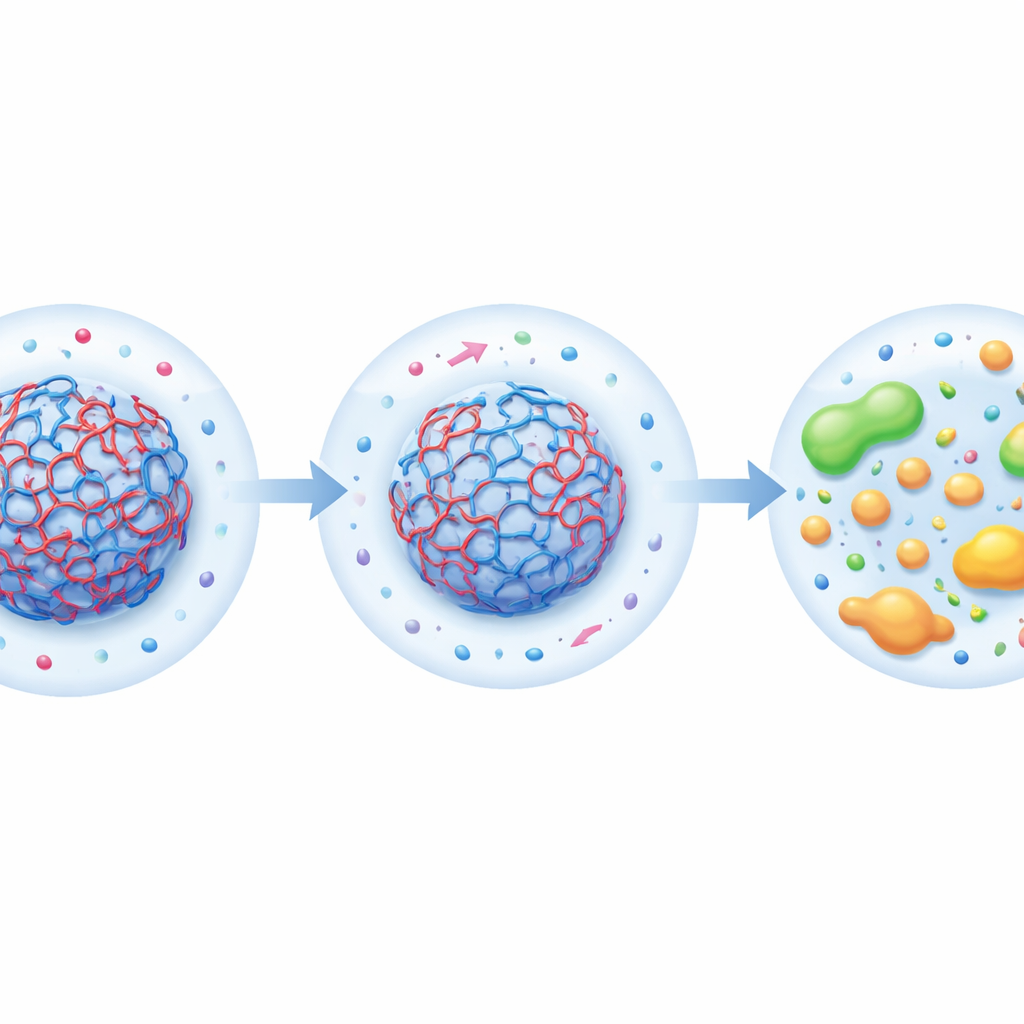
Was das für Zellen und Protocellen bedeutet
Insgesamt zeigt die Arbeit, dass durch Phasentrennung gebildete Tropfen auf natürliche Weise kleine, aber bedeutsame pH‑Unterschiede erzeugen und aufrechterhalten können — ohne Membranen, Pumpen oder aufwändige Maschinerie. In lebenden Zellen könnten ähnliche Kondensate dieses Prinzip nutzen, um fein abzustimmen, welche Reaktionen wo und wann stattfinden und so Stoffwechsel und Genregulation räumlich zu organisieren. Im Kontext des frühen Lebens fungieren solche Koacervat‑Tropfen als plausible Protocellen und bieten geschützte Umgebungen, in denen Schlüsselreaktionen wie das Kopieren genetischen Materials und die Synthese einfacher Proteine durch lokale Chemie allein gelenkt werden konnten. Indem die Studie präzise pH‑Kontrolle und komplexe Reaktionsketten in diesen minimalen Systemen demonstriert, trägt sie sowohl zum tieferen Verständnis moderner zellulärer Organisation bei als auch zur Entwicklung neuer Werkzeuge der synthetischen Biologie, die Phasengetrennte Tropfen als programmierbare, pH‑abgestimmte Mikroreaktoren nutzen.
Zitation: Wang, C., Fang, Z., Zhang, L. et al. Coacervate droplets as pH-regionalized protocells. Nat Commun 17, 2252 (2026). https://doi.org/10.1038/s41467-026-68980-6
Schlüsselwörter: membranfrei Organellen, Phasentrennung, Koacervat‑Tropfen, pH‑Regulation, Protocellen