Clear Sky Science · de
Variationen am C-Terminus von Proteinen beeinflussen Proteostase
Wie das Schwanzende von Proteinen die Gesundheit formt
Jedes Protein in unseren Zellen endet mit einem winzigen „Schwanz“ aus nur wenigen Bausteinen. Diese Schwänze wirken vielleicht wie ein Nebeneinander, aber diese Studie zeigt, dass sie still entscheiden, welche Proteine verweilen und welche schnell entfernt werden. Da Proteinmengen Krebs, genetische Störungen und die Stressantworten von Zellen beeinflussen, eröffnet das Verständnis dieser Schwänze neue Wege, Krankheitsrisiken zu beurteilen und mögliche Behandlungsansätze zu entwerfen.
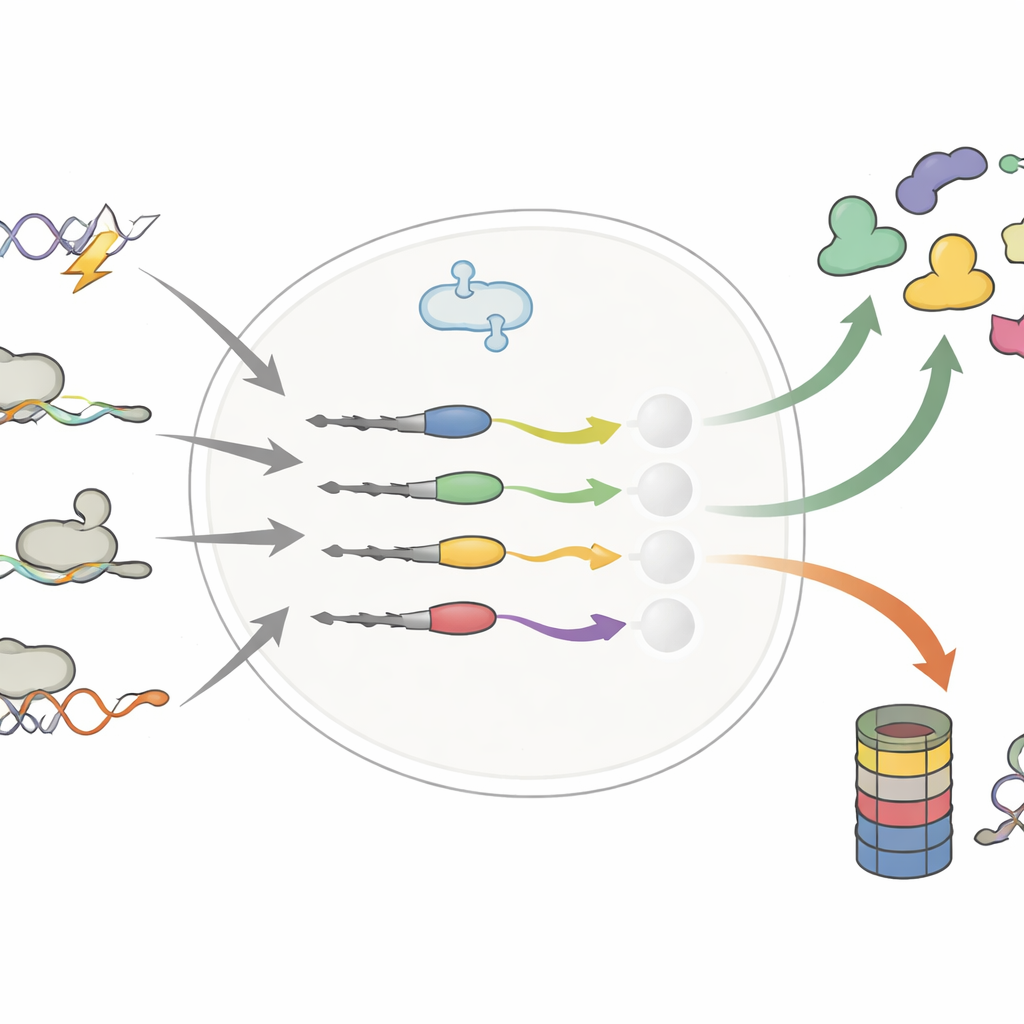
Kleine Änderungen am Proteinende, große Veränderungen in der Lebensdauer
Die Autoren konzentrierten sich auf das entfernte Ende der Proteine — das C-Terminus — wo bereits wenige zusätzlich angefügte oder ausgetauschte Bausteine durch DNA-Mutationen, alternatives RNA-Spleißen oder durch das Überschreiben des üblichen Stoppsignals entstehen können. Frühere Arbeiten nahmen an, dass solche „fehlerhaften“ Schwänze vor allem als Entsorgungsmarken wirken und defekte Proteine an den zellulären Abbauweg schicken. Durch den systematischen Vergleich von Tausenden normaler und veränderter Schwänze widerlegt diese Studie dieses vereinfachte Bild. Das Team zeigt, dass veränderte Schwänze die Lebensdauer eines Proteins entweder verkürzen oder verlängern können und dabei manchmal onkogene Treiber stabilisieren oder Tumorsuppressoren destabilisieren.
Wann genetische Fehler Proteinen helfen oder schaden
Eine wichtige Quelle für Schwanzänderungen sind Nonstop-Mutationen, bei denen ein normales Stoppsignal gelöscht wird, sodass das Ribosom in einen normalerweise stillen RNA-Abschnitt weiterliest. Die Forscher untersuchten über 3.000 mit Krankheiten assoziierte Nonstop-Varianten mit einem dualen Farbreporter, der misst, wie stark jeder Schwanz ein Modellprotein schützt oder schwächt. Im Durchschnitt machten mutante Schwänze Proteine immer noch weniger stabil als ihre normalen Gegenstücke, doch ein erheblicher Teil bewirkte das Gegenteil: Ungefähr eine von zehn Nonstop-Mutationen stabilisierte Proteine, während fast ein Drittel sie destabilisierte. Diese Veränderungen betrafen bekannte Onkoproteine und Tumorsuppressoren, was nahelegt, dass vermeintlich subtile Mutationen tatsächlich das Gleichgewicht von Zellwachstum und -tod verschieben können.
Eingebaute Vielfalt durch Spleißen und Readthrough
Nicht alle Schwanzunterschiede sind Zufall. Unsere Gene erzeugen routinemäßig mehrere Proteinvarianten durch alternatives Spleißen und programmiertes Stopcodon-Readthrough. Beim Durchsuchen menschlicher Genkataloge fanden die Autoren, dass fast zwei Drittel der Gene Proteine mit mehr als einem Schwanzdesign produzieren, wobei viele sich nur in den letzten wenigen Bausteinen unterscheiden. Tests ausgewählter Beispiele zeigten, dass diese nahezu identischen Varianten oft deutlich unterschiedliche Halbwertszeiten besitzen. Manche durch Readthrough erzeugten Schwänze machten Proteine stabiler, andere weniger stabil. Das legt nahe, dass Zellen Schwanzvariation bewusst als Feineinstellungsmechanismus nutzen, um zu regulieren, wie lange bestimmte Proteinformen in verschiedenen Geweben oder Situationen bestehen bleiben.
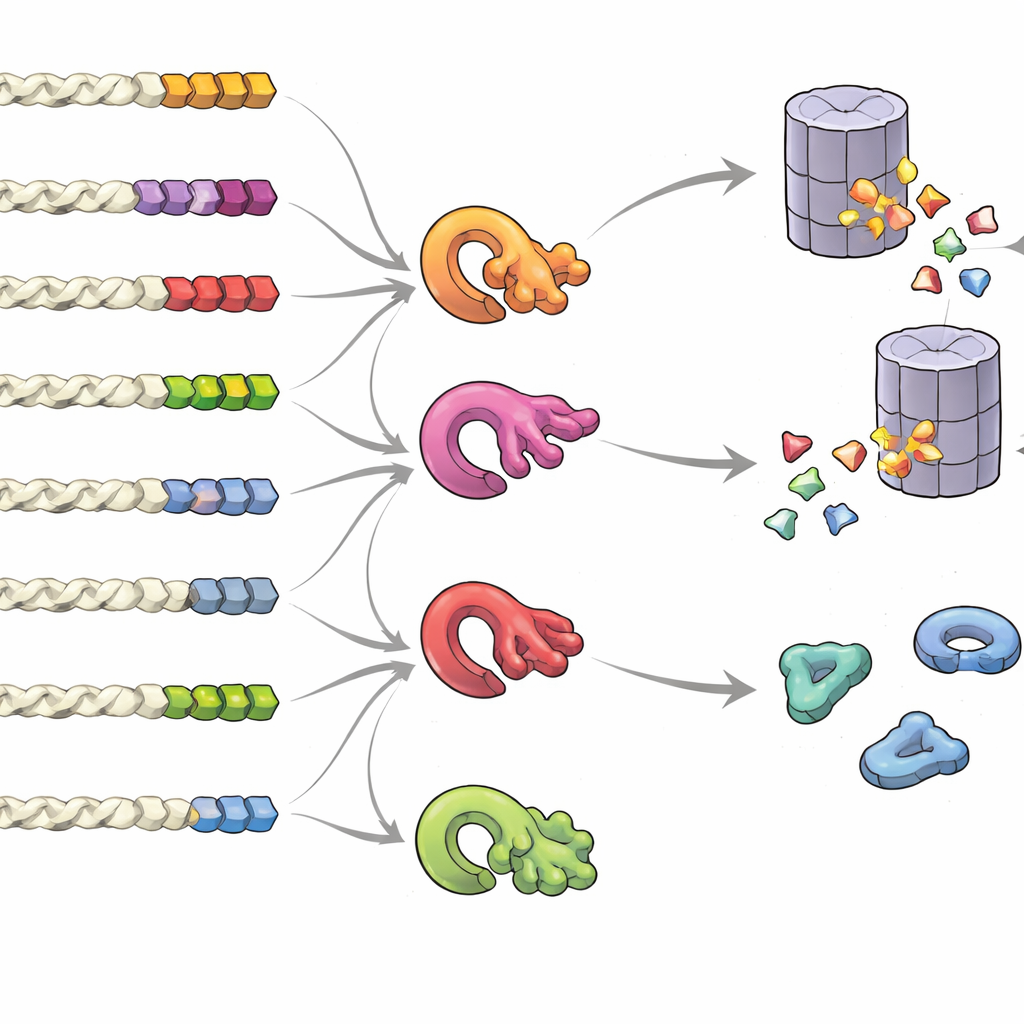
Was einen Schwanz zum „Behalte mich“- oder „Weg damit“-Signal macht
Um zu verstehen, welche Merkmale eines Schwanzes das Schicksal eines Proteins beeinflussen, erzeugte das Team Bibliotheken zufälliger Schwänze und maß deren Wirkung in großem Maßstab. Sie fanden heraus, dass es nicht nur ein einzelnes festes „Motiv“ ist, sondern die Gesamtzusammensetzung, Position und Clusterbildung bestimmter Bausteine zählen. Schwänze, die reich an kleinen oder fettliebenden Komponenten oder an den selteneren Cystein- und Tryptophan-Resten sind, neigten dazu, Abbau zu fördern, besonders wenn diese Reste gehäuft vorkamen. Im Gegensatz dazu förderten säurehaltige (acidische) Schwänze Stabilität. Beim Vergleich vieler Arten zeigten normale Proteinenden klare Spuren evolutionären Drucks, riskante Muster zu vermeiden, während fehleranfällige Readthrough- oder Frameshift-Schwänze zu destabilisierenden Zusammensetzungen neigten. Die Gruppe entdeckte außerdem, dass mehrere Qualitätskontroll-Enzyme — verschiedene Ubiquitin-Ligasen — sich darauf spezialisiert haben, unterschiedliche hydrophobe Schwanzmuster zu erkennen und so ein komplexes Netzwerk bilden, das entscheidet, welche Proteine abgebaut werden.
Warum das für Medizin und Biotechnologie wichtig ist
Die Arbeit rückt Proteinenden von passiven Abschlüssen zu aktiven Regulatoren der Proteinmenge. Für Laien bedeutet das: Viele Krankheiten könnten nicht nur durch defekte Proteine entstehen, sondern auch durch subtile Veränderungen in der Verweildauer von Proteinen, verursacht durch geringfügige Unterschiede an ihren Enden. Es warnt auch davor, dass Therapien, die gezielt Readthrough von Stoppsignalen fördern — etwa bei bestimmten genetischen Erkrankungen — unbeabsichtigt die Lebensdauern vieler normaler Proteine verändern könnten. Gleichzeitig deuten die Ergebnisse auf mächtige neue Strategien hin: Durch das gezielte Gestalten von Schwanzsequenzen oder das Fördern bestimmter Spleißformen oder Readthrough-Ereignisse könnten Wissenschaftler eines Tages Proteinmengen mit bemerkenswerter Präzision herauf- oder herunterregeln.
Zitation: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
Schlüsselwörter: Protein-Stabilität, C-terminaler Schwanz, Proteinabbau, genetische Mutationen, Proteostase