Clear Sky Science · de
OmiGA für ultraschnelles Mapping molekularer quantitativer Merkmal‑Loci
Warum das für Gesundheit und Zucht wichtig ist
Die moderne Genetik hat Millionen von DNA‑Unterschieden aufgedeckt, die Merkmale wie Krankheitsrisiko, Wachstum und Stoffwechsel fein beeinflussen. Die meisten dieser Unterschiede wirken nicht durch direkte Veränderungen von Proteinen, sondern indem sie die Aktivität von Genen fein justieren. Um diese Regulationsebene zu verstehen, ordnen Forscher „molekulare Merkmale“ wie Genexpression dem Genom zu. Dieses Paper stellt OmiGA vor, ein neues Analyse‑Toolkit, das dieses Mapping sowohl genauer als auch dramatisch schneller macht, insbesondere in Populationen, in denen viele Individuen verwandt sind – etwa Nutztierrassen und einige menschliche Familien. 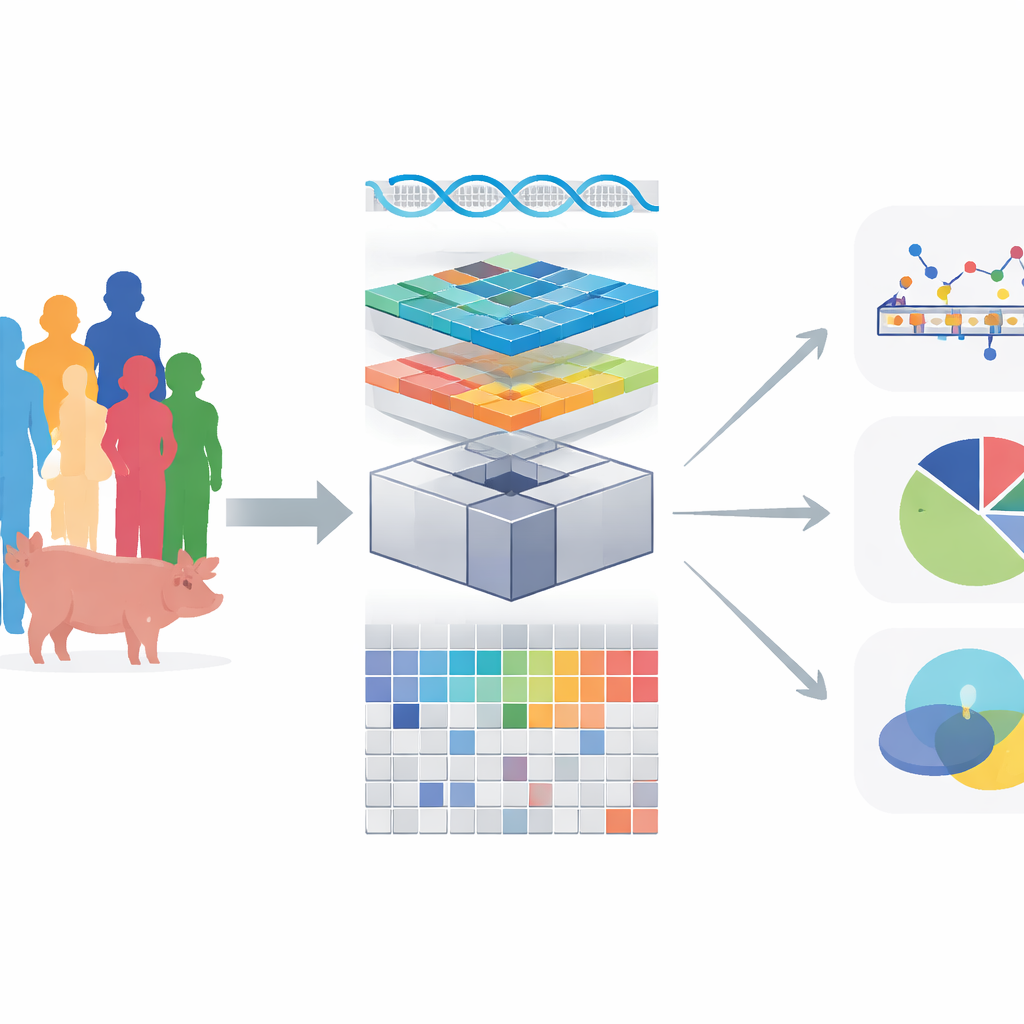
Von der DNA zu Schaltern, die Gene steuern
Anstatt nur äußere Merkmale wie Größe oder Fettgehalt zu betrachten, fragt das Mapping molekularer Merkmale, wie DNA‑Varianten interne Messgrößen verändern: welche Gene hoch- oder runterreguliert werden, wie RNA gespleißt wird und ähnliche Messungen über Tausende von Genen und Geweben hinweg. Stellen im Genom, die diese molekularen Messwerte beeinflussen, nennt man molekulare quantitative Trait‑Loci oder molQTLs. Ihre Identifizierung hilft, den Weg von DNA‑Änderung über Genregulation bis zu Krankheit oder Leistungsmerkmalen nachzuzeichnen. Gebräuchliche Werkzeuge vereinfachen jedoch oft die Statistik, um die Berechnungen handhabbar zu halten. Sie ignorieren häufig, wie eng Individuen verwandtschaftlich sind, oder wie ganze Genomabschnitte gemeinsam vererbt werden, was zu falsch positiven Signalen führen und echte Effekte verschleiern kann.
Warum Verwandtschaft ein statistisches Problem ist
In vielen Tierrassen und in Studien an menschlichen Familien teilen Individuen aufgrund jüngster gemeinsamer Vorfahren große DNA‑Segmente. Diese „komplexe Verwandtschaft“ kann dazu führen, dass zwei entfernte genetische Stellen fälschlich mit demselben molekularen Merkmal assoziiert erscheinen, nur weil sie gemeinsam vererbt werden, nicht weil beide tatsächlich das Gen regulieren. Standardlineare Modelle versuchen, dies durch einige zusammenfassende Abstammungsmaße zu korrigieren, haben aber Schwierigkeiten, wenn langreichweitige Korrelationen im Genom stark sind. Je verwandter die Population und je dichter die genetischen Daten, desto stärker blähen solche Vereinfachungen die scheinbare Signalstärke auf und erhöhen die Rate falscher Entdeckungen.
Eine zugeschnittene Engine für Omics‑skalierte Genetik
OmiGA basiert auf linearen gemischten Modellen, einer Klasse statistischer Werkzeuge, die Verwandtschaft handhaben, indem sie die hintergrundmäßige genetische Ähnlichkeit zwischen Individuen explizit modellieren. Die Autoren haben diese Modelle für Omics‑Daten umgebaut, bei denen Zehntausende molekularer Merkmale gegen Millionen DNA‑Varianten getestet werden. Sie führen neue Algorithmen ein, die die langsamsten Schritte herkömmlicher Methoden vermeiden, rechenintensive Zwischenergebnisse über viele Merkmale wiederverwenden und zusätzlich auf Grafikprozessoren ausgeführt werden können, um die Geschwindigkeit zu erhöhen. OmiGA schätzt zudem, wie viel eines molekularen Merkmals durch nahe DNA‑Veränderungen, entfernte Regionen und durch nicht‑additive Effekte, bei denen Genkopien komplexer miteinander interagieren, erklärt wird. Zusammengenommen verwandeln diese Eigenschaften einen früher umständlichen Ansatz in ein praktikables Arbeitspferd für große Studien. 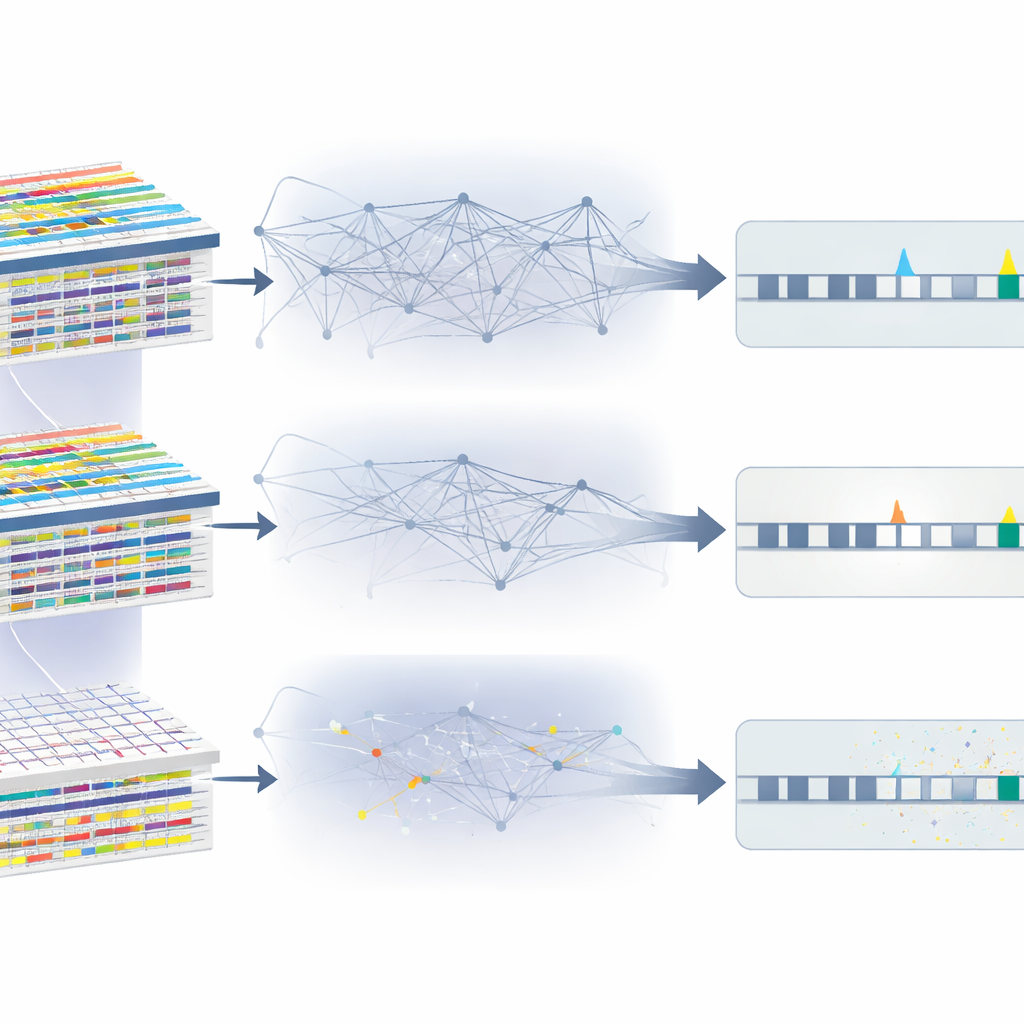
Scharfere Signale in Simulationen und realen Datensätzen
Das Team verglich OmiGA mit populären Werkzeugen wie tensorQTL, APEX, GCTA und LDAK anhand von simulierten Daten und echten Messungen aus Schwein‑ und Menschendaten. In Simulationen, die eng verwandte Schweinepopulationen und locker verwandte menschliche Kohorten nachahmen, hielt OmiGA konsistent das Hintergrundrauschen unter Kontrolle und bewahrte oder steigerte die Rate echter Entdeckungen. In realen Schweingewebedaten identifizierte OmiGA deutlich mehr Gene, deren Expression klar mit nahen DNA‑Varianten verknüpft ist, und das bei geringeren Rechenkosten. Außerdem ergaben sich engere Mengen wahrscheinlicher kausaler Varianten bei der Fokussierung auf spezifische Regionen, und es zeigte sich eine stärkere Übereinstimmung zwischen molekularen Signalen und traditionellen Merkmalassoziationsergebnissen, was darauf hindeutet, dass OmiGA besser darin ist, die tatsächlichen regulatorischen Veränderungen hinter komplexen Merkmalen zu lokalisieren.
Neue Einsichten zu Dominanz- und Kontext‑Effekten
Über standardmäßige „additive“ Effekte hinaus, bei denen jede Genkopie unabhängig beiträgt, kann OmiGA dominierende Effekte modellieren, bei denen eine Kopie die andere maskieren oder verstärken kann. Bei Anwendung auf menschliche Zell‑Daten fanden die Autoren, dass viele Gene mit klassischen Effekten auch versteckte dominante Einflüsse tragen, und in einigen Fällen tritt dominante Regulation dort auf, wo additive Effekte nicht sichtbar sind. OmiGA erkennt außerdem kontextabhängige Regulation, etwa genetische Effekte, die je nach Abstammung oder Umwelt variieren, und teilt die Heritabilität in lokale und fernere Komponenten auf. Diese Fähigkeiten eröffnen ein reichhaltigeres Bild davon, wie DNA‑Variation die molekulare Biologie in vielfältigen Populationen formt.
Was das für die Zukunft bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: OmiGA bietet ein zuverlässigeres Mikroskop, um zu sehen, wie DNA‑Unterschiede die Genaktivität einstellen, besonders in realen Populationen, in denen Verwandte häufig sind. Durch die Reduktion falscher Signale und die Hervorhebung tatsächlich kausaler Varianten hilft es, molekulare Veränderungen sicherer mit Merkmalen wie Krankheitsrisiko oder Fleischqualität zu verbinden. Das kann Folgeexperimente schärfen, Zuchtentscheidungen in der Landwirtschaft verbessern und die Interpretation humaner Genstudien stärken, indem es genau aufzeigt, welche regulatorischen Schalter im Genom am wichtigsten sind.
Zitation: Teng, J., Zhang, W., Gong, W. et al. OmiGA for ultra-efficient molecular quantitative trait loci mapping. Nat Commun 17, 2680 (2026). https://doi.org/10.1038/s41467-026-68978-0
Schlüsselwörter: Mapping molekularer QTL, Genexpressionsregulation, lineare gemischte Modelle, genetische Verwandtschaft, Omics‑Werkzeugkasten