Clear Sky Science · de
VSIG10L ist ein wichtiger Faktor für die Homöostase der Speiseröhre und die erbliche Veranlagung für Barrett-Ösophagus
Warum das für Menschen mit Sodbrennen wichtig ist
Chronisches Sodbrennen ist weit verbreitet, doch nur ein kleiner Teil der Betroffenen entwickelt einen Barrett-Ösophagus, eine Erkrankung, die zu Speiseröhrenkrebs führen kann. Diese Studie stellt eine einfache, aber wichtige Frage: Warum sind manche Familien deutlich anfälliger für Barrett-Ösophagus als andere? Indem die Forschenden ein einzelnes Gen nachvollziehen und beobachten, wie es die Auskleidung der Speiseröhre beim Menschen und bei Mäusen formt, decken sie eine fehlende Verbindung auf zwischen erblich bedingtem Risiko, Refluxschäden und der Fähigkeit des Körpers, die Speiseröhre gesund zu erhalten.
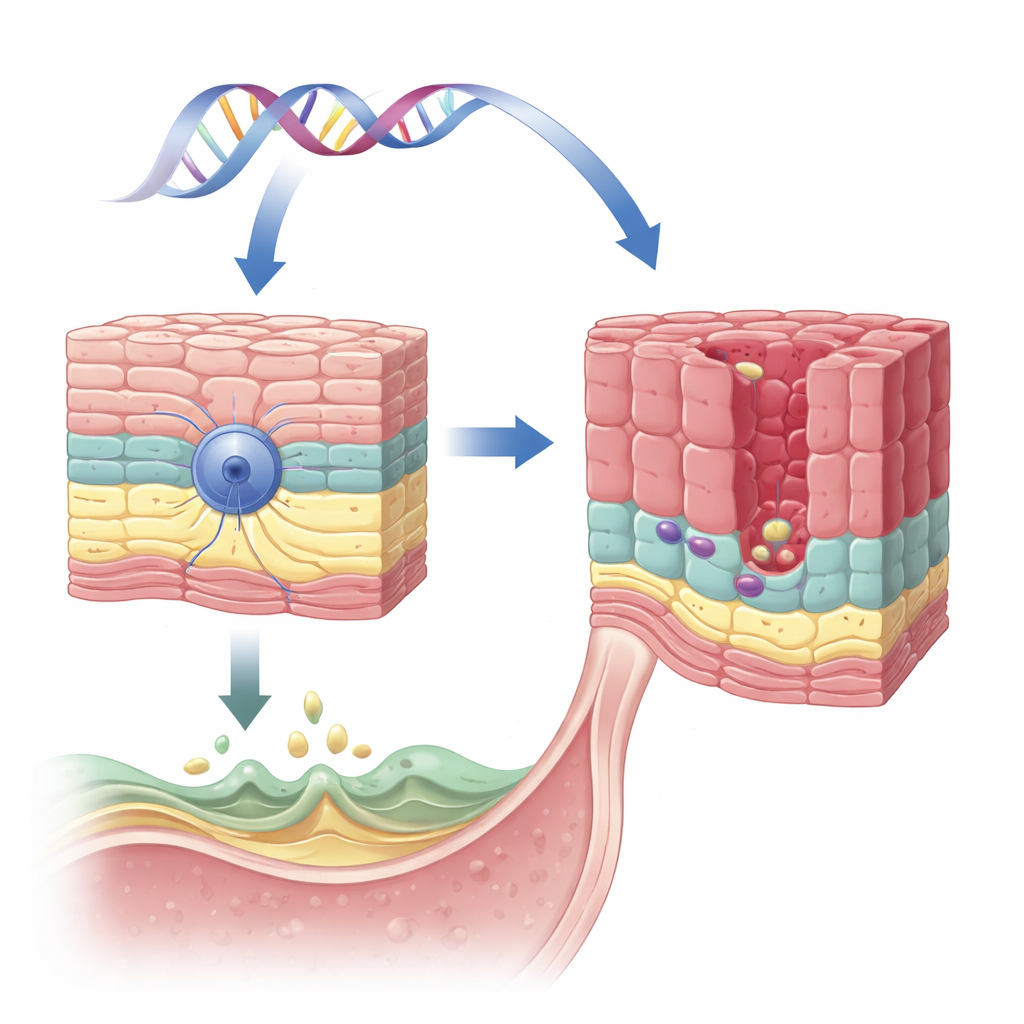
Ein schützendes Gen in der Speiseröhrenschleimhaut
Das Team konzentrierte sich auf ein Gen namens VSIG10L, das zuvor in einer großen Familie mit vielen Fällen von Barrett-Ösophagus und verwandten Krebserkrankungen aufgefallen war. VSIG10L ist in den oberen Schichten der platten (plattenepithelialen) Zellen der Speiseröhre aktiv, nicht jedoch in den tiefer liegenden, stammzellähnlichen basalen Zellen. Mit einer empfindlichen RNA-Nachweismethode in menschlichem, Schweine- und Mausgewebe sowie in dreidimensionalen Kulturen menschlicher Speiseröhrenzellen zeigten die Forschenden, dass VSIG10L beständig nur in den „reifenden“ Zellen direkt oberhalb der Basalschicht eingeschaltet ist. Dieses Muster legt nahe, dass VSIG10L den platten Epithelzellen hilft, die letzten Schritte der Reifung zu durchlaufen und eine stabile Barriere zu bilden.
Erbliche Veränderungen, die die Barriere schwächen
Durch Sequenzierung des VSIG10L-Gens bei 684 Personen aus 302 Familien mit Barrett-Ösophagus und Speiseröhrenkrebs entdeckten die Untersucher mehrere seltene, schädliche Varianten. Um zu testen, was diese Varianten bewirken, erzeugten sie aus Stammzellen des Patienten mit einer solchen Mutation Speiseröhren-Organoide. Im Vergleich zu Organoiden eines gesunden Spenders konnten die mutierten Organoide nicht die normale, geschichtete Plattenstruktur aufbauen. Stattdessen bildeten sie häufig abnorme, drüsenähnliche Zellknäuel, die in einem basalen, unreifen Zustand verharrten und durch das Protein p63 gekennzeichnet waren. Diese Verzerrung der normalen Schichtung und Reifung spiegelt frühe Schritte wider, die bei Patienten als Vorstufe des Barrett-Ösophagus vermutet werden.
Mausmodelle, die die menschliche Erkrankung nachvollziehen
Um über Zellkulturen hinauszugehen, erzeugte das Team Mäuse, die entweder eine präzise Kopie der familiären menschlichen VSIG10L-Mutation tragen oder einen vollständigen Verlust des Gens. Bei gesunden Mäusen ist das entsprechende Vsig10l-Gen wieder nur in suprabasalen Plattenepithelzellen aktiv. Unter dem Elektronenmikroskop zeigten die mutierten Mäuse einen auffälligen Verlust von Desmosomen—den winzigen „Nieten“, die benachbarte Zellen zusammenhalten—in diesen Schichten. Transkriptionskarten aus dem plattenförmigen Magen (forestomach), einem Mausgebiet, das dem unteren Teil der Speiseröhre ähnelt, zeigten eine weitreichende Störung von Struktur- und Differenzierungsprogrammen. Wenn die Mäuse mit einer Nahrung gefüttert wurden, die die Gallensäure Desoxycholat enthielt, um chronischen Reflux zu simulieren, entwickelten 70–100 % der Vsig10l-mutierten Tiere großflächige, Barrett-ähnliche, mukinreiche Herde an der Übergangszone zwischen plattem und zylindrischem Epithel, während Wildtyp-Mäuse nur kleine, begrenzte Läsionen zeigten.
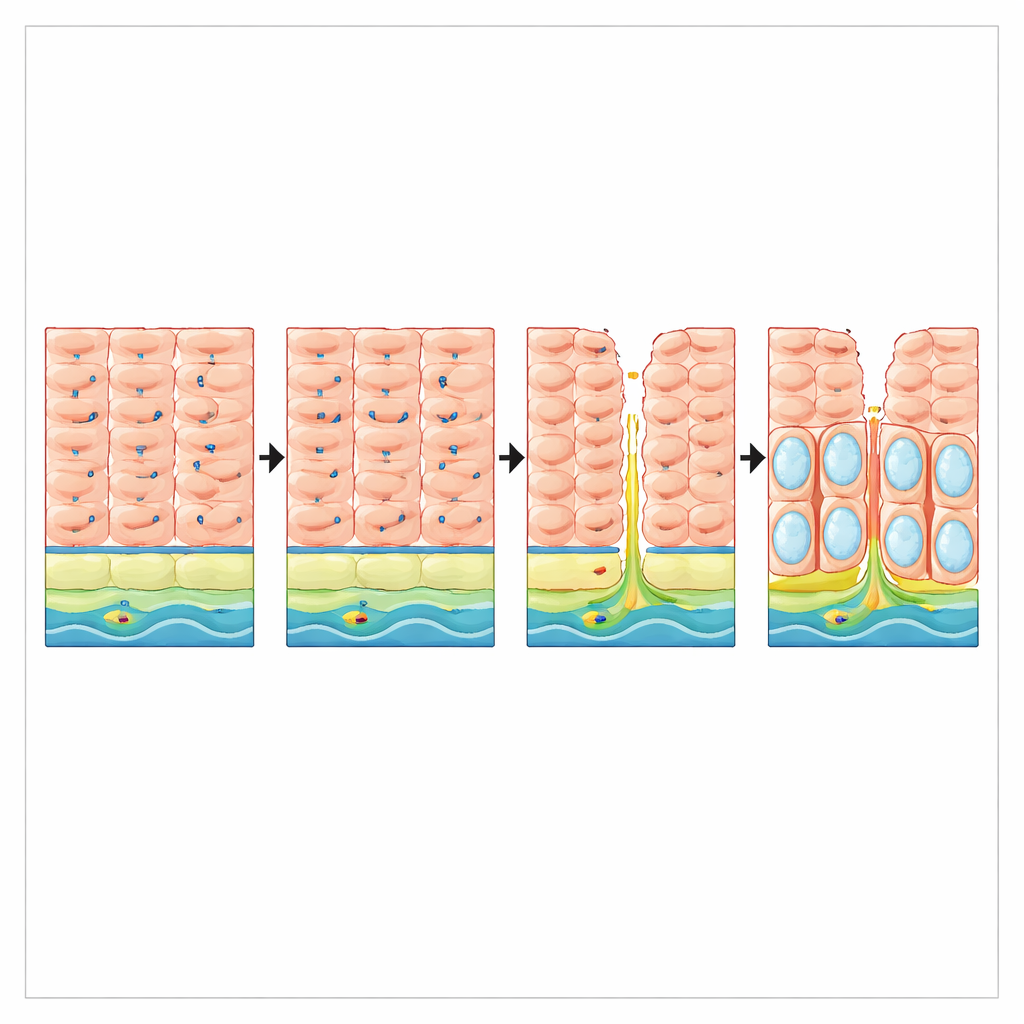
Refluxschaden und Schutzverlust bei Patienten
Die Forschenden fragten dann, ob Reflux selbst VSIG10L beim Menschen stören könnte. In Biopsien von Patienten mit langjähriger gastroösophagealer Refluxkrankheit, aber ohne Barrett-Ösophagus, lagen die VSIG10L-RNA-Spiegel etwa dreimal niedriger als bei Personen ohne Reflux, obwohl der grundlegende Plattenepithelmarker TP63 unverändert war. In Gewebeschnitten zeigte die gesunde Speiseröhrenschleimhaut einen klaren Streifen von VSIG10L-positiven Zellen oberhalb einer Basalschicht. Im Gegensatz dazu wies refluxgeschädigte Mukosa eine Ausweitung basaloider, p63-reicher Zellen und einen nahezu vollständigen Verlust des VSIG10L-positiven Differenzierungsgradienten auf. Diese Befunde deuten darauf hin, dass chronischer Reflux nicht nur die physische Integrität der Schleimhaut angreift, sondern auch das Genprogramm, das ihre geordnete Erneuerung aufrechterhält.
Die Teile zusammensetzen
Zusammenfassend stützt die Arbeit ein einfaches Modell: VSIG10L ist ein zentraler Wächter der plattenepithelialen Barriere der Speiseröhre. Erbliche Defekte in diesem Gen oder erworbene Unterdrückung durch chronischen Reflux führen zu einer mangelhaften Reifung der Schleimhaut, weniger Zell‑Zell‑Verbindungen und einer durchlässigeren Oberfläche. In diesem verletzlichen Zustand fördert wiederholte Einwirkung von Säure und Galle eine abnorme, drüsenähnliche Heilung, statt die ursprüngliche Plattenepithel‑Auskleidung wiederherzustellen, und schafft damit die Grundlage für Barrett-Ösophagus. Für Patientinnen und Patienten sowie Familien weist diese Forschung auf mögliche künftige Gentests hin, die Hochrisikopersonen identifizieren könnten, und auf neue Therapien, die darauf abzielen, VSIG10L-Funktion zu erhalten oder wiederherzustellen, mit dem langfristigen Ziel, Barrett-Ösophagus und dessen Progression zu Krebs zu verhindern.
Zitation: Ravillah, D., Singh, S., Katabathula, R.M. et al. VSIG10L is a major determinant of esophageal homeostasis and inherited predisposition to Barrett’s esophagus. Nat Commun 17, 2167 (2026). https://doi.org/10.1038/s41467-026-68975-3
Schlüsselwörter: Barrett-Ösophagus, gastroösophagealer Reflux, genetische Veranlagung, epitheliale Homöostase, Risiko für Speiseröhrenkrebs