Clear Sky Science · de
Photoinduzierte, polaritätsnichtübereinstimmende Umwandlungen von Isochinolinen in Naphthalene
Neue Wege für Medikamente beleuchten
Viele moderne Medikamente bestehen aus flachen, ringförmigen Kohlenstoffgerüsten. Das Austauschen eines Ringkerns durch einen anderen kann das Verhalten eines Wirkstoffs im Körper drastisch verändern, erfordert aber meist lange und teure Synthesewege. Diese Studie stellt eine lichtgetriebene Abkürzung vor: ein Verfahren, das einen häufigen, stickstoffhaltigen Ring—das Isochinolin—direkt in einen eng verwandten rein kohlenstoffhaltigen Ring, ein Naphthalin, umformt. Die Methode arbeitet unter milden Bedingungen, verträgt viele funktionelle Gruppen und lässt sich spät im Lebenszyklus eines Wirkstoffmoleküls anwenden, was schnellere Wege zu verbesserten Wirkstoffen eröffnet.
Warum der Ringkerntausch wichtig ist
In der Wirkstoffforschung bauen Chemiker große Bibliotheken verwandter Moleküle auf und testen sie, um Eigenschaften wie Wirksamkeit, Selektivität und Stabilität zu optimieren. Schon der Austausch eines einzelnen Atoms im Zentralring kann stark beeinflussen, wie eine Verbindung an ihr biologisches Ziel bindet oder wie lange sie im Körper bestehen bleibt. Isochinoline und Naphthaline sind klassische Beispiele für solche austauschbaren „Look‑alike“‑Kerne: Sie haben ähnliche Größe und Form, tragen aber unterschiedlich ein Stickstoffatom beziehungsweise nur Kohlenstoff. Traditionell erfordert der Wechsel von einem Kern zum anderen den Neuaufbau des Moleküls in vielen mühsamen Schritten. Eine direkte One‑Step‑Umwandlung zwischen beiden würde es erlauben, vorhandene Moleküle in neue Varianten zu überführen, statt bei null zu beginnen.
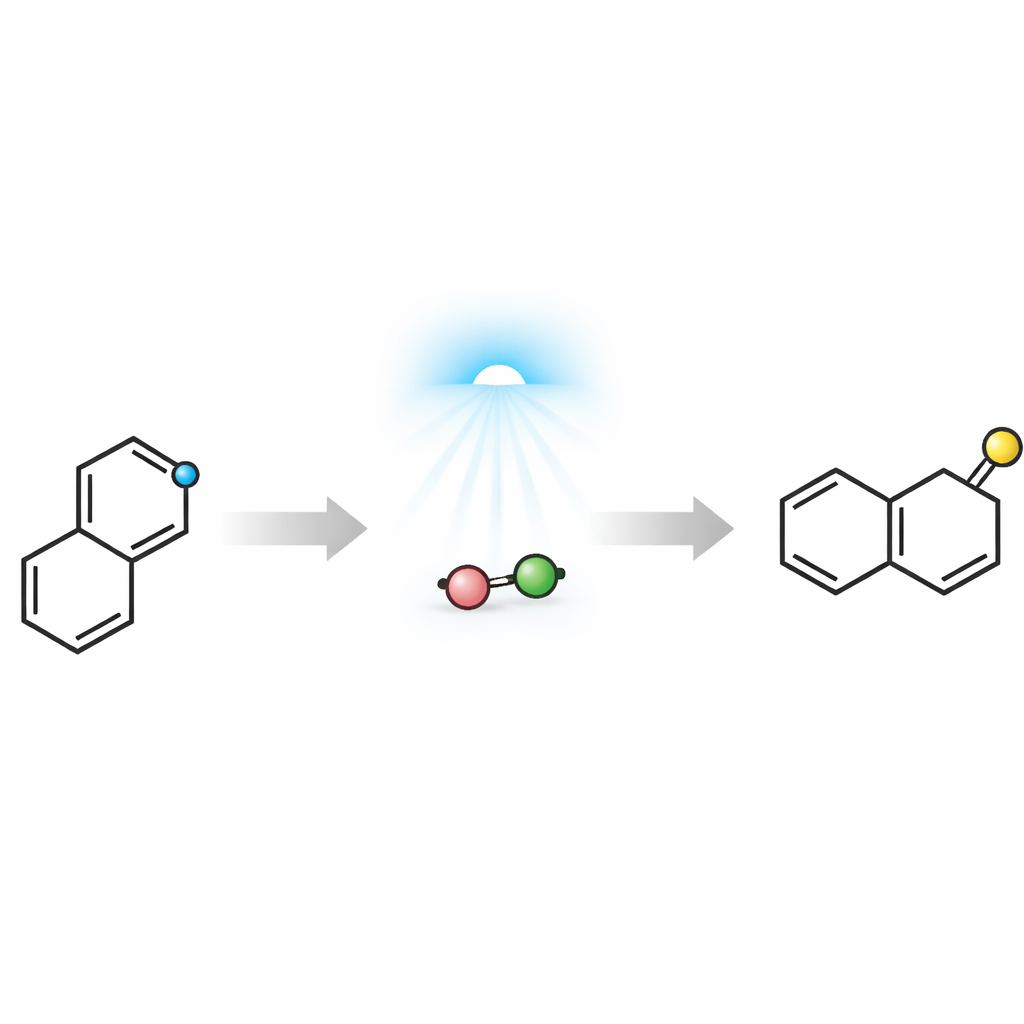
Elektronische Unverträglichkeit als Vorteil nutzen
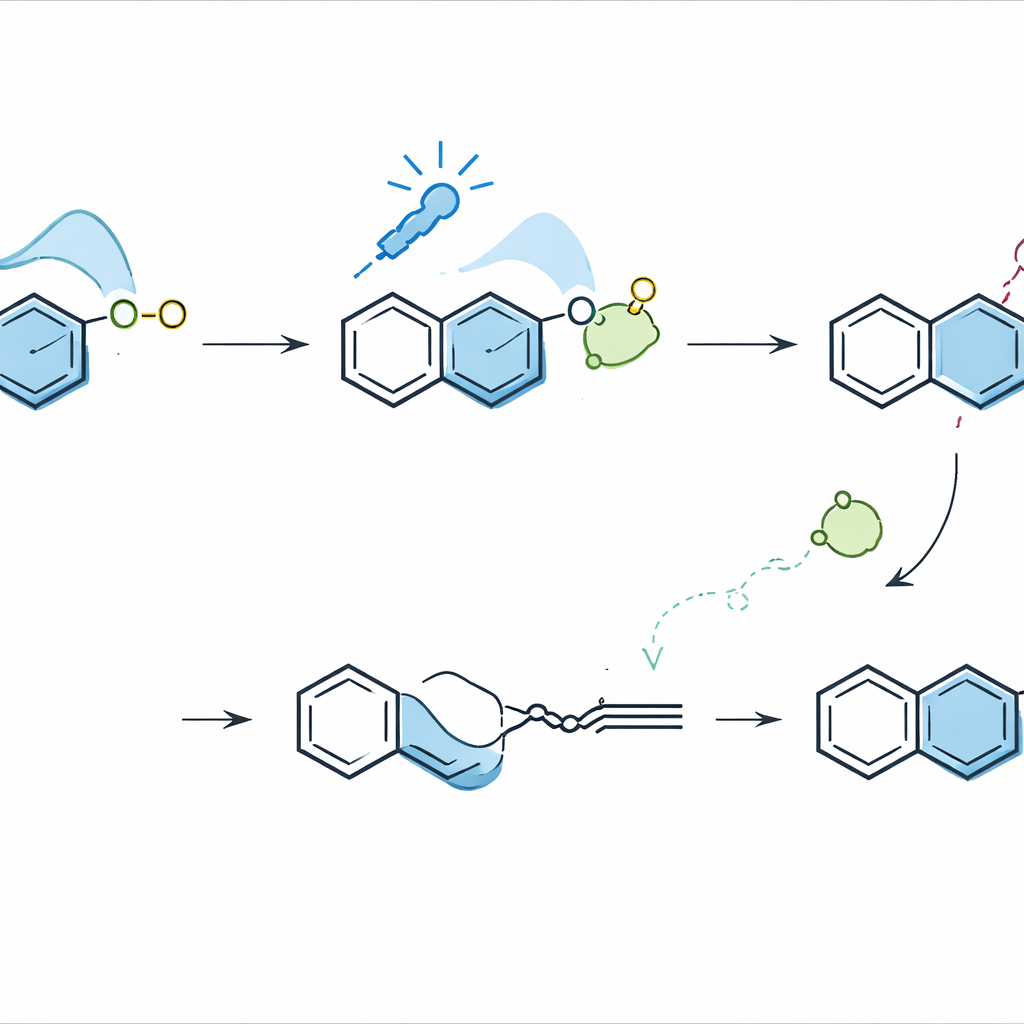
Die Herausforderung besteht darin, dass Isochinoline und die Alkine, aus denen Naphthaline aufgebaut werden, beide relativ elektronenvonarm sind und sich daher normalerweise im entscheidenden Bindungsbildungs‑Schritt—einer sechsgliedrigen Ringbildungsreaktion—abstoßen. Die Autoren überwanden diese „Polaritäts‑Mismatch“ durch Einsatz sichtbaren Lichts und einer einfachen anorganischen Base. Wird ein Isochinolin in ein Salz überführt und mit Carbonat gepaart, bilden die beiden eine lockere Assoziation, die blaues Licht absorbieren kann. Rechnerische Studien leiteten das Design und zeigten, dass Lichtanregung ein Elektron vom Carbonat auf den Isochinoliniumsring verschiebt und diesen vorübergehend in ein elektronenreiches Radikal verwandelt. In diesem aktivierten Zustand kann das Isochinolin schrittweise an ein elektronenvonarmes Alkin addieren, ein neues Ringsystem bilden und sich letztlich in ein Naphthalin umarrangieren, wobei ein stickstoffhaltiger Fragment abgespalten wird.
Reaktionsuntersuchungen im Labor
Experimentell ist die Umwandlung einfach durchzuführen: Isochinoliniumsalze, Alkine und Natriumcarbonat werden in Ethanol unter blauen LEDs gerührt, ohne zusätzlichen Photokatalysator. Das Team optimierte die Bedingungen und zeigte, dass Carbonat nicht nur als Base, sondern auch als Elektronendonor entscheidend ist und dass Bromidionen den Prozess fördern. Radikalfänger schalten die Reaktion aus und fingen Zwischenaddukte ein, was den durch Rechnungen vorgeschlagenen Radikalweg stützt. Spektroskopische Experimente bestätigten, dass das Isochinoliniumsalz–Carbonat‑Paar das eigentliche lichtabsorbierende Komplex ist; ein Wechsel von Gegenionen oder Basen veränderte die Ausbeuten auf eine Weise, die mit ihrer Fähigkeit zum Elektronentransfer übereinstimmt.
Von Modellsystemen zu wirkstoffähnlichen Molekülen
Nach Feinabstimmung der Reaktionsbedingungen zeigten die Autoren eine breite Anwendbarkeit. Viele unterschiedlich substituierte Alkine reagierten mit, einschließlich solcher mit empfindlichen Gruppen wie Iod, zusätzlichen Doppelbindungen oder Fragmenten aus Naturstoffen bzw. bestehenden Arzneistoffen. Eine große Palette an Isochinoliniumsalzen funktionierte ebenfalls, selbst stark sterisch gehinderte oder heterozyklische Substrate, was Zugang zu mehrfach substituierten Naphthalinen ermöglicht, die auf traditionellen Wegen schwer zugänglich sind. Die Methode konnte sogar komplexe bioaktive Moleküle wie den PRMT3‑Inhibitor SGC707 und das Vasospasm‑Medikament Fasudil in einem einzigen späten Schritt in ihre Naphthalin‑Analoga überführen. Die neuen Produkte tragen Estergruppen, die sowohl als mögliche Proteinbindungsstellen als auch als vielseitige synthetische Eingangsstellen dienen.
Größere Architekturen aus den neuen Ringen aufbauen
Die frisch hergestellten Naphthalin‑ester sind nicht nur Endpunkte; sie dienen als Bausteine für komplexere Strukturen. Das Team demonstrierte mehrere Folgeumwandlungen, die diese Ester in wertvolle polyzyklische aromatische Kohlenwasserstoffe und chirale Liganden überführen, etwa Benzofluorenone, Carbazole, BINOLs und QUINOLs—Gerüste, die in der Materialwissenschaft und asymmetrischen Katalyse weithin verwendet werden. In einer weiteren Demonstration nutzten sie die Methode als Schlüsselschritt zur Herstellung eines Adapalen‑Analogons, eines Dermatologika, aus einem leicht zugänglichen Isochinolin‑Vorläufer.
Was das für die Zukunft bedeutet
Durch den Einsatz sichtbaren Lichts, um den elektronischen Charakter eines stickstoffhaltigen Rings umzukehren, verwandelt diese Arbeit eine zuvor ungünstige Reaktion in ein leistungsfähiges Werkzeug des Skelett‑Editings. Chemiker können nun reich funktionalisierte Naphthaline direkt aus weit verbreiteten Isochinolinen erzeugen, lange Synthesestrecken umgehen und empfindliche Seitenketten bewahren. Für Nicht‑Spezialisten lautet die Quintessenz: Das „Recyceln“ bestehender Moleküle in neue Kernstrukturen wird praktikabler, was die Suche nach besseren Arzneimitteln und fortschrittlichen Materialien beschleunigen und zugleich Kosten und Abfall reduzieren könnte.
Zitation: Zhang, C., Zhang, J., Lan, Y. et al. Photoinduced polarity-mismatched transformations of isoquinolines into naphthalenes. Nat Commun 17, 2547 (2026). https://doi.org/10.1038/s41467-026-68969-1
Schlüsselwörter: Skelett‑Editing, Photochemie, Isochinolin, Naphthalin, Arzneimittelentwicklung