Clear Sky Science · de
FANCD2 bremst Gabelprogression und verhindert Bruchstellen an frühen Origins bei Re-Replikation
Wenn DNA-Kopien leicht vom Drehbuch abweichen
Jedes Mal, wenn sich eine Zelle teilt, muss sie ihre gesamte DNA-Bibliothek genau einmal kopieren. Werden Teile dieser Bibliothek zweimal kopiert oder in hastiger, schlampiger Weise vervielfältigt, können Chromosomen brechen und Mutationen entstehen, die Krebs vorantreiben. Diese Studie untersucht, was passiert, wenn die zellulären Schutzmechanismen gegen zusätzliche Kopierrunden versagen, und zeigt, wie ein Reparaturprotein namens FANCD2 eingreift, um leicht fehlregulierte Zellen daran zu hindern, in ein vollständiges genomisches Chaos zu rutschen.
Leitplanken für eine saubere Kopie
Unsere Chromosomen werden von tausenden Startpunkten oder „Origins“ dupliziert, die lizenziert und dann in einer sorgfältig getimten Reihenfolge aktiviert werden. Ein kleines Protein namens Geminin sorgt normalerweise dafür, dass jeder Origin nur einmal pro Zellzyklus feuert. Geht Geminin verloren oder wird es geschwächt, können einige Origins erneut auf bereits kopierter DNA aktiv werden — ein Zustand, der als Re-Replikation bezeichnet wird. Krebszellen, die oft zu viele Lizenzierungsfaktoren produzieren, sind besonders anfällig für dieses Problem. Die Autoren führten zunächst einen hochskaligen genetischen Screen in menschlichen Zellen durch, die durch Geminin-Depletion für eine geringfügige Re-Replikation präpariert waren. Sie fragten, welche DNA-Reparatur- und Checkpoint-Gene unter diesem Stresszustand entscheidend werden, und fanden, dass FANCD2, bekannt vor allem für die Reparatur von DNA-Querbrücken bei der Fanconi-Anämie, als zentraler Schutzfaktor für Zellüberleben und Genomintegrität hervorging.
Ein Ersthelfer an überlasteten Replikationsmaschinen
Das Team verfolgte anschließend, wo und wann FANCD2 in Zellen auftritt, die Re-Replikation durchlaufen. Kurz nachdem Geminin entfernt wurde, reichert sich FANCD2 rasch am Chromatin an und bildet helle Kernfoci, noch bevor großflächige DNA-Brüche nachweisbar sind. Durch Markierung neu synthetisierter DNA zusammen mit proximitätsbasierten Assays zeigten sie, dass FANCD2 direkt an aktiven Replikationsmaschinen rekrutiert wird, insbesondere in Zellen, deren DNA bereits ein zweites Mal kopiert wird. In synchronisierten Zellen, die in den nächsten Teilungszyklus entlassen wurden, trat eine deutliche Population mit einem diffusen Muster übermäßiger Replikation auf. Diese Zellen zeigten starke FANCD2- und RPA-Signale, was auf anhaltenden Replikationsstress hindeutet, und wurden durch einen aktiven Checkpoint vor der Mitose angehalten, was darauf hindeutet, dass FANCD2 Teil einer frühen Reaktion ist, die gestresste Gabeln stabilisiert, statt nur auf gebrochene DNA zu reagieren.
Das Zurückhalten entfesselter Gabeln und verborgener Lücken
Um zu testen, wie FANCD2 die DNA-Kopie beeinflusst, kombinierten die Forscher den Verlust von Geminin mit der Depletion von FANCD2. Überraschenderweise erhöhte das Entfernen von FANCD2 nicht den Anteil der Zellen mit offensichtlich re-replizierten Genomen. Stattdessen zeigten Einzelmolekül-DNA-Faser-Assays, dass Replikationsgabeln weiter vorrückten und asymmetrischer wurden, ein Hinweis auf ungleichmäßige und instabile Progression. Diese schnelleren Gabeln hinterließen mehr einzelsträngige Lücken in der neu synthetisierten DNA, sichtbar als intensive RPA- und native BrdU-Foci und bestätigt durch die Empfindlichkeit markierter Trakte gegenüber einem Enzym, das einzelsträngige Regionen schneidet. Zellen, denen sowohl Geminin als auch FANCD2 fehlten, zeigten einen Anstieg an Chromosomenbrüchen, Fragmenten, Kernkörperchen und Mikronuklei — alles Kennzeichen schwerer genomischer Instabilität. Die Blockade von PARP, einem Faktor, der diese Lücken normalerweise hilft zu managen, ahmte diese Defekte nach und verschlimmerte sie, was unterstreicht, dass die unkontrollierte Bildung von Lücken zentral für den Schaden ist.
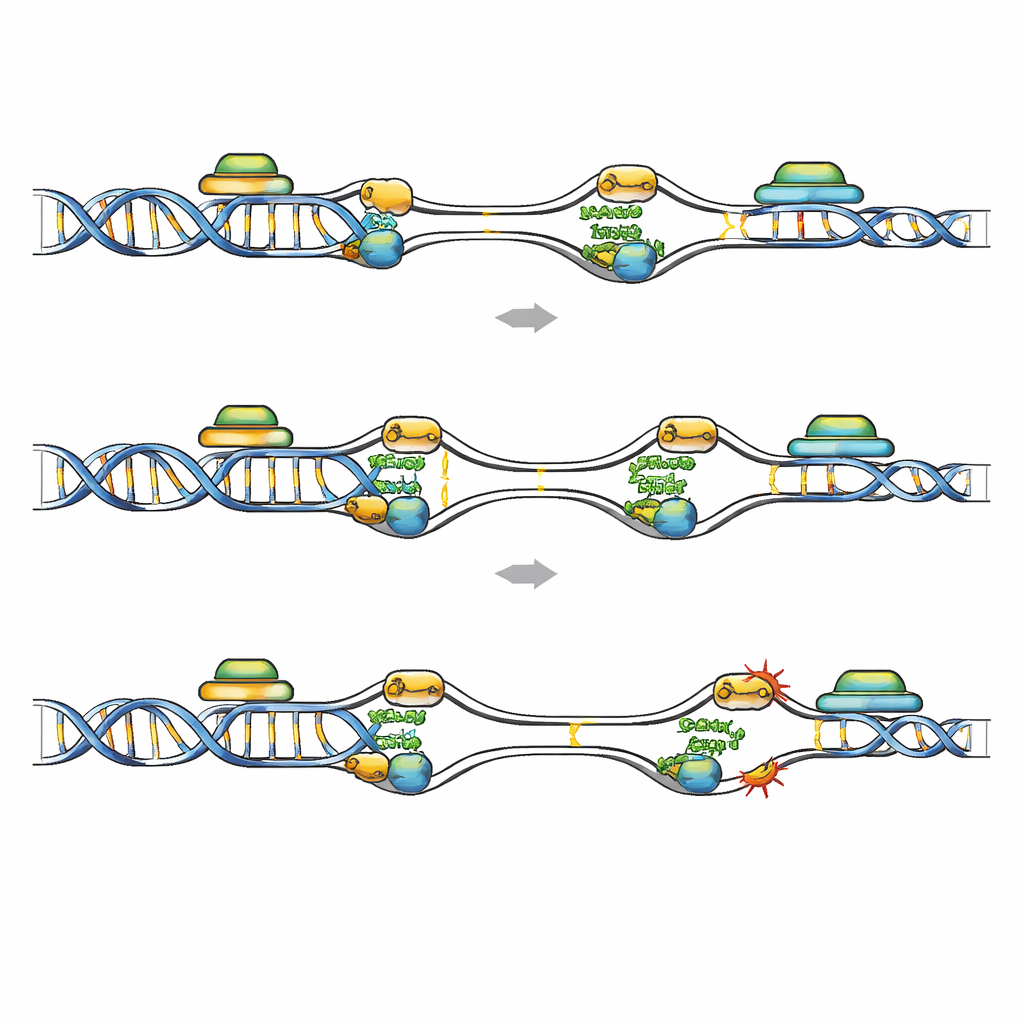
Fragile Hotspots, wo Kopieren und Ablesen kollidieren
Eine genomweite Kartierung der FANCD2-Bindung ergab, wo Re-Replikation am gefährlichsten ist. In leukämischen Zellen mit Geminin-Depletion verlagerte sich FANCD2 von klassischen common fragile sites zu früh-aktivierten Replikationsorigins, die in kurzen, GC-reichen, stark transkribierten Genen liegen. Diese Regionen tragen Merkmale aktiver Transkription und neigen zu R-Loops, bei denen naszierende RNA mit der DNA-Vorlage hybridisiert und so die Replikation blockieren kann. Öffentliche Datensätze zeigten mehr DNA-Schäden und erhöhte RNA–DNA-Hybrid-Signale in FANCD2-angereicherten Genen nach Geminin-Verlust, und diese Regionen überschneiden sich mit sogenannten early replicating fragile sites. Wird die Transkription allgemein mit einem Medikament gedämpft oder werden R-Loops spezifisch durch Überexpression von RNase H1 entfernt, sinkt die Anzahl der FANCD2-, RPA- und DNA-Schadensfoci in Geminin-defizienten Zellen deutlich. Das deutet darauf hin, dass Kollisionen zwischen erneut feuerten Origins und aktiven Transkriptionseinheiten, verstärkt durch R-Loops, fragile Hotspots schaffen, die FANCD2 schützen muss.
Feinabstimmung des Schutzes durch chemische Markierungen
FANCD2 wird teilweise durch die Anheftung eines kleinen ubiquitinähnlichen Tags aktiviert. Durch Depletion von FANCA, einer Kernkomponente der Markierungsmaschinerie, und durch Verwendung von Zellen, die eine FANCD2-Mutation exprimieren, die gegen diese Modifikation resistent ist, zeigten die Autoren, dass Mono-Ubiquitinierung das Überleben re-replizierender Zellen verbessert, aber nicht absolut erforderlich ist. Selbst nicht markiertes FANCD2 bot einen teilweisen Schutz, was mit unterschiedlichen Rollen beim Erkennen und Stabilisieren gestresster Gabeln vereinbar ist. Das Gesamtbild ist, dass FANCD2 hilft, die Replikation an anfälligen frühen Origins zu verlangsamen und zu organisieren und begrenzt, wie viele und wie groß die einzelsträngigen Lücken werden.
Warum das für die Krebstherapie wichtig ist
Für Nicht-Spezialisten lautet die Kernbotschaft, dass nicht alle Replikationsfehler von Anfang an katastrophal sind. Milde Re-Replikation, wie sie in einigen Tumoren vorkommt, kann toleriert werden, wenn Schutzsysteme wie FANCD2 das entfesselte DNA-Kopieren in Schach halten und verhindern, dass fragile Lücken zu gebrochenen Chromosomen werden. Wird diese Schutzfunktion entfernt oder überfordert, eskalieren dieselben geringfügigen Lizenzierungsfehler schnell zu einer Zerschmetterung des Genoms. Da Geminin-Verlust und Defekte in der Replikationslizenzierung in Krebszellen gehäuft auftreten und viele Tumoren bereits Schwächen im Fanconi/BRCA-Netzwerk aufweisen, deuten die hier aufgedeckten Verwundbarkeiten auf therapeutische Strategien hin: Die Kombination von Inhibitoren, die Krebszellen zur Re-Replikation treiben, mit Medikamenten, die die Akkumulation von Lücken verschärfen — etwa PARP-Inhibitoren — könnte bösartige Zellen selektiv über ihre Toleranzgrenze treiben, während normale Zellen mit intaktem Schutz verschont bleiben.
Zitation: Badra-Fajardo, N., Karydi, E., Bayona-Feliu, A. et al. FANCD2 restrains fork progression and prevents fragility at early origins upon re-replication. Nat Commun 17, 2478 (2026). https://doi.org/10.1038/s41467-026-68966-4
Schlüsselwörter: DNA-Replikationsstress, FANCD2, Geminin, Re-Replikation, Genomintegrität