Clear Sky Science · de
Assoziationsinduzierte Faltung steuert den Zusammenbau der Surrogat-Leichtkette und des Vor-B-Zell-Rezeptor-Kerns
Wie unser Körper neue Antikörper auf Probefahrt schickt
Bevor eine junge B-Zelle im Knochenmark ins Immunsystem aufgenommen wird, muss sie einen harten Test bestehen: Kann sie einen funktionierenden Antikörperkern aufbauen? Dieses Paper untersucht, wie eine spezielle "Probeversion" eines Antikörperteils, die sogenannte Surrogat-Leichtkette, bei diesem Test hilft. Indem die Autoren beobachten, wie diese Proteine falten und zusammenpassen, offenbaren sie ein verstecktes Qualitätskontrollsystem, das entscheidet, welche zukünftigen Antikörper gut genug sind, um behalten zu werden — und welche verworfen werden.
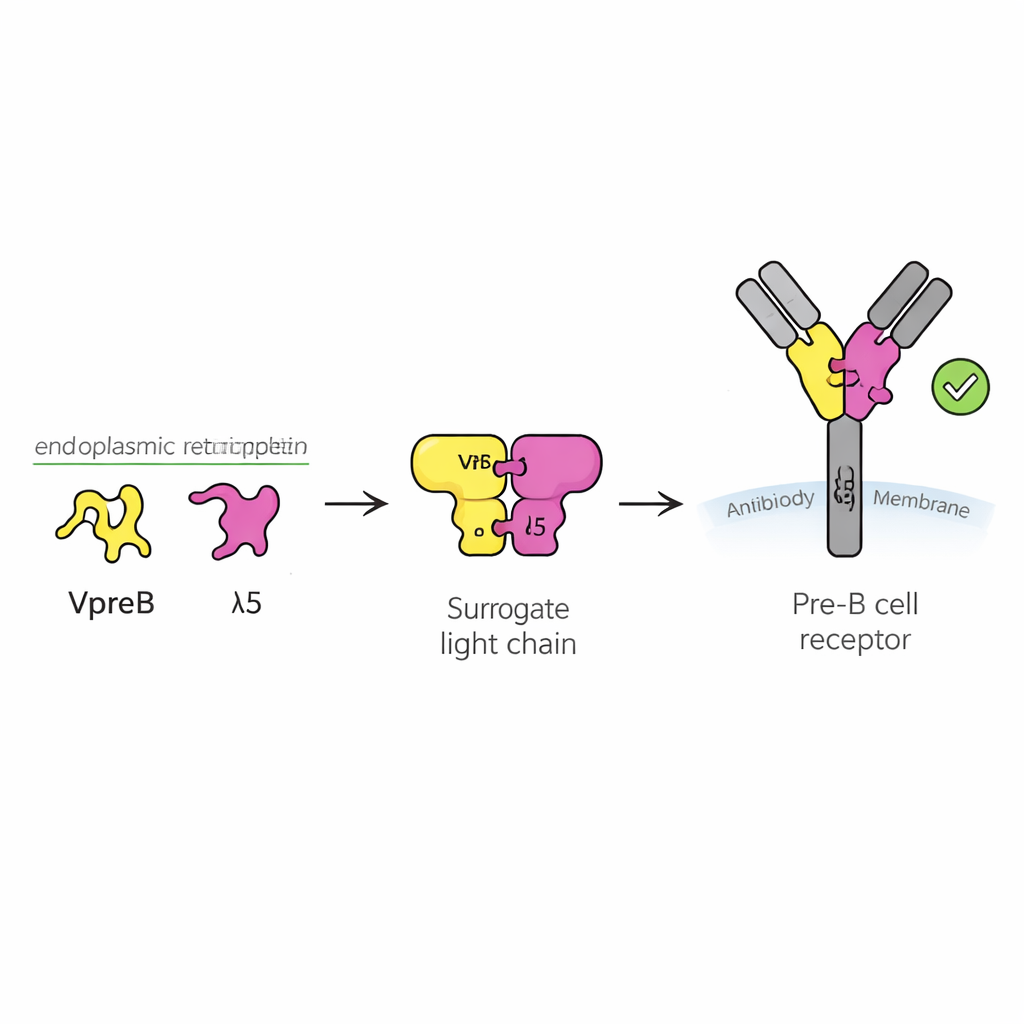
Eine Sicherheitsprüfung für junge Immunzellen
Antikörper sind Y‑förmige Proteine, die Eindringlinge erkennen. Sie bestehen aus zwei Hauptteilen: schweren Ketten und leichten Ketten. Während der B-Zell-Entwicklung wird die schwere Kette zuerst hergestellt, und die Zelle muss feststellen, ob diese neue schwere Kette nützlich ist, bevor sie Energie in die Produktion einer passenden leichten Kette investiert. Dazu verwendet die Zelle einen temporären Ersatz, die Surrogat-Leichtkette, bestehend aus zwei Proteinen namens VpreB und λ5. Zusammen mit der schweren Kette bilden sie den Vor-B-Zell-Rezeptor, einen Sensor an der Zelloberfläche, der ein "Weiter"- oder "Stop"-Signal sendet. Etwa die Hälfte der neu umgeordneten schweren Ketten scheitert an diesem Test, weshalb das Verständnis der Funktionsweise der Surrogat-Leichtkette entscheidend dafür ist, wie ein gesundes Antikörperrepertoire entsteht.
Faltung durch Assoziation: einem instabilen Partner helfen
Die Autoren fanden heraus, dass eine Komponente, VpreB, allein weitgehend entfaltet und instabil ist. Mit biophysikalischen Methoden zeigten sie, dass sie erst dann in ihre richtige dreidimensionale Form schnellt, wenn sie an λ5 bindet. Eine kurze Region von λ5, geformt wie ein Beta-Strang, schiebt sich in VpreB und vervollständigt dessen Struktur, ähnlich wie ein fehlender Zahn in ein Zahnrad eingesetzt wird. Diese "assoziationsinduzierte Faltung" stabilisiert nicht nur VpreB, sondern schafft auch eine sehr enge Partnerschaft zwischen den beiden Proteinen mit einer Affinität im niedrigen Nanomolarbereich. In Zellen entkommen VpreB und λ5 nur dann der Zurückhaltung im endoplasmatischen Retikulum und werden sezerniert oder weitertransportiert, wenn sie sich zu dieser Surrogat-Leichtkette zusammensetzen — ein Hinweis darauf, wie eng Faltung und Qualitätskontrolle gekoppelt sind.
Die schwere Kette fertigstellen und die Inspektion bestehen
Die Geschichte endet nicht bei VpreB und λ5. Eine entscheidende Region der schweren Kette, CH1 genannt, ist anfänglich ungeordnet und verbleibt in der Zelle. Die Forscher zeigten, dass λ5, das etwas wie ein Chaperon wirkt, CH1 zur Faltung anregen kann, wenn sie binden. Dieser zweite Schritt der assoziationsinduzierten Faltung ist essentiell für den Aufbau des vollständigen Vor-B-Zell-Rezeptors und dafür, dass dieser das endoplasmatische Retikulum verlassen und an die Zelloberfläche gelangen kann. Interessanterweise können beide Teile der Surrogat-Leichtkette — VpreB und λ5 — die schwere Kette berühren, doch nur λ5 vermag CH1 in seinen fertigen, faltfähigen Zustand zu überführen. Wenn dies nicht geschieht, wird der partielle Rezeptor zurückgehalten und die Zelle lehnt die betreffende schwere Kette effektiv ab.
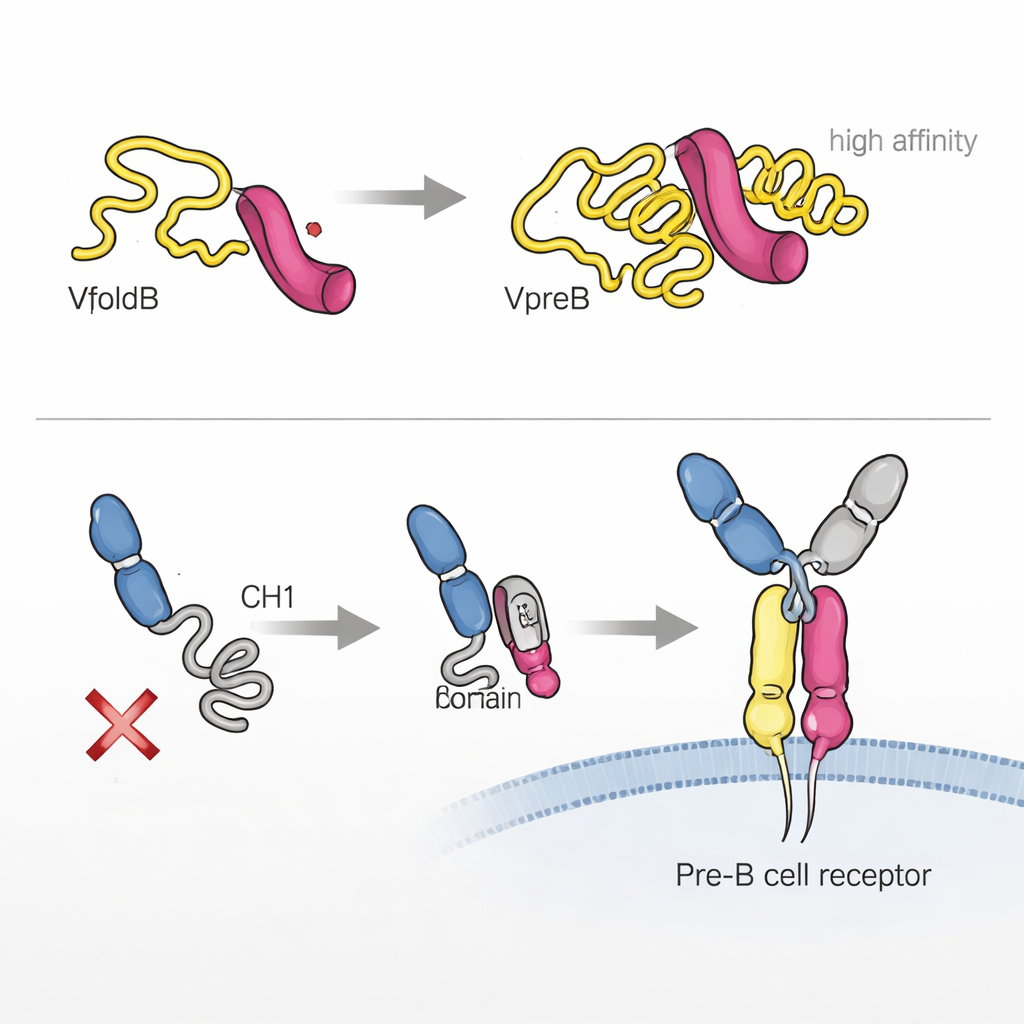
Flexible Schwänze, die Bindung und Signalgebung feinabstimmen
Sowohl VpreB als auch λ5 tragen schlaffe, ungeordnete Abschnitte, bekannt als einzigartige Regionen, die keine erkennbaren Ähnlichkeiten zu bekannten Proteinsequenzen aufweisen. Obwohl diese Schwänze für die Assemblierung der beiden Proteine im Reagenzglas nicht unbedingt erforderlich sind, fanden die Autoren heraus, dass sie stark beeinflussen, wie schnell die Surrogat-Leichtkette entsteht, wie stabil sie ist und wie gut sie an Abschnitte der schweren Kette bindet. In Zellen verringerte das Entfernen dieser Regionen die Effizienz, mit der die zusammengesetzten Komplexe sezerniert wurden. Besonders der λ5-Schwanz erwies sich als Multitalent: Er beschleunigt die Assemblierung, ist für bestimmte Kontakte mit der variablen Region der schweren Kette unerlässlich und trägt maßgeblich dazu bei, wie der Vor-B-Zell-Rezeptor Antigene und andere Liganden bindet. In einigen Fällen näherte sich die Antigenbindungsstärke einer Surrogat-Leichtkette–schwere Kette-Kombination der eines normalen Antikörperfragments an.
Warum das für die Antikörpervielfalt wichtig ist
Indem sie diese schrittweisen Faltungs- und Assemblierungsereignisse kartieren, schlagen die Autoren vor, dass die Surrogat-Leichtkette mehr tut, als die schwere Kette einfach an Ort und Stelle zu halten. Sie fungiert als dynamischer Inspektor, der mit ihrem strukturierten Kern und den flexiblen Schwänzen prüft, ob eine schwere Kette korrekt falten und produktiv mit potenziellen Zielen interagieren kann. Erfolgreiche Kombinationen werden gefaltet, stabilisiert und dürfen die Zelloberfläche erreichen, wo sie Signale senden, die der B-Zelle erlauben, weiter zu reifen. Fehlerhafte Kombinationen werden festgehalten und schließlich eliminiert. Für Laien lautet die Botschaft: Ihr Immunsystem betreibt einen ausgeklügelten "Prüfstand" für zukünftige Antikörper, aufgebaut aus Proteinen, die einander buchstäblich in Form falten und so sicherstellen, dass nur wohlverhaltene Antikörperkerne weiterlaufen, um Sie zu verteidigen.
Zitation: König, J., Sarmiento Alam, N.C., He, R. et al. Association-induced folding governs surrogate light chain and pre-B cell receptor core assembly. Nat Commun 17, 1202 (2026). https://doi.org/10.1038/s41467-026-68965-5
Schlüsselwörter: B-Zell-Entwicklung, Antikörperfaltung, Surrogat-Leichtkette, Protein-Qualitätskontrolle, Vor-B-Zell-Rezeptor