Clear Sky Science · de
Entschlüsselung enzymatischer Deracemisierung strukturell vielfältiger Allene durch designte Photoenzyme
Warum das Kombinieren von Molekülen zählt
Viele Arzneimittel wirken nur, wenn ihre Atome in einer sehr bestimmten dreidimensionalen Anordnung vorliegen, ähnlich wie eine linke Hand in einen linken Handschuh passt, nicht aber in einen rechten. Chemiker können solche „einhändigen“ Moleküle oft herstellen, doch wird es schwierig, wenn die Bausteine komplex sind. Diese Arbeit geht diese Herausforderung für eine knifflige Klasse verdrehter Strukturen — die Allene — an, indem maßgeschneiderte, lichtgetriebene Enzyme eingesetzt werden. Die Studie zeigt, wie Biologie und Photochemie kombiniert werden können, um aus einem verwirrten Gemisch gezielt die gewünschte molekulare „Hand“ herauszufiltern, was schnellere und sauberere Wege zu künftigen Wirkstoffen und Materialien verspricht.
Verdrehte Bausteine mit großem Nutzen
Allene sind lineare Ketten aus drei Kohlenstoffatomen mit zwei benachbarten Doppelbindungen; diese einfache Anordnung verdreht jedoch den Raum so, dass das gesamte Molekül eine Händigkeit erhält. Diese axiale Verdrehung tritt in Naturstoffen, Pflanzenschutzmitteln und fortgeschrittenen Katalysatoren auf. Leider sind traditionelle Methoden zur Herstellung chiraler Allene meist stark spezialisiert: Ein Katalysator, der für ein Allenen ausgezeichnet funktioniert, versagt oft bei einem anderen mit nur kleinen strukturellen Änderungen. Selbst neu entwickelte, lichtgetriebene chemische Katalysatoren haben mit diesem Problem zu kämpfen. Daher müssen Chemiker beim Erschließen neuer Allene häufig Katalysatoren von Grund auf neu entwerfen, was die Forschung verlangsamt und Abfall erhöht.
Natürliche Selektivität nutzen und Licht hinzufügen
Enzyme in lebenden Systemen sind hervorragend darin, bestimmte Formen mit bemerkenswerter Präzision zu erkennen und umzusetzen, doch sie haben sich für natürliche Zielmoleküle entwickelt, nicht für menschengemachte Allene. Die Autoren machten sich daran, ein „Photoenzym“ zu schaffen, das enzymähnliche Selektivität mit der Fähigkeit verbindet, Licht als Energiequelle zu nutzen. Sie begannen mit einem Proteingerüst namens CTB10 und veränderten es genetisch so, dass es eine nicht‑natürliche Aminosäure trägt, die wie eine winzige eingebaute Lichtantenne wirkt. Wenn dieser besondere Baustein ultraviolettes Licht absorbiert, kann er Energie an ein benachbartes Allenen weitergeben, es kurzzeitig anregen und so seine Verdrehung verwirren. Durch wiederholtes Anwenden dieses Prozesses kann das Enzym selektiv eine Hand aus einem 50:50‑Gemisch entfernen und überwiegend die andere zurücklassen. 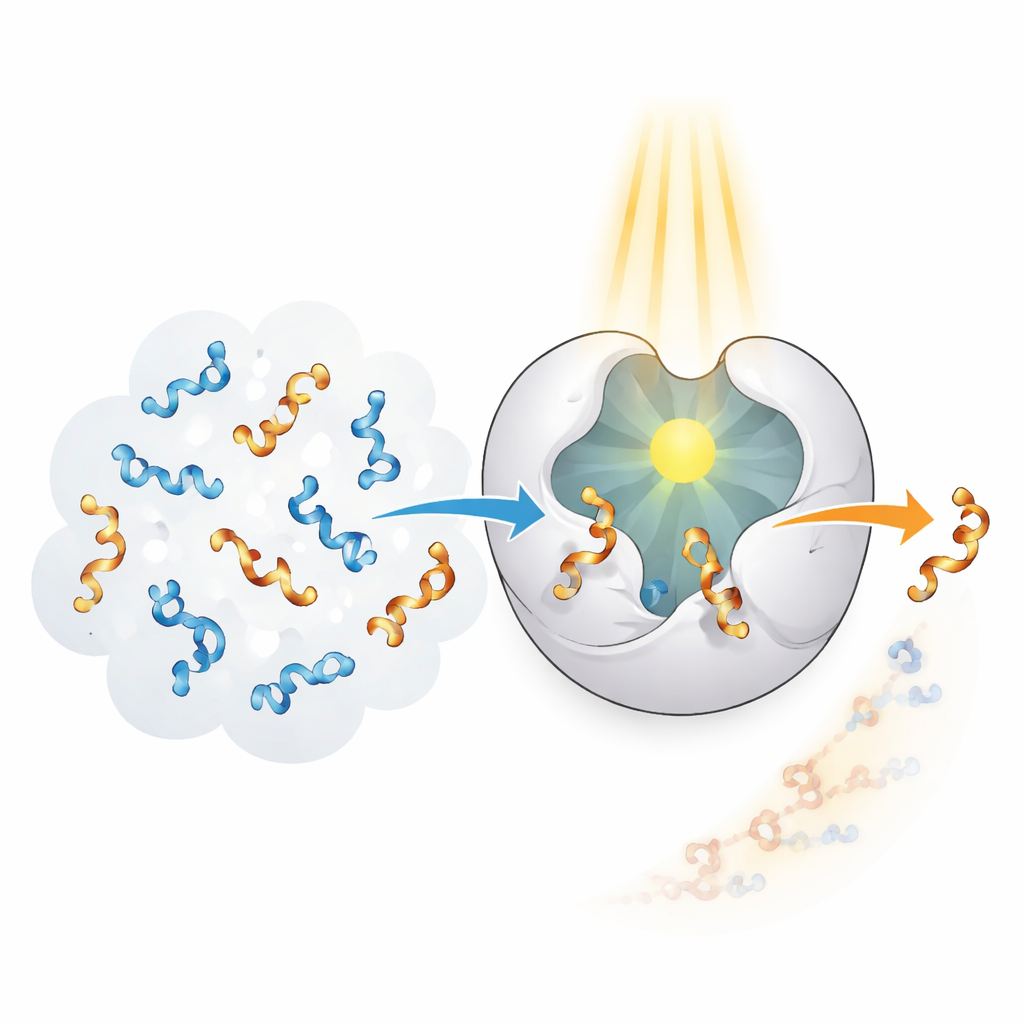
Passgenaue Taschen für viele verschiedene Gäste schnitzen
Ein solches System zu entwerfen ist nicht so einfach wie Licht auf ein Protein zu richten. Das Team nutzte Computermodellierung, gezielte Mutationen und Röntgenaufnahmen, um mehrere Varianten des Photoenzyms zu formen, jede mit einer leicht unterschiedlichen inneren Tasche. Diese Taschen halten das Allenen in einer definierten Pose neben der Lichtantenne und stabilisieren wichtige Bereiche des Moleküls durch Wasserstoffbrücken und subtile Packungswechselwirkungen. Schritt für Schritt verbesserten die Forscher sowohl die Bindungsstärke als auch die Ausrichtung zwischen Enzym und Allenen, die für eine effiziente Energieübertragung entscheidend sind. Die finalen Varianten zeigten beeindruckende Leistungen und wandelten Allenen‑Carbonsäuren, Ester und Amide in einhändig vorliegende Produkte mit sehr hoher Reinheit um, oft über 99% einer Händigkeit, und das unter Luft ohne empfindliche Bedingungen.
Den Mechanismus in atomarer Auflösung beobachten
Um zu verstehen, warum die neuen Photoenzyme eine Händigkeit bevorzugen, kristallisierten die Autoren Enzym‑Substrat‑Paare und untersuchten sie in atomarer Auflösung. Sie fanden, dass die bevorzugte Allenen‑Hand näher an der lichtsammelnden Gruppe liegt und mehrere leicht unterschiedliche Konformationen einnehmen kann, die alle mit effizienter Energieübertragung kompatibel sind. Die weniger bevorzugte Hand bindet entweder schwach oder sitzt weiter entfernt, wodurch sie viel unwahrscheinlicher angeregt wird. Zusätzliche Experimente mit rein rechten und linken Ausgangsstoffen bestätigten diese Präferenz: Das Enzym wandelt die bevorzugte Hand schnell in ein reaktives Zwischenprodukt um, das sich dann in Lösung wieder in ein Gemisch entspannt, in dem sich die entgegengesetzte Hand anreichert. Im Kern verhält sich das Protein wie ein molekularer Drehkreuz, das wiederholt eine Hand anregt und verbraucht, während die andere sich ansammelt. 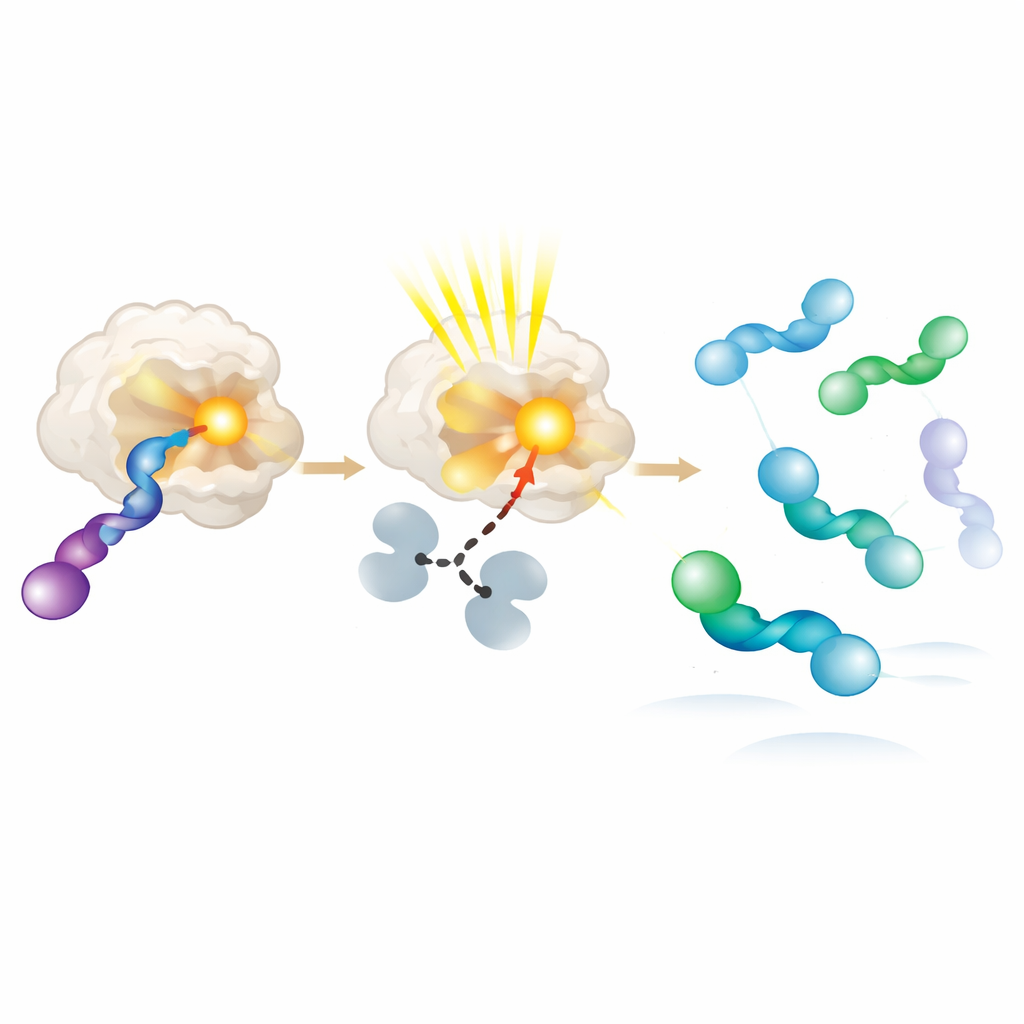
Was das für die Chemie von morgen bedeutet
Für Nichtfachleute ist die Hauptaussage, dass das Team eine programmierbare Proteineinrichtung geschaffen hat, die Licht nutzt, um verdrehte Moleküle mit unerreichter Vielseitigkeit zu sortieren und aufzuwerten. Anstatt für jedes Zielmolekül einen völlig neuen chemischen Katalysator zu entwerfen, können Forschende nun von dieser Photoenzym‑Plattform ausgehen und die innere Tasche so anpassen, dass sie viele verschiedene Allene akzeptiert. Dieser Ansatz verkleinert die Lücke zwischen der feinen Kontrolle der Natur und dem Bedarf der chemischen Industrie an breiten, robusten Methoden. Langfristig könnten solche lichtbetriebenen Enzyme Chemikern helfen, komplexe, einhändig vorliegende Bausteine für Arzneimittel und Materialien effizienter, mit weniger Schritten und geringerem Abfall herzustellen.
Zitation: Fu, K., Li, M., Deng, Z. et al. Unlocking enzymatic deracemization of structurally diverse allenes by designed photoenzymes. Nat Commun 17, 2082 (2026). https://doi.org/10.1038/s41467-026-68964-6
Schlüsselwörter: Photoenzym, Deracemisierung, chirales Allenen, Biokatalyse, Triplet-Energieübertragung