Clear Sky Science · de
HCMV-Infektion stört Barrierefunktionen und fördert epithelial–mesenchymale Transition in einem Cholangiocyten-Organoidmodell
Warum diese Virus-im-Leber-Geschichte wichtig ist
Das humane Zytomegalovirus ist ein sehr verbreitetes Virus, das viele von uns unbemerkt in sich tragen. Bei Neugeborenen und Menschen mit geschwächtem Immunsystem kann es jedoch mit schweren Leber- und Gallengangsproblemen in Verbindung gebracht werden, einschließlich einer seltenen, aber verheerenden Kinderkrankheit namens Gallengangsatresie. Diese Studie verwendet miniaturisierte, im Labor gezüchtete menschliche Gallengänge, um zu zeigen, wie das Virus diese sensiblen Röhrchen direkt schädigen und narbige Veränderungen auslösen kann, die die seit langem diskutierten Zusammenhänge zwischen Infektion und lebenslanger Lebererkrankung erklären könnten.
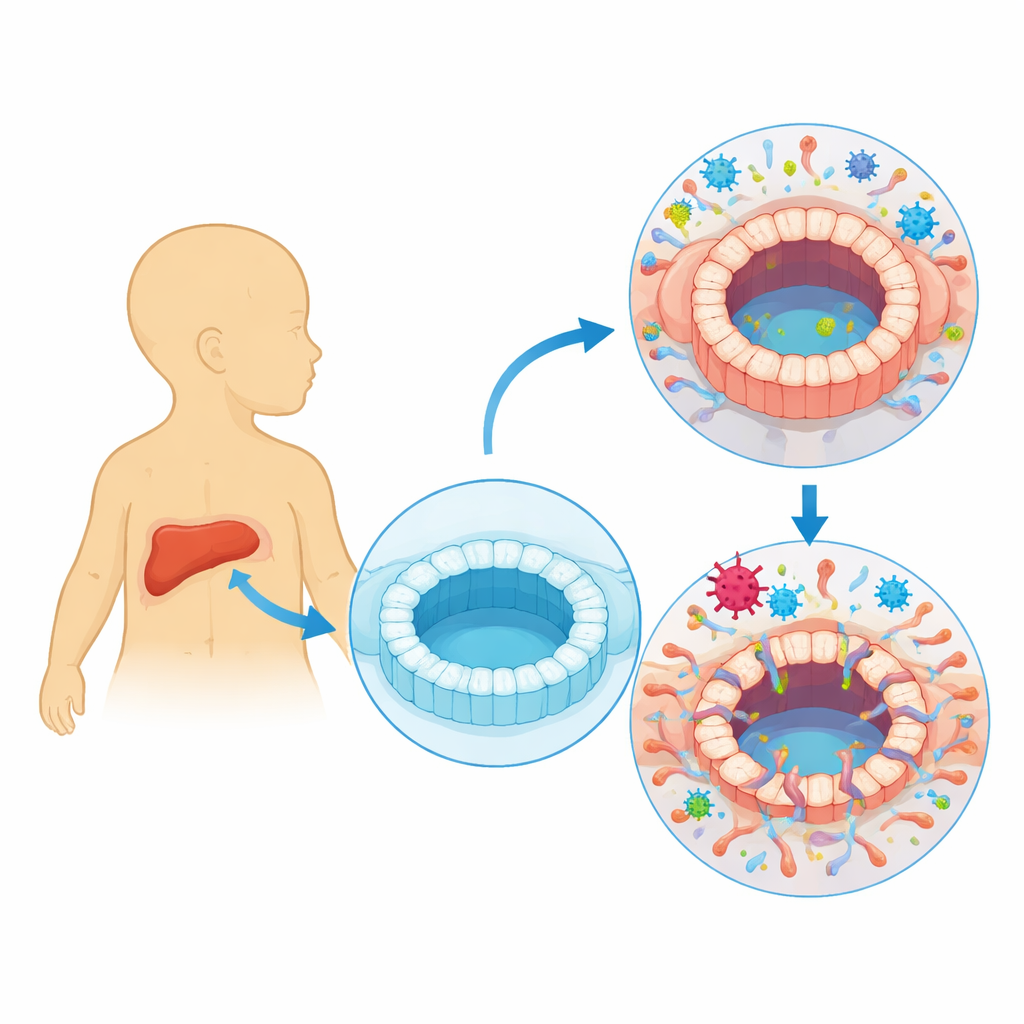
Ein genauerer Blick auf ein häufiges, aber ruhiges Virus
Das humane Zytomegalovirus (HCMV) verbleibt meist inaktiv in unserem Körper und wechselt zwischen einer aktiven Phase, in der es neue Viruspartikel produziert, und einer stillen Phase, in der es in bestimmten Blutzellen verborgen liegt. Kliniker beobachten seit Langem, dass Menschen mit eindeutiger HCMV-Infektion Gallengangsverletzungen und Cholestase entwickeln können, bei der der Gallenfluss gestört ist. Viele Säuglinge mit Gallengangsatresie — einem Zustand, bei dem Gallengänge kurz nach der Geburt blockiert und vernarbt sind — zeigen ebenfalls Hinweise auf eine kürzlich durchgemachte HCMV-Infektion. Allerdings war lange unklar, ob das Virus tatsächlich die Zellen auskleidend der Gallengänge infiziert oder nur als Begleiterscheinung bei der Erkrankung nachweisbar ist.
Winzige Gallengänge in der Schale nachbauen
Um das zu klären, erzeugten die Forschenden dreidimensionale „Organoide“, die menschliche Gallengänge nachahmen. Sie begannen mit induzierten pluripotenten Stammzellen, die aus menschlichem Blut reprogrammiert wurden, und leiteten diese zu cholangiocytenähnlichen Zellen — dem Zelltyp, der Gallengänge auskleidet. Diese Zellen organisierten sich selbst zu hohlen Kugeln mit einem zentralen Hohlraum und engen Zell–Zell-Verbindungen, die einem miniaturisierten Gallengang ähneln. Das Team exponierte diese Organoide dann einem HCMV-Stamm, der mit einem fluoreszierenden Marker versehen war, der aufleuchtet, wenn das Virus aktiv repliziert. So konnten sie infizierte Zellen verfolgen und messen, wie sich die Organoide im Verlauf veränderten.
Wie die Infektion Struktur verzerrt und die Barriere schwächt
Nach der Infektion hörten die Organoide auf, normal zu wachsen, und wurden verformt, mit verdickten und unregelmäßigen Wänden. Einige Zellen leuchteten stark und zeigten vollständige virale Aktivität und Produktion neuer Partikel; andere enthielten virales genetisches Material in geringerer Menge, was auf einen eher ruhenden, latenzähnlichen Zustand hindeutet. Funktionelle Tests zeigten, dass infizierte Organoide wichtige Gallengangsfunktionen verloren. Sie schwellten nicht mehr richtig als Reaktion auf einen Reiz, der von Ionentransportkanälen abhängt, und sie zeigten erhöhte Leckagen in einem elektrischen Widerstandsassay, der die Dichtigkeit der Barriere misst. Proteine, die normalerweise die Räume zwischen Zellen abdichten, wie Komponenten der Tight Junctions, waren reduziert, und der Transport eines Testfarbstoffs in den Hohlraum hinein und wieder hinaus war gestört. Zusammengenommen zeigen diese Veränderungen, dass HCMV die Gallengangswand direkt schwächen und undicht sowie funktionsgestört machen kann.
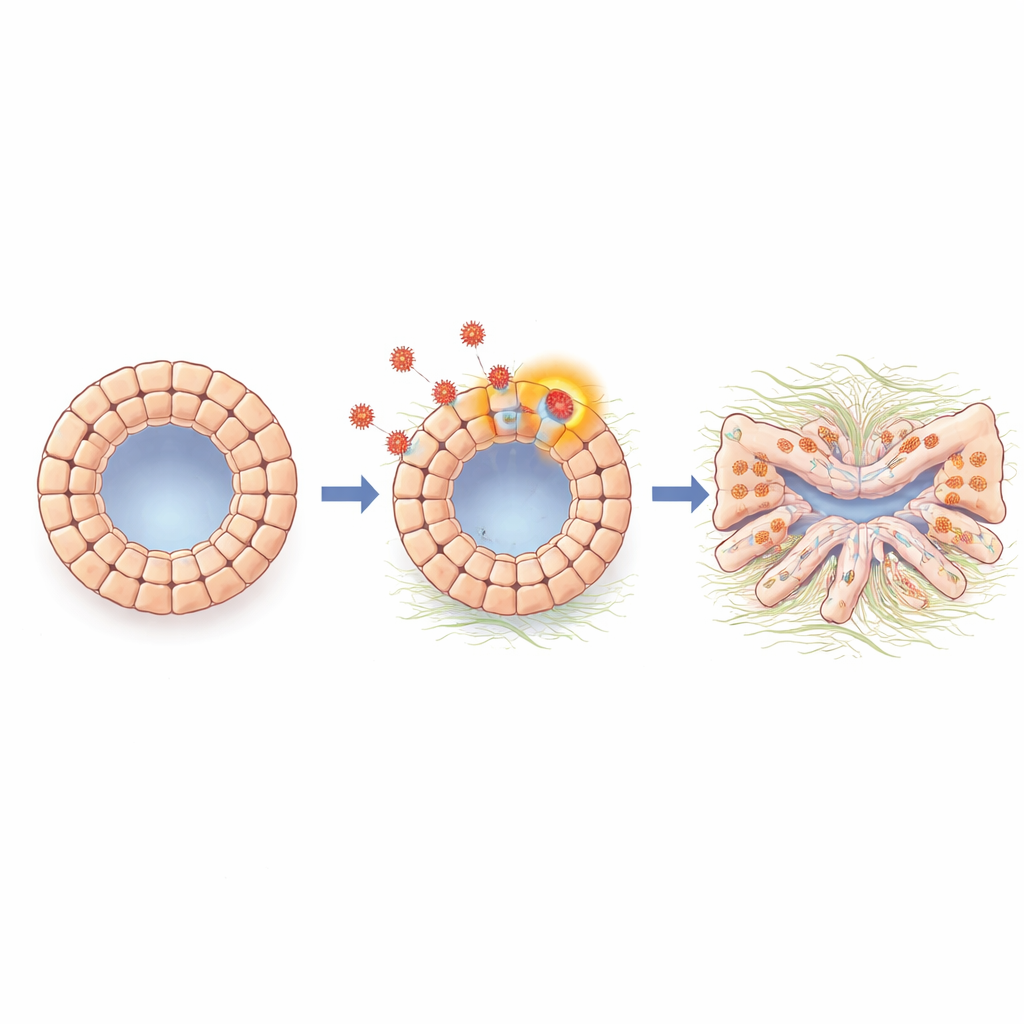
Zellen verändern ihre Identität in Richtung Narbenbildung
Vertiefte Analysen der Genaktivität in den Organoiden — sowohl in Bulk als auch auf Einzelzellebene — zeigten eine starke Aktivierung eines epithelial–mesenchymalen-Transition-ähnlichen Programms. Dabei lösen sich eng verbundenen Oberflächenzellen, nehmen ein mobileres, faseriges Verhalten an und beginnen, Moleküle zu produzieren, die mit Gewebenarbung assoziiert sind. In infizierten Organoiden wurden erhöhte Mengen an N-Cadherin und anderen Markern beobachtet, die mit dieser Umstellung verbunden sind, ebenso wie Gene, die an Fibrose und Matrixproduktion beteiligt sind. Ein Signalmolekül namens TGF-beta, das bekannt dafür ist, in vielen Organen Narbenbildung voranzutreiben, war während der Infektion verstärkt. Wenn das Team die TGF-beta-Signalgebung mit einem kleinen Molekül-Inhibitor oder einem Antikörper blockierte, nahmen die Organoide eine normalere Form an, und viele der narben- und transitionsbezogenen Gene fielen wieder in Richtung Ausgangswert, was darauf hindeutet, dass TGF-beta ein wichtiger Vermittler ist, der virale Präsenz mit schädlichen Zellveränderungen verbindet.
Von im Labor gezüchteten Röhrchen zurück zu kranken Kindern
Um zu prüfen, ob diese Beobachtungen im Labor mit realen Erkrankungen zusammenhängen, untersuchten die Forschenden Lebergewebe von Kindern mit Gallengangsatresie und von anderen pädiatrischen Lebererkrankungen. Mit sensiblen Sonden detektierten sie HCMV-DNA in Cholangiocyten — den Gallengangszellen — in etwa zwei Dritteln der Gallengangsatresie-Proben, deutlich seltener jedoch in Lebern ohne Gallengangsatresie. In denselben Bereichen, in denen virale DNA gefunden wurde, zeigten die Gallengangszellen erhöhte Werte von TGF-beta und N-Cadherin, was dem in den Organoiden beobachteten Muster von Transition und Narbenbildung entspricht. Das deutet darauf hin, dass in zumindest einem Teil der betroffenen Kinder HCMV die Gallengangszellen direkt infiziert und sie durch Aktivierung TGF-beta-vermittelter Wege in einen fibrotischen Zustand treibt.
Was das für das Verständnis und die Behandlung von Gallengangserkrankungen bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass ein häufiges Virus die Zellen, die Gallengänge auskleiden, infizieren, ihre engen Verbindungen lösen und sie über ein TGF-beta-abhängiges Signal in eine narbenbildende, weniger spezialisierte Identität drängen kann. Diese Veränderungen schwächen die Barriere- und Transportfunktionen der Gänge und könnten zu den blockierten, fibrotischen Gallengängen beitragen, wie sie bei Erkrankungen wie der Gallengangsatresie beobachtet werden. Zwar wird nicht jeder Fall von Gallengangserkrankung durch HCMV verursacht, doch stärkt die Studie die Annahme, dass bei anfälligen Säuglingen eine virale Infektion ein wichtiger Faktor sein könnte — und dass die gezielte Blockade TGF-beta-assoziierter Wege eines Tages helfen könnte, fragile Gallengänge zu schützen oder wiederherzustellen.
Zitation: Ye, Z., Hu, X., Rahaman, S.M. et al. HCMV infection disrupts barrier functions and promotes epithelial–mesenchymal transition in a cholangiocyte organoid model. Nat Commun 17, 2273 (2026). https://doi.org/10.1038/s41467-026-68962-8
Schlüsselwörter: Zytomegalovirus, Gallengangsatresie, Gallengang-Organoide, epithelial-mesenchymale Transition, TGF-beta-Signalgebung