Clear Sky Science · de
Divergente photochemische Ring‑Austauschreaktion von Isoxazolen
Licht ins Dunkel der Arzneibauklötze
Viele moderne Arzneimittel bestehen aus kleinen, ringförmigen Fragmenten, die das Verhalten eines Wirkstoffs im Körper maßgeblich bestimmen. Chemiker möchten solche Ringe oft gegen nahe verwandte Varianten austauschen, um die Aktivität zu optimieren, doch heute bedeutet das meist, das gesamte Molekül von Grund auf neu zu synthetisieren. Diese Studie zeigt, dass gezielt eingesetztes ultraviolettes Licht einen verbreiteten Ring, das Isoxazol, direkt in mehrere andere nützliche Ringe umwandeln kann und damit Zeit, Kosten und Aufwand bei der Wirkstoffsuche sparen könnte.
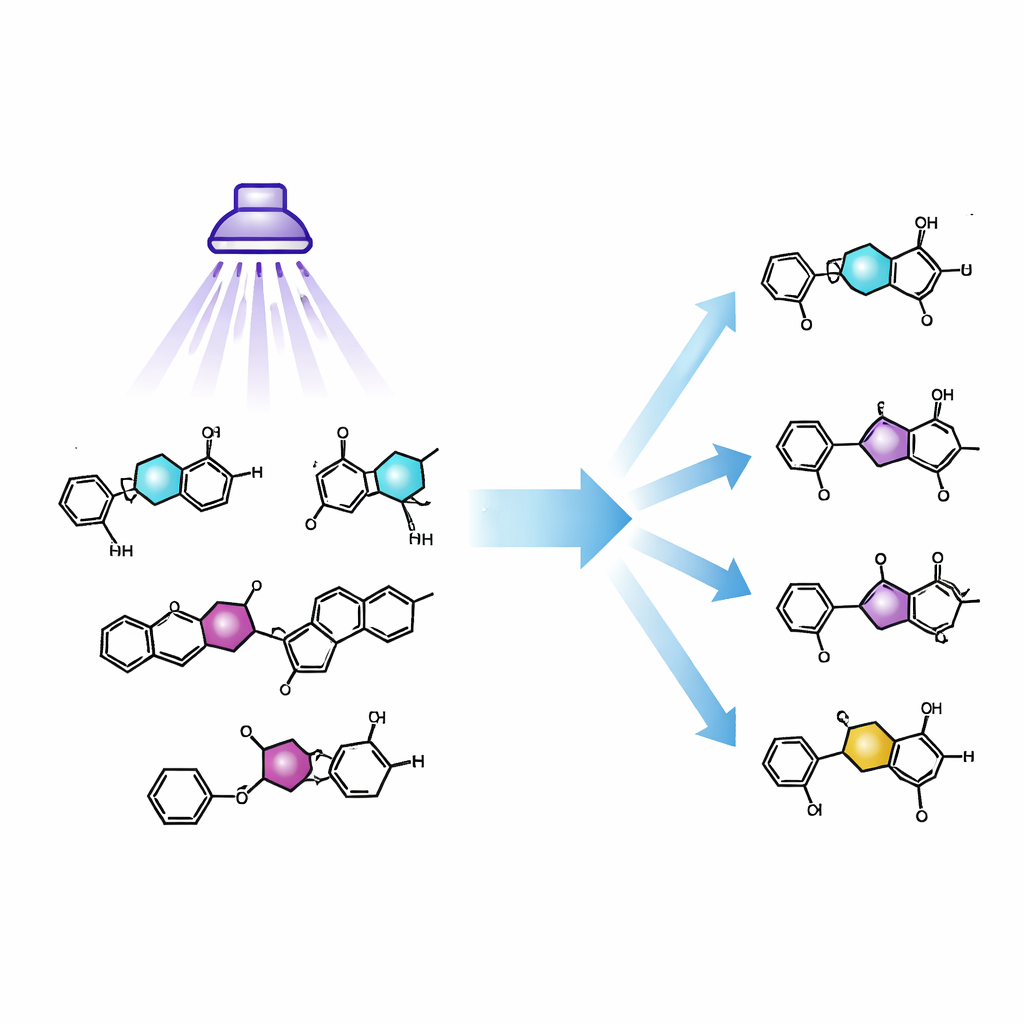
Warum diese kleinen Ringe wichtig sind
Fünfringige Systeme mit Sauerstoff-, Stickstoff‑ oder Schwefelatomen finden sich in Arzneimitteln und Pflanzenschutzmitteln überall. Isoxazole und Oxazole können typische funktionelle Gruppen wie Ketone oder Ester ersetzen und verbessern dabei oft Stabilität und Wirksamkeit eines Wirkstoffs. Wenn Forscher untersuchen, wie sich ein Ringwechsel auf biologische Aktivität auswirkt, bereiten sie in der Regel für jeden Ringtyp eine eigene Molekülvariante zu — ein aufwändiger Prozess, der als de‑novo‑Synthese bekannt ist. Eine Methode, die von einem einzigen isoxazolbasierten Lead ausgeht und dessen Ring direkt in mehrere nahe Verwandte umwandelt, würde diese Erkundung des chemischen Raums erheblich beschleunigen.
Licht als präzises Werkzeug
Die Autoren fanden heraus, dass ultraviolettes Licht an Isoxazolringen hochselektive Umordnungen auslösen kann, sofern die «Dekorationen» des Moleküls und das umgebende Lösungsmittel sorgfältig gewählt sind. Ausgehend von einem einfachen Isoxazol identifizierten sie Bedingungen, unter denen Licht es entweder in einen Oxazolring umwandelt oder alternativ den Ring öffnet und ein Zwischenprodukt, ein alpha‑Ketonitril, bildet. Frühere Arbeiten hatten auf ähnliches Verhalten hingedeutet, litten jedoch unter geringen Ausbeuten und unübersichtlichen Produktgemischen. Hier variierten die Forschenden systematisch die Substituenten am Ring und das Lösungsmittel und kartierten, wann eine saubere Ring‑Umtauschreaktion stattfindet und wann das Molekül stattdessen zerfällt oder unverändert bleibt.
Blick ins Innenleben mit theoretischen Methoden
Um zu verstehen, warum kleine strukturelle Änderungen zu so unterschiedlichen Ergebnissen führen, griffen die Forschenden auf quantenchemische Rechnungen zurück. Diese Computerstudien zeigen, dass das Isoxazol nach Lichtabsorption kurz einen angeregten Zustand durchläuft, in dem eine Schlüsselbindung aufbricht und ein hochenergetisches Zwischenprodukt entsteht. Von dort aus kann das System entweder wieder zum ursprünglichen Ring zurückschließen, in einen dreigliedrigen Azirin kontrahieren oder sich weiter umordnen. Ob der Prozess sauber zu einem neuen Ring führt oder in Zersetzung endet, hängt empfindlich davon ab, wo Substituenten am Ausgangsring sitzen und wie gut die einzelnen Zwischenstufen zusätzliches Licht absorbieren. Die Analyse ergab, dass Isoxazole mit bestimmten Gruppen an einer spezifischen Ringposition besonders gut für kontrollierten Ringtausch geeignet sind.
Von einem Ring zu vielen
Mit diesen Erkenntnissen konzentrierte sich das Team auf eine Familie von Isoxazolen, die zuverlässig auf Licht reagieren. In alkoholischen Lösungsmitteln verwandeln sich diese Substrate unter milden Bedingungen glatt in Oxazole und vertragen eine breite Palette zusätzlicher funktioneller Gruppen, einschließlich empfindlicher Gruppen, wie sie häufig in Wirkstoffkandidaten vorkommen. In einem weniger polaren Lösungsmittel liefert dasselbe Licht stattdessen das alpha‑Ketonitril‑Zwischenprodukt, das in einem einen Topf‑Verfahren in mehrere andere Ringe überführt werden kann — Pyrazole, Pyrrole, amino‑substituierte Isoxazole und Isothiazole — mittels einfacher Nachreaktionen. Ausgehend von nur sieben kommerziell erhältlichen Isoxazolen stellten die Autorinnen und Autoren eine Bibliothek von 34 verschiedenen heterocyclischen Produkten zusammen, ohne ein Molekül von Grund auf neu zu bauen.
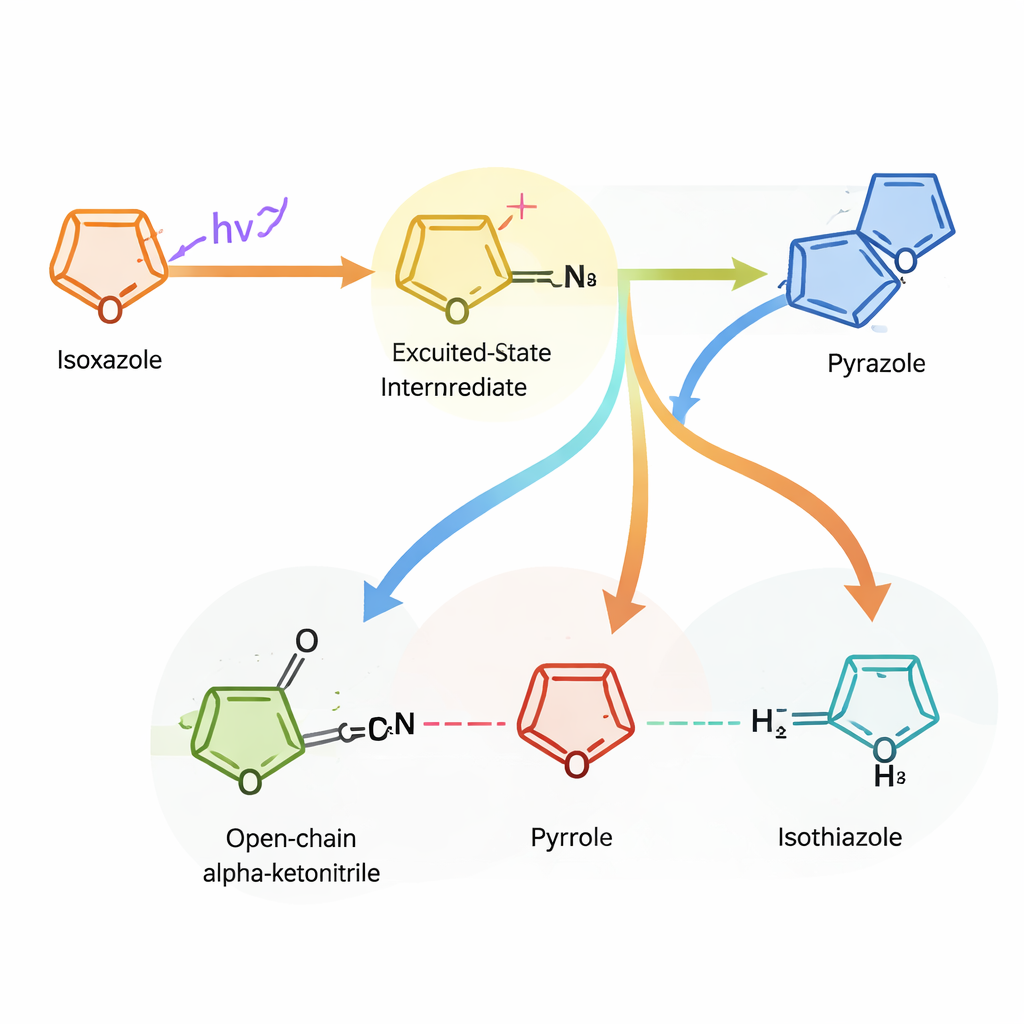
Auswirkungen auf künftige Arzneimittel
Diese Arbeit führt eine praktikable Methode ein, den zentralen Ring komplexer Moleküle spät in der Synthese zu «editieren», statt sie aus einfacheren Bausteinen neu aufzubauen. Durch den Einsatz von Licht zur selektiven Ring‑Umwandlung können Chemiker rasch Familien eng verwandter Strukturen erzeugen und deren Verhalten in biologischen Systemen testen. Die milden Bedingungen und die Verträglichkeit mit realen Wirkstoffmolekülen deuten darauf hin, dass diese Methode ein wertvolles Werkzeug für die medizinische Chemie werden könnte, um bessere Therapien mit weniger Syntheseschritten zu finden.
Zitation: Xu, Y., Poletti, L., Arpa, E.M. et al. Divergent photochemical ring-replacement of isoxazoles. Nat Commun 17, 2141 (2026). https://doi.org/10.1038/s41467-026-68960-w
Schlüsselwörter: photochemische Ring‑Bearbeitung, Isoxazol‑Umwandlung, Heterozyklus‑Diversifizierung, Methoden der medizinischen Chemie, Scaffold‑Hopping