Clear Sky Science · de
KI-basierte Multiomik-Profile zeigen komplementäre Omik-Beiträge zur personalisierten Vorhersage von Herz-Kreislauf-Erkrankungen
Warum es wichtig ist, Herzprobleme früher vorherzusagen
Herzkrankheiten und Schlaganfälle bleiben die weltweit führenden Todesursachen und treten oft bei scheinbar gesunden Menschen ohne Vorwarnung auf. Ärztinnen und Ärzte verwenden bereits Checklisten mit Alter, Blutdruck, Cholesterin und Raucherstatus, um das Risiko einzuschätzen, doch diese Instrumente können viele zukünftige Patientinnen und Patienten übersehen und bei anderen das Risiko überschätzen. Diese Studie stellt eine aktuelle Frage: Wenn wir tiefer in die im Blut zirkulierenden Moleküle schauen und sie mit künstlicher Intelligenz analysieren, können wir Herz-Kreislauf-Erkrankungen dann Jahre vor ihrem Auftreten erkennen — und die Prävention individuell anpassen?
Im Blut nach verborgenen Warnsignalen suchen
Die Forschenden nutzten die UK Biobank, ein umfangreiches Gesundheitsprojekt, das Hunderttausende Freiwillige über viele Jahre verfolgt. Für eine Untergruppe dieser Teilnehmerinnen und Teilnehmer hatten Wissenschaftlerinnen und Wissenschaftler tausende Moleküle in Blutproben sorgfältig gemessen: kleine Metaboliten im Zusammenhang mit Fetten, Zuckern und Aminosäuren sowie Proteine, die an Entzündungen, Blutgerinnung und anderen Körperprozessen beteiligt sind. Das Team konzentrierte sich auf sechs wichtige kardiovaskuläre Erkrankungen — koronarer Herzkrankheit, Schlaganfall, Herzinsuffizienz, Vorhofflimmern, periphere arterielle Verschlusskrankheit und venöse Blutgerinnsel — um zu prüfen, ob diese molekularen Fingerabdrücke vorhersagen können, wer welche Erkrankung entwickeln wird.
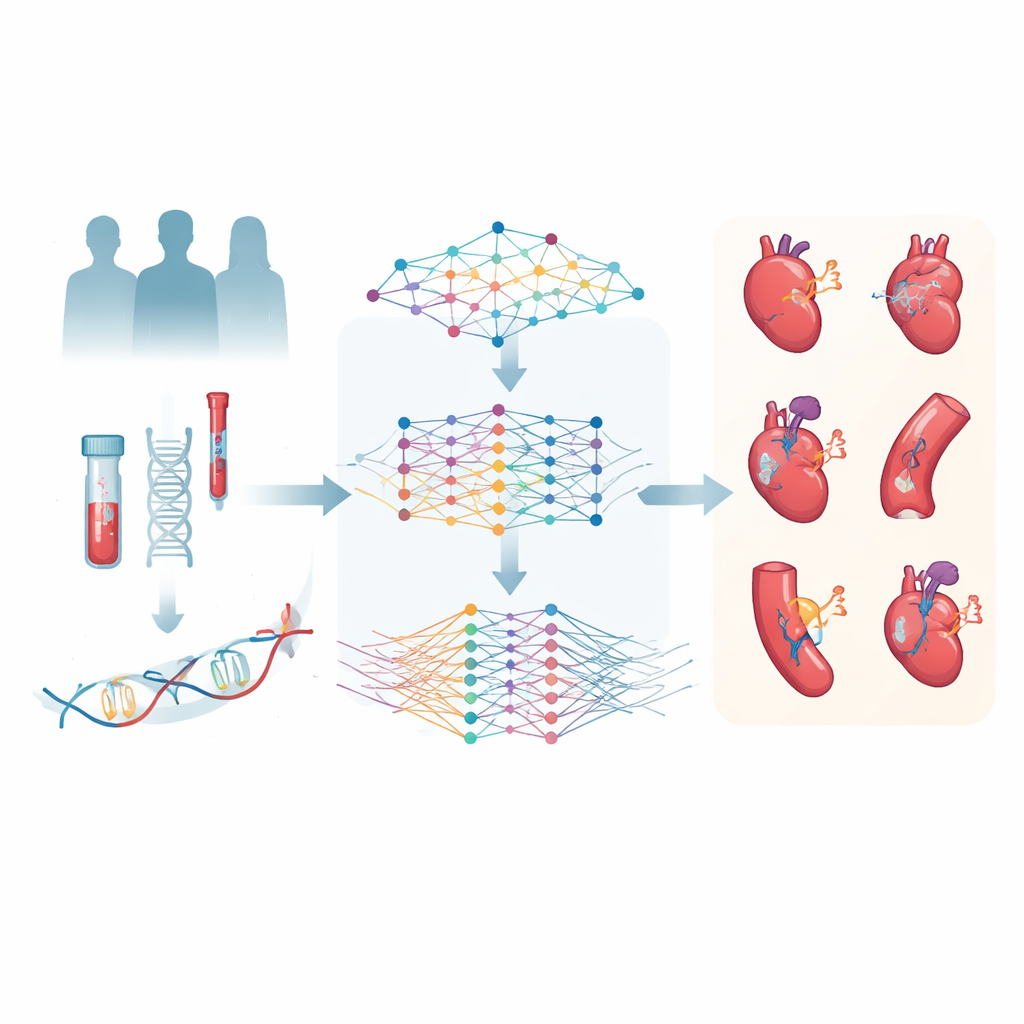
Künstliche Intelligenz das Lesen molekularer Muster beibringen
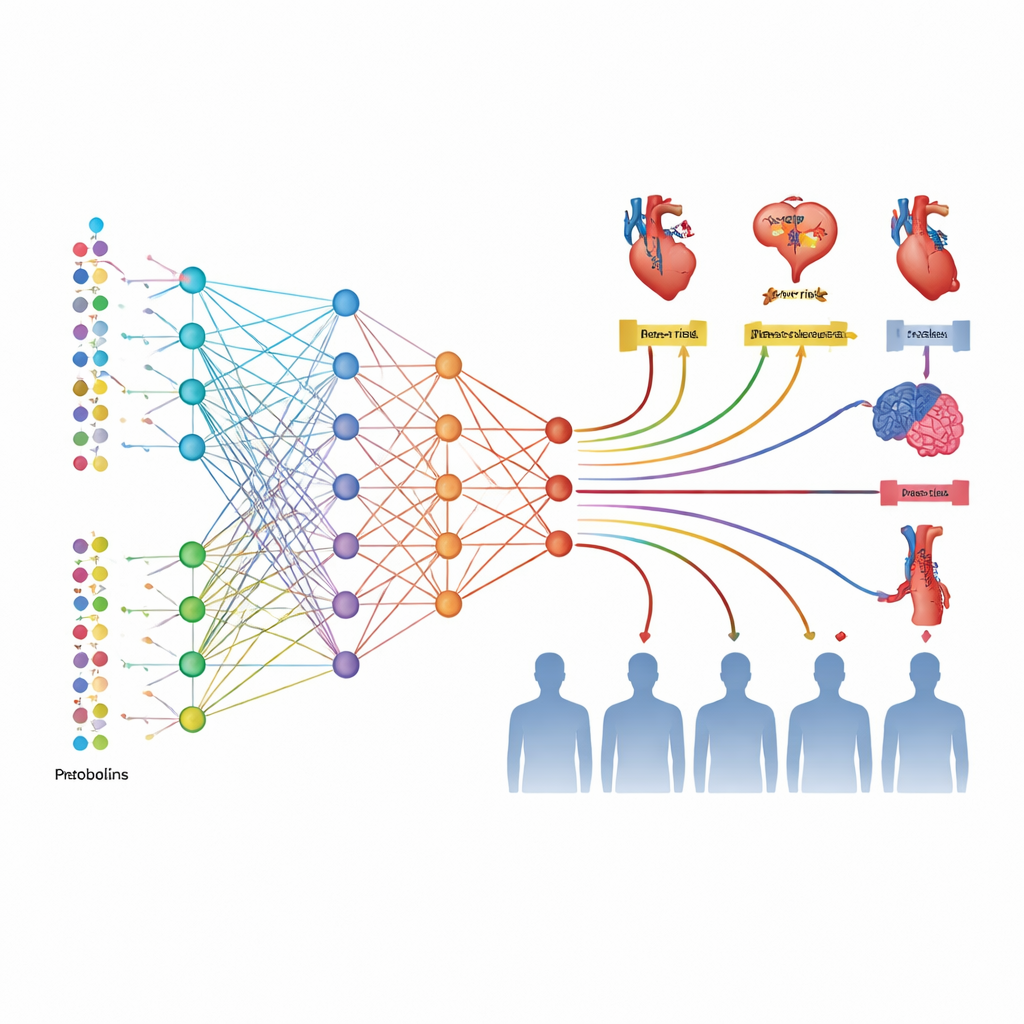
Um aus fast 3.000 Proteinen und 168 Metaboliten Sinn zu machen, entwickelten die Autorinnen und Autoren zwei Deep-Learning-Modelle, MetNet und ProNet. Statt jeweils nur eine Erkrankung vorherzusagen, lernten diese Modelle Muster, die mit allen sechs kardiovaskulären Ergebnissen zugleich zusammenhängen. Aus den Metabolitendaten erzeugte MetNet einen kombinierten Risikoscore namens MetScore; aus den Proteindaten lieferte ProNet den ProScore. Jede Person erhielt somit pro System sechs Scores — je einen für jeden Erkrankungstyp — die Millionen möglicher molekularer Wechselwirkungen in eine überschaubare Anzahl von Zahlen zusammenfassen, welche ein standardmäßiges statistisches Modell zusammen mit Alter, Blutdruck, Medikamenten und genetischem Risiko verwenden kann.
Wie viel besser sind diese molekularen Risikoscores?
Als das Team die Scores in einer unabhängigen Gruppe von 24.287 Personen testete, für die alle Datentypen vorlagen, waren sowohl MetScore als auch ProScore allein starke Prädiktoren und teilten die Teilnehmenden über 15 Jahre Nachbeobachtung klar in Niedrig-, Mittel- und Hochrisikogruppen ein. Proteinbasierte Scores schnitten am besten ab und übertrafen häufig traditionelle polygenetische (DNA-basierte) Risikomaße deutlich. Die Ergänzung konventioneller klinischer Faktoren durch ProScore und MetScore verbesserte die Genauigkeit der Risikovorhersage für jedes untersuchte kardiovaskuläre Ergebnis, selbst wenn die Basismodelle bereits ausführlich waren. In einigen Fällen, insbesondere bei peripherer arterieller Verschlusskrankheit und Vorhofflimmern, war die Leistungssteigerung erheblich, und Entscheidungs-Kurven-Analysen deuteten darauf hin, dass Ärztinnen und Ärzte vorteilhaftere Entscheidungen darüber treffen könnten, wer präventiv behandelt werden sollte.
Was die Moleküle über die Krankheitsbiologie verraten
Über die Vorhersage hinaus fragten die Forschenden, welche spezifischen Moleküle in den KI-Modellen mit Hilfe einer Erklärmethode namens SHAP am einflussreichsten waren. Sie bestätigten die Bedeutung bekannter Marker wie Kreatinin und Albumin (als Hinweis auf Nierenfunktion und allgemeinen Gesundheitszustand) sowie entzündlicher Signale wie GlycA und herzbelastender Proteine wie NT‑proBNP. Gleichzeitig hoben die Modelle weniger bekannte Proteine und Metaboliten hervor, die mit Entzündung, Gerinnung, Gefäßumbau und sogar Nervenschäden verknüpft sind, mit teils gemeinsamen, teils krankheitsspezifischen Mustern. Interessanterweise erreichte kein einzelnes Molekül die Vorhersagekraft des kombinierten MetScore oder ProScore, was unterstreicht, dass kardiovaskuläres Risiko aus vielen subtilen Veränderungen entsteht, die zusammenwirken, statt aus einem einzelnen Übeltäter.
Von Big Data zu persönlicherer Herzversorgung
Die Studie kommt zu dem Schluss, dass die Verknüpfung von Genetik, detaillierten molekularen Blutprofilen und routinemäßigen klinischen Informationen unsere Einschätzung, wer wahrscheinlich schwere kardiovaskuläre Erkrankungen entwickelt, erheblich schärfen kann — oft ein Jahrzehnt oder länger im Voraus. Insbesondere Proteinmessungen scheinen reichhaltige, verwertbare Informationen über anhaltenden biologischen Stress zu liefern, lange bevor Symptome auftreten. Zwar sind die nötigen Tests derzeit noch nicht weit verbreitet oder günstig, aber die Kosten sinken, und die Autorinnen und Autoren haben ihren CardiOmicScore-Ansatz als Prototool verfügbar gemacht. Mit weiterer Validierung in vielfältigeren Populationen könnte ein derart KI-getriebenes Multiomik-Profiling Klinikerinnen und Klinikern helfen, von Einheits-Checklisten zu wirklich personalisierter Prävention überzugehen — Hochrisikopersonen früher zu identifizieren, Behandlungen an die zugrunde liegende Biologie anzupassen und möglicherweise die globale Belastung durch Herz- und Gefäßerkrankungen zu verringern.
Zitation: Luo, Y., Zhang, N., Yang, J. et al. AI-based multiomics profiling reveals complementary omics contributions to personalized prediction of cardiovascular disease. Nat Commun 17, 2269 (2026). https://doi.org/10.1038/s41467-026-68956-6
Schlüsselwörter: Vorhersage des kardiovaskulären Risikos, Proteomik, Metabolomik, Tiefes Lernen, Biomarker