Clear Sky Science · de
Verständnis der Förderung durch Alkalimetalle in der Hydrierungskatalyse über starke Metall–Base‑Wechselwirkung
Warum die Feinabstimmung von Katalysatoren für den Alltag wichtig ist
Die Umwandlung einfacher Moleküle wie Kohlendioxid und Wasserstoff in nützliche Brennstoffe und Chemikalien ist zentral für sauberere Energie und eine umweltfreundlichere Industrie. Viele der Metallkatalysatoren, die diese Reaktionen antreiben, enthalten bereits winzige Mengen an Alkalimetallen wie Natrium oder Kalium als „Promotoren“, doch ihre tatsächliche Rolle war überraschend unklar. Diese Studie deckt ein vereinheitlichendes Prinzip auf, wie diese Zusätze tatsächlich wirken, und liefert damit einen Weg, intelligentere Katalysatoren zu entwerfen, die Reaktionen gezielt in Richtung gewünschter Produkte und weg von Abfall lenken können.
Ein genauerer Blick auf verstärkte Metallkatalysatoren
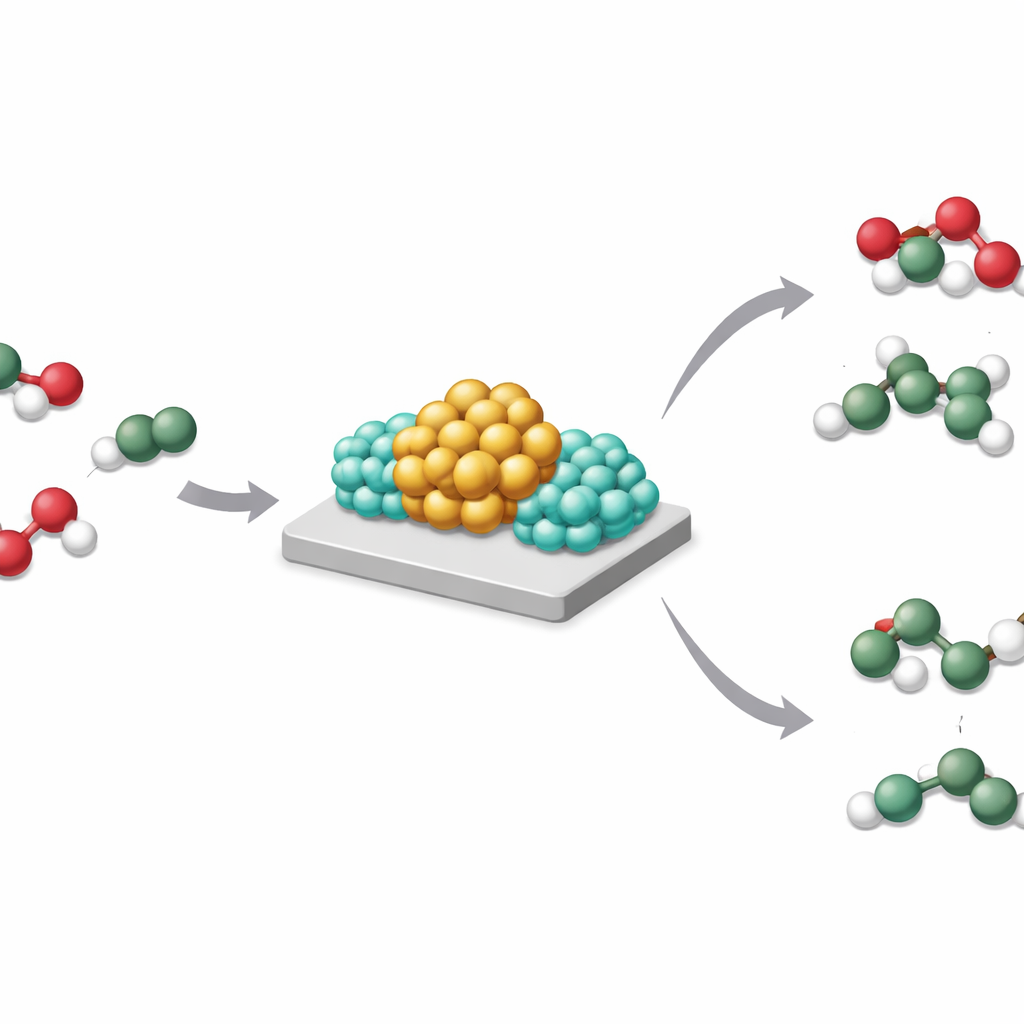
Katalysatoren aus Übergangsmetallen wie Rhodium und Nickel sitzen auf festen Trägern und helfen dabei, chemische Bindungen zu brechen und neu zu knüpfen. Seit Jahrzehnten mischt die Industrie Alkalimetalle bei, um diese Katalysatoren aktiver, selektiver oder langlebiger zu machen. Übliche Erklärungen konzentrierten sich auf einfache geometrische Effekte (Änderung von Partikelform und -größe) oder direkte Elektronenspende vom Alkalimetall zum aktiven Metall. Unter realen Betriebsbedingungen liegen diese Promotoren jedoch überwiegend als Oxide vor, nicht als freie Metallatome, was eine direkte Elektronenübertragung zu einem unvollständigen Bild macht.
Entdeckung einer starken Partnerschaft an der Oberfläche
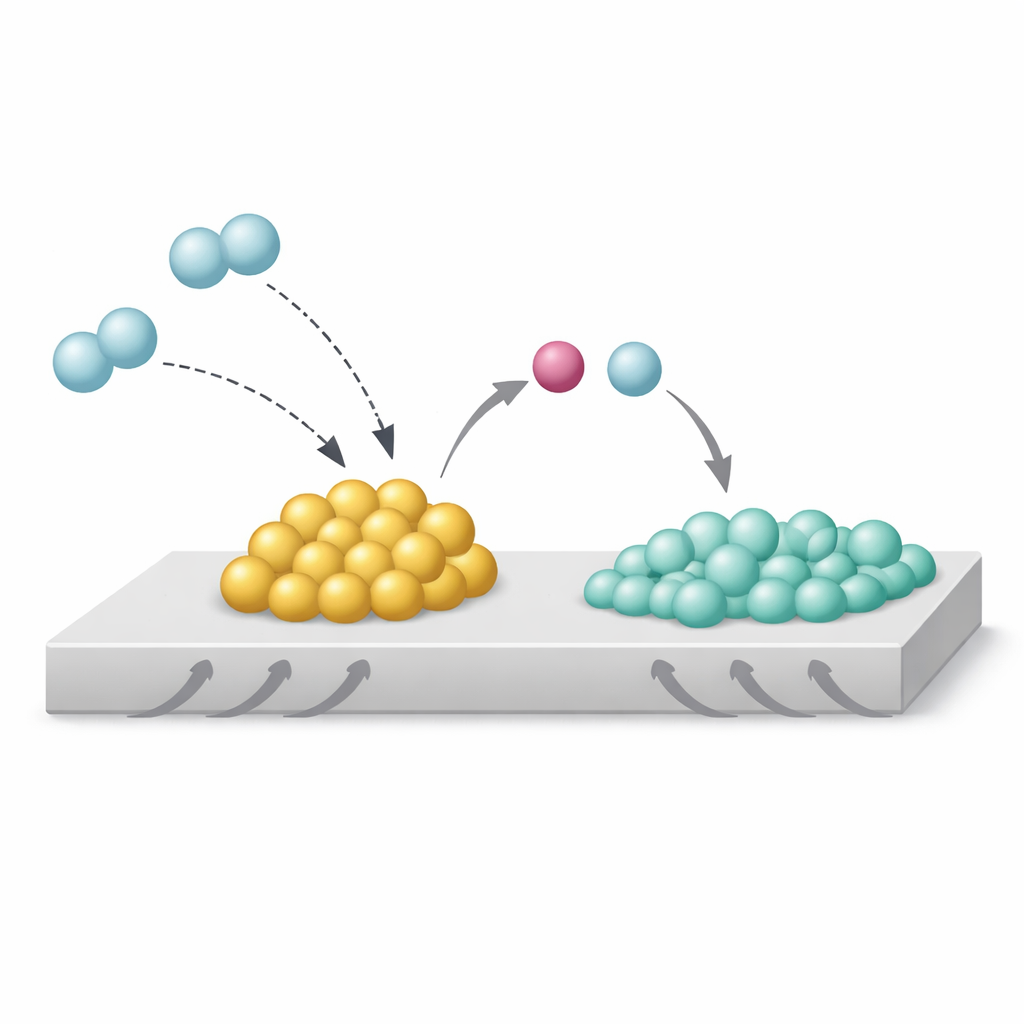
Die Autorinnen und Autoren untersuchten ein Modellsystem: Rhodium‑Nanopartikel auf Titandioxid, mit und ohne zugesetztem Natrium. Mithilfe fortschrittlicher Elektronenmikroskopie, Röntgenspektroskopie und Computersimulationen fanden sie heraus, dass Natrium als Oxid, Na₂O, genau an der Grenze sitzt, an der die Rhodiumpartikel den Träger berühren. Unter Wasserstoffbedingungen entsteht dadurch eine sogenannte Strong Metal–Base Interaction (SMBI). An diesen speziellen Kontaktpunkten spalten ankommende Wasserstoffmoleküle heterolytisch: das basischere Na₂O nimmt den protonenähnlichen Teil auf, während das Rhodium das elektronreiche Gegenstück hält. Diese heterolytische Spaltung macht die Rhodiumoberfläche ungewöhnlich elektronengereich und verhindert, dass Wasserstoff auf den Titandioxid‑Träger »überschwemmt« oder »spillovert«.
Wie dieser versteckte Effekt Reaktionen lenkt
Diese subtile Umverteilung von Wasserstoff und Elektronen hat große Folgen. Bei der Hydrierung von Kohlendioxid begünstigt unmodifiziertes Rhodium auf Titandioxid eine starke Hydrierung bis hin zu Methan. Wird Natrium zugesetzt, produziert derselbe Katalysator stattdessen hauptsächlich Kohlenmonoxid, einen wertvollen Baustein, und deutlich weniger Methan. Ein ähnliches Verhalten zeigt sich bei Einsatz von Lithium oder Kalium bzw. wenn Rhodium durch Nickel ersetzt wird. Die Autorinnen und Autoren zeigen, dass freie Wasserstoff‑Spillover auf dem Träger zu tiefer Hydrierung führt; wenn SMBI den Wasserstoff am Metall–Base‑Grenzbereich konzentriert und vom Träger fernhält, entstehen mildere Produkte.
Unterschiedliche Doppelbindungen, unterschiedliche Ergebnisse
Das Team untersuchte anschließend, wie SMBI typische organische Hydrierungsreaktionen beeinflusst, die Kohlenstoff‑Kohlenstoff‑, Kohlenstoff‑Sauerstoff‑ und Stickstoff‑Sauerstoff‑Doppelbindungen betreffen. Bei einer C=C‑Doppelbindung in Vinylacetat macht die Natriumförderung den Katalysator schneller, vermutlich weil das elektronengerechte Rhodium diese Bindung schwächt und schwächer gebundener Wasserstoff effizient addiert. Im Gegensatz dazu verlangsamt dieselbe Natriumzugabe bei Molekülen wie Acetophenon und Nitrobenzol die Reaktion, deren reaktive Gruppen bevorzugt auf dem Oxidträger sitzen. Hier verhindert der unterdrückte Wasserstoff‑Spillover, dass der Träger genug Wasserstoff erhält, um diese Umsetzungen voranzutreiben, und zeigt, dass nicht alle Doppelbindungen gleichermaßen von demselben Fördermechanismus profitieren.
Katalysatoren mit gezielter Steuerung entwerfen
Durch die Kombination von Experimenten und Theorie argumentieren die Autorinnen und Autoren, dass SMBI eine einheitliche Erklärung dafür liefert, wie Alkalimetall‑Promotoren katalytische Oberflächen umgestalten. Anstatt als einfache Elektronenspender zu wirken, agieren Alkalioxid‑Spezies als starke Protonenfallen, die die Wasserstoffspaltung polarisieren und reaktiven Wasserstoff in der Nähe der Metall–Base‑Schnittstelle konzentrieren. Diese Einsicht erklärt rätselhafte Trends über viele Hydrierungsreaktionen und Metalle hinweg und gibt eine praktische Designregel vor: Durch das Abstimmen von Menge und Position der Alkalioxide um Metallpartikel können Chemiker Reaktionen gezielt in Richtung bestimmter Produkte lenken und gleichzeitig Aktivität und Stabilität für sauberere chemische Prozesse optimieren.
Zitation: Jung, M., Dickieson, M.P., Chen, P. et al. Understanding alkali metal promotion in hydrogenation catalysis through Strong Metal–Base Interaction. Nat Commun 17, 2465 (2026). https://doi.org/10.1038/s41467-026-68952-w
Schlüsselwörter: Hydrierungskatalyse, Förderstoffe aus Alkalimetallen, CO2‑Umwandlung, heterogene Katalysatoren, Metall–Oxid‑Schnittstellen