Clear Sky Science · de
Proteomik des präfrontalen Kortex des menschlichen Gehirns identifiziert beeinträchtigten Energiestoffwechsel und neuronale Funktion bei Schizophrenie
Warum Energie und Verschaltung des Gehirns bei Schizophrenie wichtig sind
Schizophrenie wird oft anhand von Halluzinationen und Wahnvorstellungen beschrieben, aber unter den Symptomen liegt ein Problem darin, wie Gehirnzellen Energie nutzen und miteinander kommunizieren. Diese Studie untersucht die Chemie des präfrontalen Kortex — des Gehirnbereichs, der für Planung, Entscheidungsfindung und Arbeitsgedächtnis entscheidend ist — indem sie direkt Tausende von Proteinen in gespendeten menschlichen Gehirnen misst. Durch den Vergleich von Personen mit Schizophrenie mit sorgfältig abgeglichenen Personen ohne Erkrankung entdecken die Forschenden ein Muster: Die Energiefabriken des Gehirns scheinen weniger leistungsfähig zu sein, während die Kommunikations- und Signalgebungssysteme in einen Überbetriebsmodus geraten.
Ein genauer Blick auf das Denkzentrum des Gehirns
Das Team konzentrierte sich auf den dorsalen präfrontalen Kortex, eine Region, die wiederholt mit kognitiven Problemen bei Schizophrenie in Verbindung gebracht wurde. Mit lasergeführter Dissektion trennten sie die oberen und tieferen Schichten dieses Kortex von 96 postmortalen Gehirnen (47 mit Schizophrenie und 49 Kontrollen). Anschließend wendeten sie fortgeschrittene Massenspektrometrie an, um mehr als 5000 verschiedene Proteine zu quantifizieren. Eine wichtige Stärke der Arbeit ist, dass sie die Analyse unabhängig in beiden Kortexschichten wiederholten und zahlreiche mögliche Verzerrungen korrigierten, wie Alter, Zeit zwischen Tod und Gewebeaufbereitung sowie technische Verarbeitungsunterschiede. Das Muster der Veränderungen bei Schizophrenie erwies sich in den oberen und tieferen Schichten als hochgradig konsistent, was auf eine breit angelegte, schichtübergreifende Störung und nicht auf einen lokalisierten Defekt hindeutet.
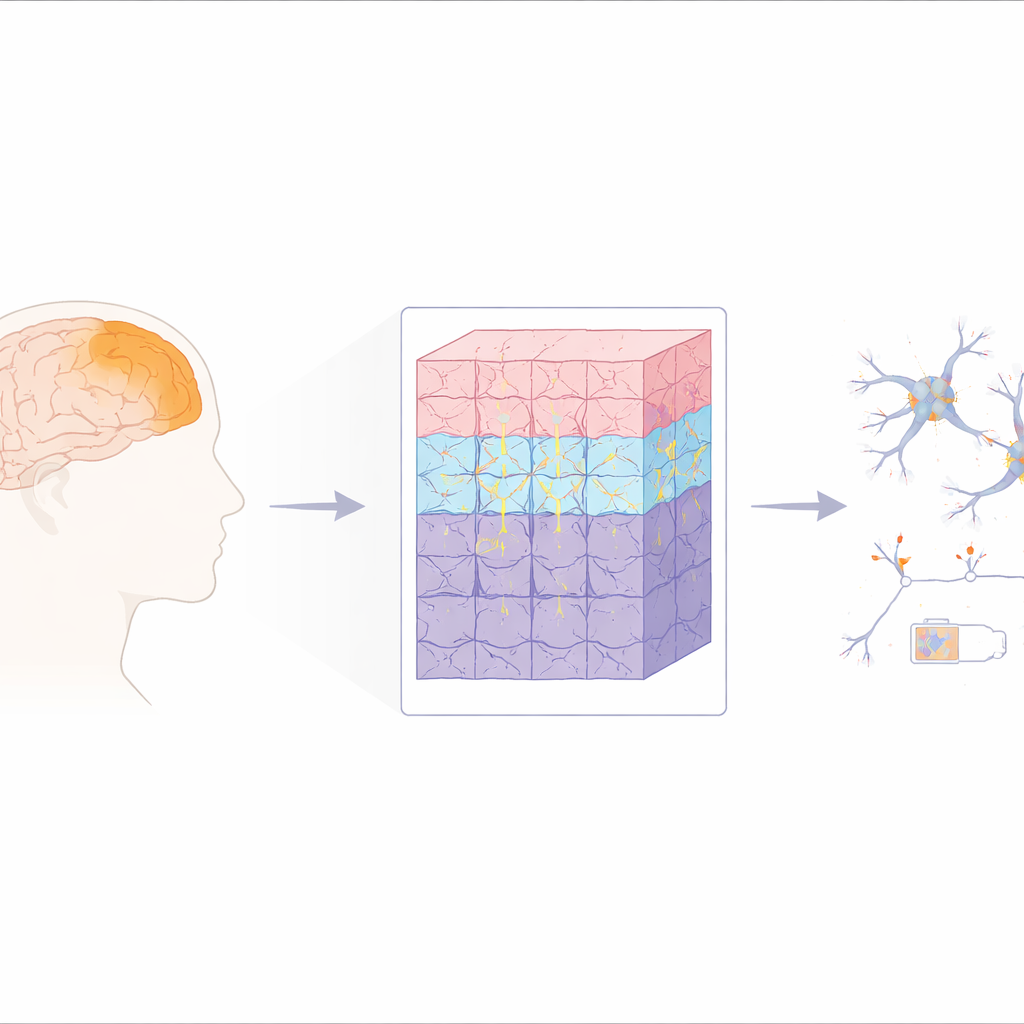
Energetische Fabriken arbeiten unter Kapazität
Eines der deutlichsten Signale war ein weit verbreiteter Rückgang von Proteinen, die in der inneren Membran der Mitochondrien sitzen — den kleinen Strukturen, die den Großteil des neuronalen Brennstoffs in Form von ATP erzeugen. Komponenten mehrerer wichtiger Schritte der energieerzeugenden Kette — bekannt als Komplexe I, II, IV und V — waren vermindert. Diese Komplexe helfen beim Elektronentransport und beim Protonenpumpen, um die ATP‑Synthase, die letzte Turbine zur ATP‑Herstellung, anzutreiben. Wenn die Proteine, aus denen diese Maschinerie besteht, seltener sind, fällt die Fähigkeit des Systems zur Energieproduktion wahrscheinlich ab. Die Studie fand außerdem weniger Bausteine für Ribosomen, die Proteinfabriken der Zelle, sowie Bestandteile des Proteasoms, das abgenutzte Proteine abbaut. Zusammengenommen deuten diese Veränderungen auf ein Hirnumfeld mit geringerer Energieversorgung und einer reduzierten Fähigkeit hin, zelluläre Komponenten kontinuierlich zu erneuern und zu entfernen.
Signal- und Transportsysteme im Übertrieb
Im auffälligen Kontrast dazu waren viele Proteine, die Signale und zellulären Verkehr steuern, in Schizophreniegehirnen erhöht. Die Forschenden beobachteten höhere Konzentrationen zahlreicher Kinasen — Enzyme, die andere Proteine durch Phosphorylierung an- oder abschalten — sowie Proteine, die kleine molekulare Schalter namens GTPasen regulieren. Diese Schalter steuern Membrantransport und den intrazytoplasmatischen Transport von Fracht. Proteine, die an Materialtransport entlang des zellulären Skeletts und am Vesikeltransport zur und von der Zelloberfläche beteiligt sind, waren ebenfalls vermehrt vorhanden. Analysen, die auf Synapsen — die Verbindungsstellen, an denen Neurone Informationen austauschen — fokussierten, zeigten, dass sowohl die präsynaptische als auch die postsynaptische Seite veränderte Proteinsätze aufwiesen. Das legt nahe, dass sowohl die Maschinerie zur Freisetzung chemischer Botenstoffe als auch die Strukturen, die diese empfangen, gestört sind.
Gene, Gehirnzellen und Krankheit verbinden
Um diese Proteinveränderungen in einen breiteren biologischen Kontext zu stellen, verglichen die Autorinnen und Autoren ihre Ergebnisse mit großen genetischen Studien zur Schizophrenie und mit einzelkernigen RNA‑Sequenzdaten aus derselben Gewebe‑Kohorte. Viele der veränderten Proteine gehörten zu Genmengen, die bereits durch genomweite Assoziationsstudien, insbesondere für Schizophrenie und bipolare Störung, in Verbindung gebracht wurden, was darauf hindeutet, dass die beobachteten Proteinstörungen auf ererbtem Risiko aufbauen. Ein erheblicher Teil der betroffenen Signalwege — besonders jene, die mit mitochondrialer Funktion und oxidativer Phosphorylierung zusammenhängen — zeigte ähnliche Trends auf RNA‑Ebene, was die These stützt, dass es sich nicht um zufälliges Rauschen handelt. Einige Merkmale, wie der breite Anstieg von Kinasen und spezifischen synaptischen Regulatoren, kamen jedoch auf Proteinebene stärker zum Ausdruck, was auf zusätzliche Kontrollschichten nach der RNA‑Synthese hinweist.
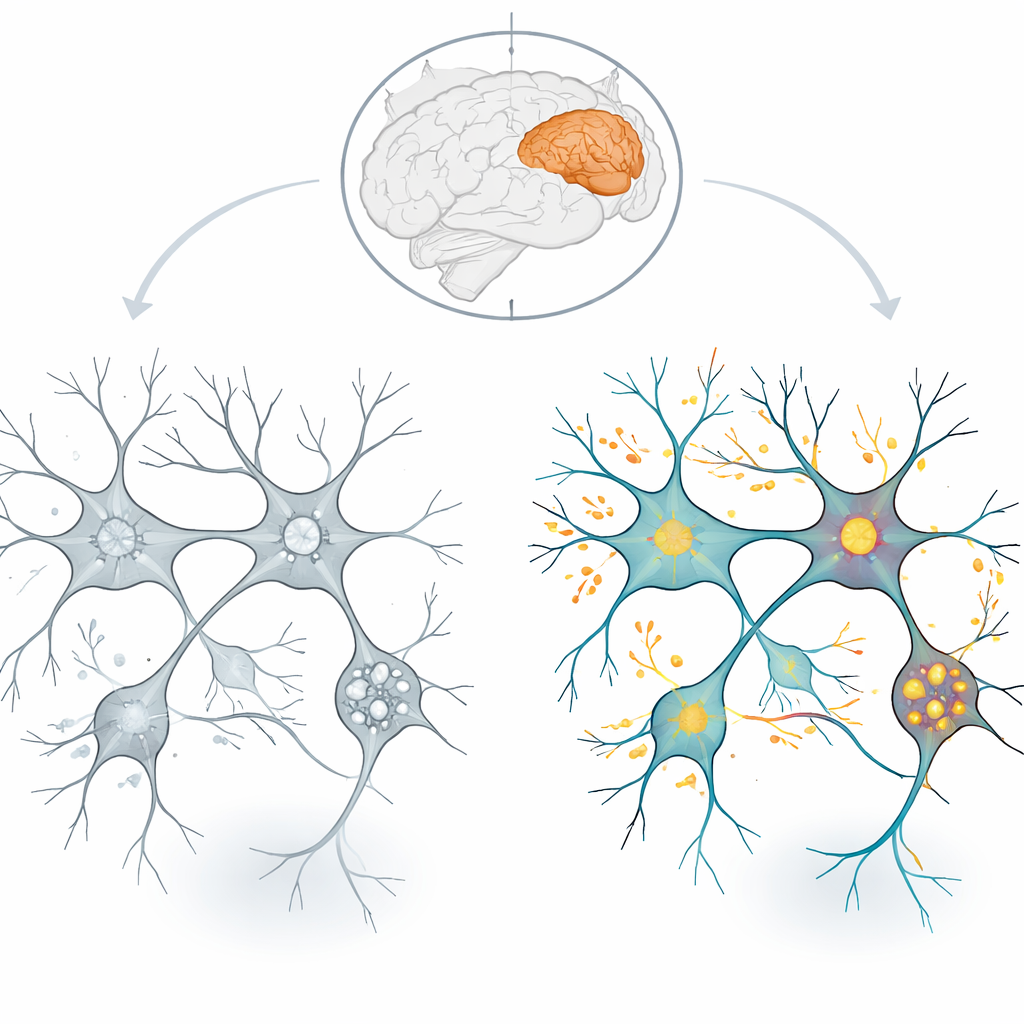
Was das für das Verständnis und die Behandlung von Schizophrenie bedeutet
Für eine interessierte Leserschaft ist die Kernbotschaft, dass Schizophrenie im präfrontalen Kortex wie ein Missverhältnis zwischen Angebot und Nachfrage aussieht. Auf der einen Seite sind die energieproduzierenden und wartenden Systeme des Gehirns heruntergefahren; auf der anderen Seite sind die Signal‑ und Kommunikationsnetzwerke hochgefahren und umgestaltet. Neurone gehören zu den energiehungrigsten Zellen des Körpers, insbesondere an ihren Synapsen, weshalb selbst moderate, langanhaltende Einbußen in der ATP‑Produktion es ihnen erschweren könnten, präzise und schnelle Kommunikation aufrechtzuerhalten. Die Autorinnen und Autoren argumentieren, dass dieser chronische Energiemangel, kombiniert mit veränderten synaptischen und Transportproteinen, den Grund für die kognitiven Schwierigkeiten und andere Symptome der Schizophrenie bilden könnte. Ihre Arbeit weist auf Strategien hin, die die mitochondriale Funktion stärken und ein gesundes synaptisches Gleichgewicht wiederherstellen, als vielversprechende Richtungen für künftige Therapien.
Zitation: Koopmans, F., Dijkstra, A.A., Li, WP. et al. Human brain prefrontal cortex proteomics identifies compromised energy metabolism and neuronal function in Schizophrenia. Nat Commun 17, 2131 (2026). https://doi.org/10.1038/s41467-026-68950-y
Schlüsselwörter: Schizophrenie, präfrontaler Kortex, Mitochondrien, synaptische Proteine, Gehirnproteomik