Clear Sky Science · de
RiboBright zeigt zelltypspezifische Unterschiede in Organisation und Bewegung der Ribosomen
Die Proteinfabriken der Zelle sichtbar werden lassen
Sekunde für Sekunde produzieren unsere Zellen mit winzigen Maschinen, den Ribosomen, Tausende neuer Proteine. Bislang war es überraschend schwierig zu beobachten, wo diese Maschinen in lebenden Zellen sitzen und wie sie sich bewegen. Diese Studie stellt RiboBright vor, ein kleines fluoreszierendes Molekül, das an Ribosomen bindet und sie zum Leuchten bringt, sodass Forscher diese Proteinfabriken Zelle für Zelle verfolgen können. Die Arbeit zeigt, dass Ribosomen in verschiedenen Zelltypen sehr unterschiedlich organisiert und genutzt werden, besonders wenn Stammzellen ihre zukünftige Identität wählen.
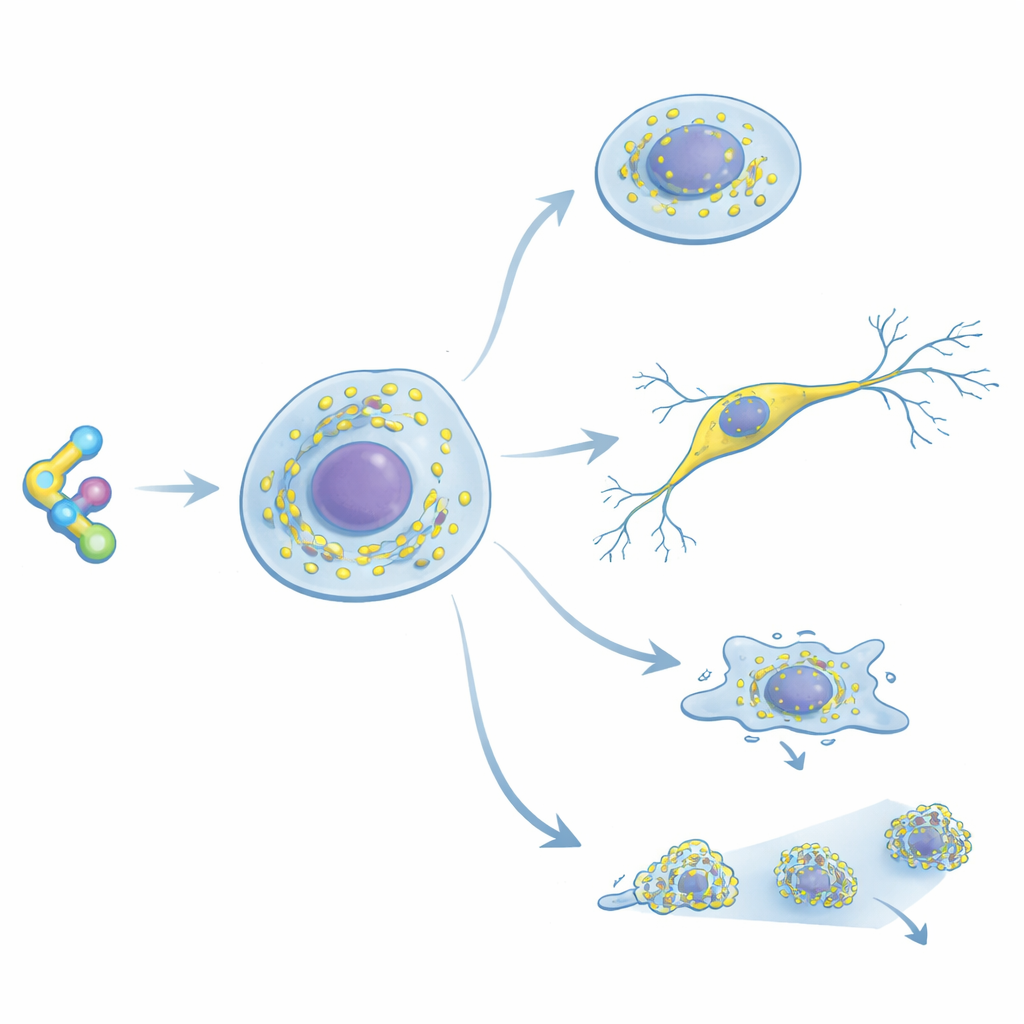
Ein neuer Weg, Ribosomen hervorzuheben
Die Forscher bauten RiboBright, indem sie Cycloheximid modifizierten, ein klassisches Medikament, das dafür bekannt ist, in Tieren und Menschen stark und selektiv an Ribosomen zu binden. Sie befestigten einen speziellen „molekularen Rotor“-Farbstoff an einer Position des Wirkstoffs, die seine Bindung an das Ribosom nicht schwächt. Dieser Farbstoff leuchtet kaum, wenn er sich frei in Lösung dreht, wird aber hell, wenn seine Bewegung eingeschränkt ist – etwa wenn die Sonde in das Ribosom einklemmt. Tests in Reagenzgläsern zeigten, dass die modifizierten Moleküle die Proteinproduktion bei nahezu denselben Dosen wie das ursprüngliche Medikament noch hemmen, was bestätigt, dass sie gut binden. In lebenden Zellen erzeugte eine Version besonders scharfe, helle Punkte, was darauf hinweist, dass sie das richtige Gleichgewicht zwischen starker Ribosomenbindung und intensiver Lichtemission besitzt; diese optimierte Sonde nannten die Autor:innen RiboBright.
Nachweis, dass die Sonde echte Ribosomen markiert
Um sicherzugehen, dass RiboBright tatsächlich Ribosomen markiert, kombinierte das Team mehrere komplementäre Methoden. Wenn Zellen zuvor entweder mit Cycloheximid selbst oder mit einer anderen, nicht verwandten ribosomenblockierenden Verbindung behandelt wurden, verschwand das RiboBright-Signal nahezu vollständig, was nahelegt, dass alle drei um dieselbe Bindungstasche konkurrieren. Chemische Untersuchungen der ribosomalen RNA zeigten außerdem, dass RiboBright dasselbe Nukleotid schützt, das auch Cycloheximid abschirmt, konsistent mit einem identischen Andockort. Mikroskopie mit hoher Auflösung zeigte, dass das RiboBright-Signal stark mit Markern für die große ribosomale Untereinheit und mit Strukturen wie dem endoplasmatischen Retikulum und Mitochondrien überlappt, wo viele Ribosomen sitzen. Gleichzeitig schwimmen einige helle Punkte frei im Zytoplasma, wahrscheinlich mobile Ribosomen, die nicht an Membranen gebunden sind.
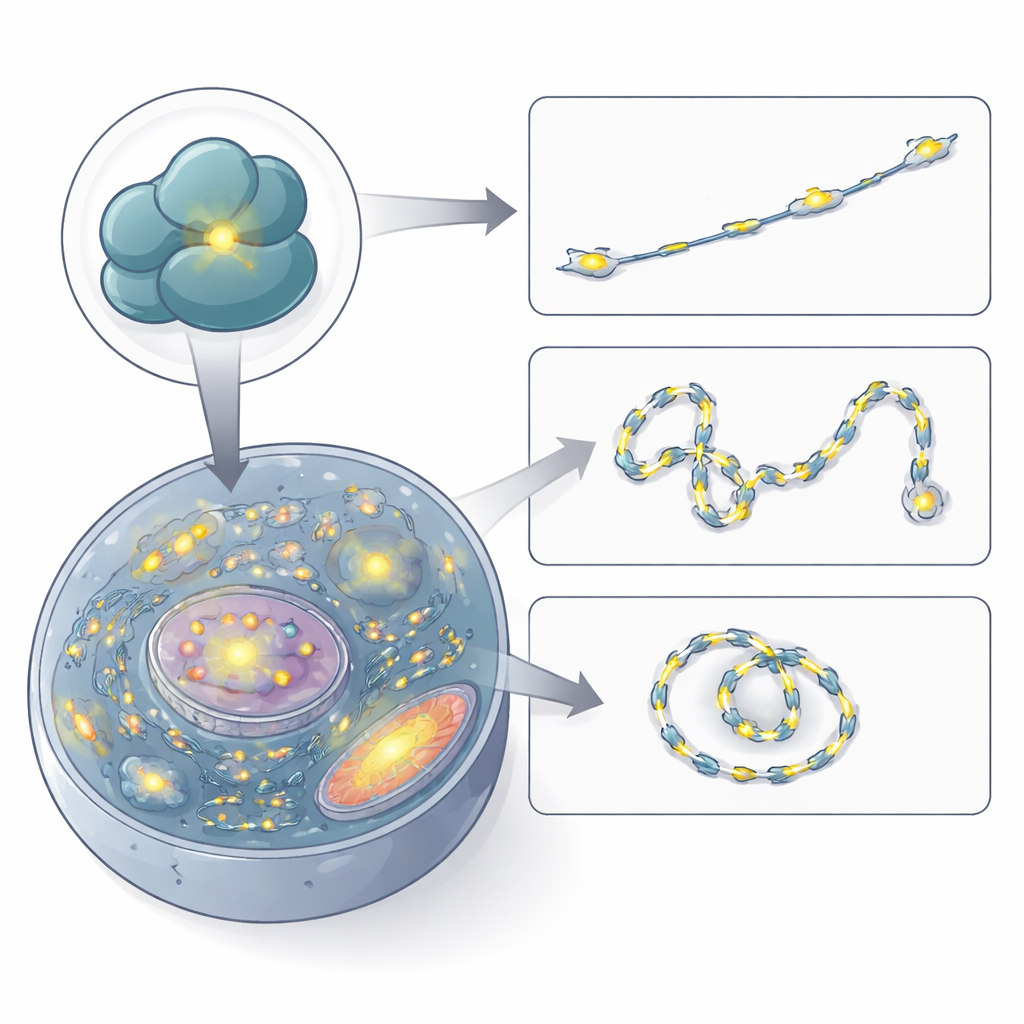
Ribosomenbewegung in lebenden Zellen beobachten
Mit gesicherter Spezifität nutzten die Autor:innen RiboBright, um Ribosomen in Aktion zu filmen. Durch Aufnahmen alle paar hundert Millisekunden verfolgten sie die Bahnen einzelner fluoreszierender Punkte durch die Zelle. Viele Punkte bewegten sich kaum oder blieben auf kleinen Bereichen begrenzt, was auf Ribosomen hindeutet, die an Ort und Stelle an gebundenen Boten-RNAs oder am endoplasmatischen Retikulum übersetzen. Andere schritten in diffuser, zufälliger Weise umher, und ein kleinerer Anteil zeigte klare gerichtete Bewegungen, was auf aktiven Transport entlang zellulärer Schienen hinweist. Die gemessenen Geschwindigkeiten stimmen mit früheren Schätzungen für Boten-RNAs und Ribosomencluster überein und bestätigen, dass RiboBright realistische Ribosomendynamiken in Echtzeit erfassen kann.
Verschiedene Zelltypen, verschiedene Ribosomenstrategien
RiboBright zeigte außerdem, wie stark Ribosomengehalt und -organisation von der Zellidentität abhängen. In zehn menschlichen und Maus-Zelllinien, darunter Stammzellen, Krebszellen und nicht-krebsartige Zellen, variierten Muster und Helligkeit der Ribosomenpunkte dramatisch. Manche Zellen enthielten große, helle Cluster, die Regionen intensiver Proteinsynthese entsprechen könnten, während andere vorwiegend kleine, verstreute Punkte zeigten. Überraschenderweise sagte die schiere Zahl der Ribosomen in einer Zelle nicht zuverlässig voraus, wie viel Protein sie herstellte: In den meisten Zelltypen korrelierten Proteinproduktion und Ribosomengehalt wenig miteinander. Embryonale Stammzellen fielen dadurch auf, dass sie eine geringe Produktivität pro Ribosom und relativ gleichmäßige Translation zwischen einzelnen Zellen zeigten, was darauf hindeutet, dass sie große Reserven wenig genutzter Ribosomen vorhalten und gleichzeitig die Schwankungen der Proteinproduktion gering halten.
Ribosomen während früher Zellschicksalsentscheidungen
Das Team verfolgte dann Maus-embryonale Stammzellen, während diese begannen, sich in zwei frühe Linien zu differenzieren: einen ectodermähnlichen Zweig und einen extraembryonalen Endoderm (XEN)-ähnlichen Zweig. Mit RiboBright und Oberflächenmarkern für Zellen stellten sie fest, dass beide entstehenden Linien etwas mehr Gesamt-Ribosomengehalt als undifferenzierte Zellen erwarben, diese Ribosomen aber unterschiedlich anordneten. XEN-ähnliche Zellen, die lange Ausläufer entwickeln, zeigten langsamere und stärker eingeschränkte Ribosomenbewegung, konsistent mit lokalisierter Proteinsynthese in spezialisierten Regionen. Im Gegensatz dazu zeigten ectodermähnliche Zellen mobilere Ribosomen und entwickelten nach etwa zwei Tagen auffällige „Translations-Hubs“, in denen sowohl Ribosomensignal als auch neue Proteinsynthese ihren Höhepunkt erreichten. Über die ersten 72 Stunden der Differenzierung sanken die Gesamtproteinproduktion und die Ribosomenzahlen moderat, doch die verbleibenden Ribosomen wurden etwas effizienter, besonders in den differentiierenden Zellen.
Was das für das Verständnis von Zellen bedeutet
Zusammen zeichnen diese Befunde ein reichhaltigeres Bild von Ribosomen als dynamischen, kontextabhängigen Maschinen statt einheitlicher Arbeitstiere. RiboBright bietet Forscher:innen ein praktisches Werkzeug, um Ribosomen in vielen Zelltypen zu visualisieren und zu zählen, in fixierten wie in lebenden Proben, und um Position und Bewegung von Ribosomen mit der tatsächlichen Proteinproduktion einer Zelle in Beziehung zu setzen. Für Nicht-Fachleute ist die wichtigste Erkenntnis, dass Zellen nicht nur einstellen, wie viele Proteinfabriken sie bauen, sondern auch, wo sie diese platzieren und wie aktiv sie betrieben werden — abhängig von Zelltyp und Entwicklungszustand. Diese neue fluoreszierende Sonde macht jene verborgene Logistik sichtbar und eröffnet die Möglichkeit, zu untersuchen, wie Ribosomenverhalten zur Entwicklung, Krankheit und zur Reaktion auf Therapien beiträgt.
Zitation: Poulladofonou, G., Grandi, C., Hu, X. et al. RiboBright reveals cell-type-specific differences in ribosome organization and movement. Nat Commun 17, 2734 (2026). https://doi.org/10.1038/s41467-026-68947-7
Schlüsselwörter: Ribosomen, fluoreszierende Sonden, Einzelzellanalyse, Stammzelldifferenzierung, Proteinsynthese