Clear Sky Science · de
Ein allosterischer Inhibitor des Zika-Virus-NS2B-NS3-Protease mit oraler Wirksamkeit in Mausmodellen
Eine neue Methode, einen gefährlichen Virus auszutricksen
Das Zika-Virus sorgte vor einem Jahrzehnt weltweit für Schlagzeilen, als Infektionen bei Schwangeren mit Kindern mit ungewöhnlich kleinem Kopf und Hirnschäden in Verbindung gebracht wurden. Bis heute gibt es jedoch kein zugelassenes Medikament zur Behandlung oder Vorbeugung von Zika. Diese Studie beschreibt eine vielversprechende, pillenähnliche Verbindung, die ein zentrales virales Enzym auf unerwartete Weise ausschaltet und Mäuse vor einer schweren Zika-Infektion schützt — ein möglicher Weg zu einem zukünftigen Medikament, das besonders verletzliche Menschen während Ausbrüchen schützen könnte.
Warum Zika weiterhin wichtig ist
Das Zika-Virus wird hauptsächlich von Aedes-Mücken übertragen und gehört zur selben Familie wie Dengue- und West-Nil-Viren. Die meisten Infizierten haben wenig oder gar keine Symptome, doch etwa jeder fünfte entwickelt Probleme von Fieber und Hautausschlag bis hin zu schweren Komplikationen wie Augenschäden, Organversagen und Störungen des Nervensystems. Die größte Gefahr besteht für Föten: Eine Infektion während der Schwangerschaft kann zu Mikrozephalie und lebenslanger Behinderung führen. Da weder ein zugelassener Impfstoff noch eine antivirale Behandlung verfügbar sind, können Ärztinnen und Ärzte nur unterstützende Pflege anbieten. Wissenschaftler betrachten Zika daher als Priorität für die Pandemie-Vorsorge und suchen nach Medikamenten, die sowohl gefährdete Gruppen schützen als auch neue Ausbrüche eindämmen könnten.
Auf der Suche nach verborgenen Schwachstellen
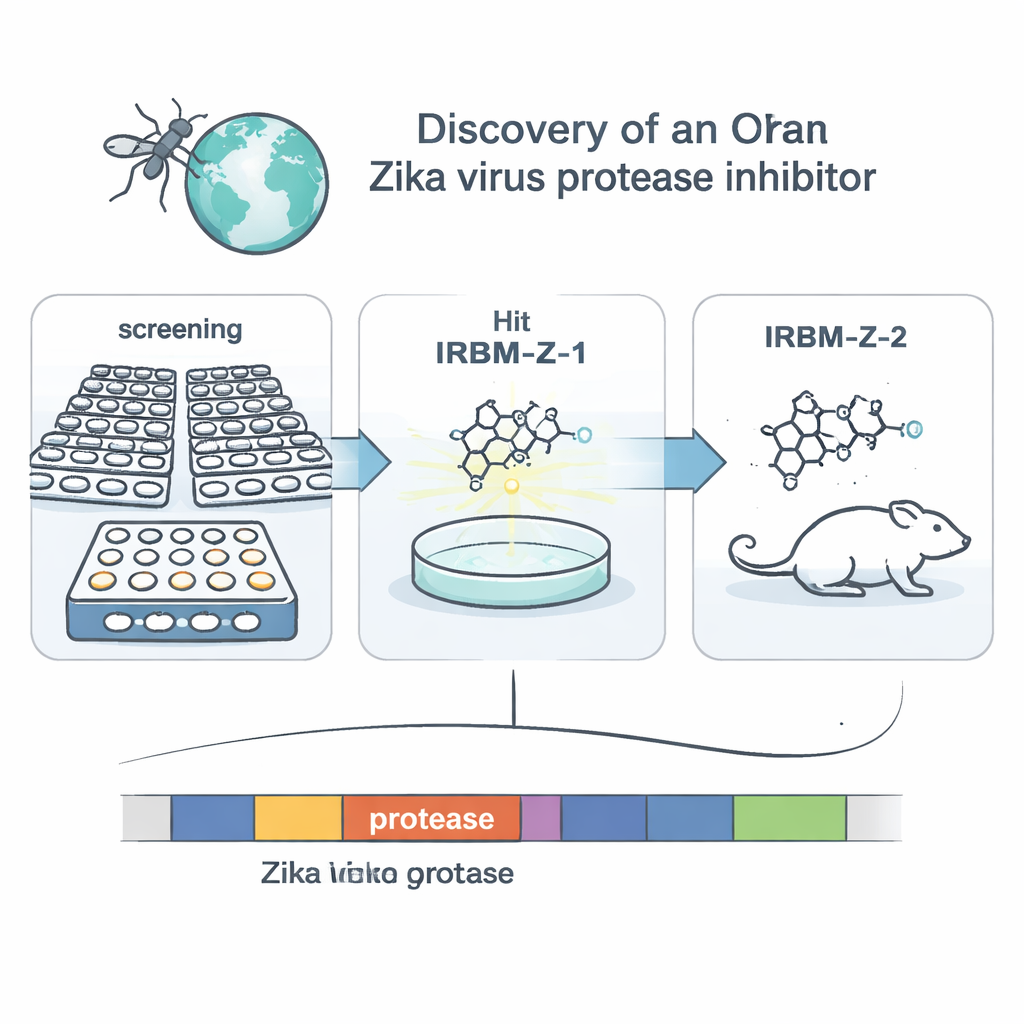
Die Forschenden konzentrierten sich auf ein virales Enzym namens NS2B–NS3-Protease. Diese molekularen „Schere“ zerschneidet das große virale Vorläuferprotein in die Stücke, die zum Aufbau neuer Viren benötigt werden, und ist daher ein attraktives Wirkstoffziel. Anstatt ein Medikament gegen die offensichtliche Schnittstelle zu entwerfen, nutzte das Team ein zellbasiertes Screening-System, das die Zika-Replikation in Affennierenzellen nachahmt. Sie bauten ein modifiziertes Zika-Genom, einen sogenannten Replikon, der strukturelle Gene nicht enthält, dafür aber einen Luciferase-Reporter, sodass die Lichtemission die Virusvermehrung nachverfolgt. Nach dem Screening von mehr als 120.000 kleinen Molekülen aus einer nationalen Chemikaliensammlung wählten sie solche aus, die das Lichtsignal stark reduzierten, ohne Zellen zu schädigen, und züchteten anschließend Virusreplikons, die gegen jeden Treffer resistent wurden. Diese genetische Spurensuche wies auf die Protease als Schlüsselziel für eine Wirkstofffamilie hin, angeführt von einem Initialmolekül namens IRBM-Z-1.
Das Enzym in die falsche Form sperren
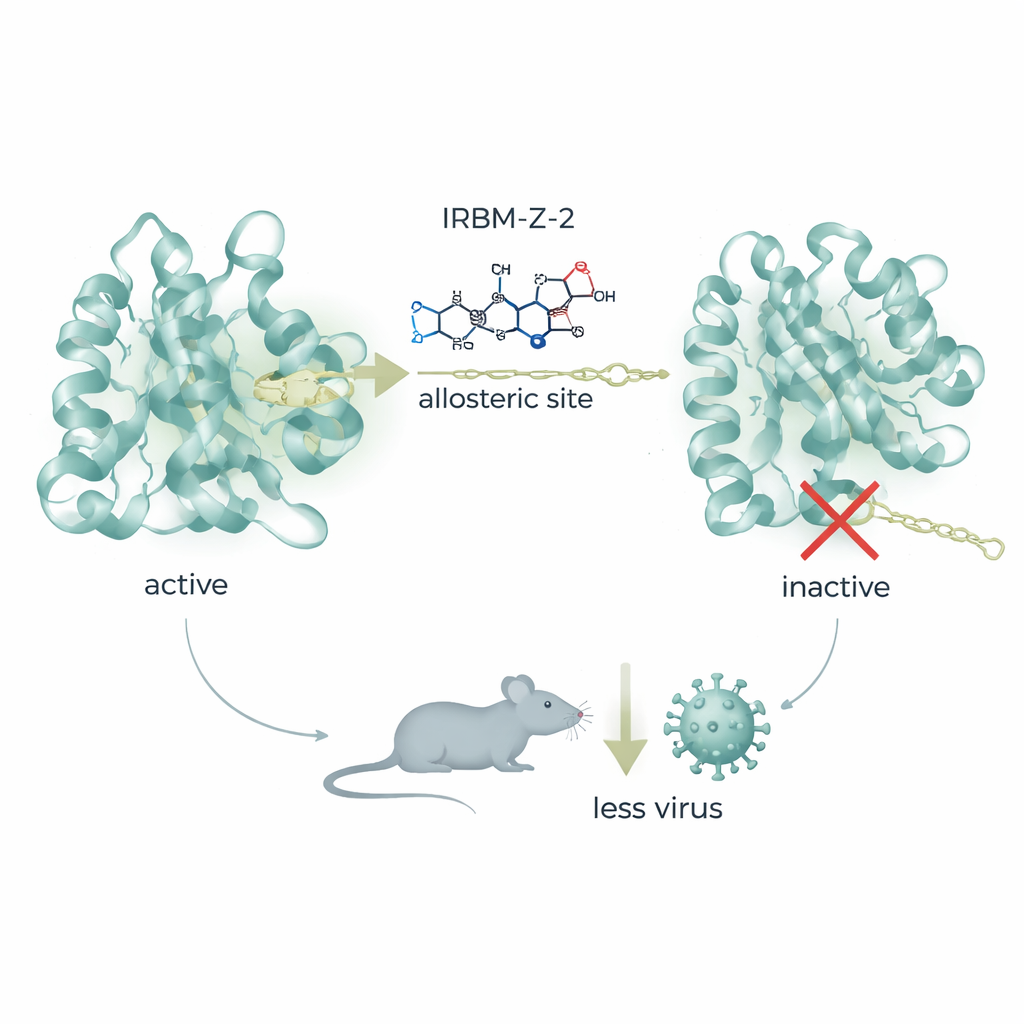
Biochemische Tests zeigten, dass IRBM-Z-1 nicht mit dem üblichen Substrat an der Schnittstelle konkurrierte. Stattdessen verhielt es sich wie ein nicht-kompetitiver beziehungsweise allosterischer Inhibitor — es bindet an einer separaten Tasche und verhindert, dass das Enzym seine aktive Form annimmt. Hochauflösende Röntgenkristallographie enthüllte, dass die Verbindung in eine zuvor unbekannte Tasche weit entfernt vom katalytischen Zentrum passt. Dort bildet ihr ungewöhnlicher „N‑acylsydnon‑imin“-Kern ein Netz aus Wasserstoffbrücken und Stapelwechselwirkungen, die eine Schlüsselregion der Protease in eine offene, inaktive Konformation drücken. Eine einzelne Aminosäureänderung in dieser Region, an Position 156, macht das Virus resistent und unterstreicht, wie gezielt die Verbindung diese verborgene Stelle ausnutzt. Diese Tasche unterscheidet sich außerdem von allosterischen Stellen, die bei verwandten Flaviviren beschrieben wurden, und bietet damit einen wirklich neuen Ansatzpunkt für Wirkstoffdesign.
Vom Treffer zum schützenden Medikament in Mäusen
Anhand struktureller Erkenntnisse verfeinerte das Team IRBM-Z-1 zu einem potenteren Molekül namens IRBM-Z-2. Die verbesserte Verbindung blockiert die Zika-Protease in Nanomolarkonzentrationen, hemmt die Virusreplikation in mehreren Zelltypen stark und zeigt Aktivität gegen verwandte Dengue- und West-Nil-Proteasen, während menschliche Enzyme verschont bleiben. In Tierversuchen zeigte IRBM-Z-2 vorteilhafte „arzneimittelähnliche“ Eigenschaften: Es war im Körper stabil, zeigte gute orale Resorption und hielt die Blutspiegel deutlich über den für die Virushemmung notwendigen Werten, ohne klare Hinweise auf Toxizität. In hoch empfänglichen AG129-Mäusen, die mit Zika infiziert wurden, senkte die tägliche Behandlung — entweder per Injektion oder oral — die Menge an viraler RNA im Blut dramatisch, verhinderte Gewichtsverlust und Krankheitssymptome und ließ alle behandelten Tiere überleben, während unbehandelte Kontrollen der Infektion erlagen.
Was das für künftige Ausbrüche bedeuten könnte
Insgesamt stellen diese Ergebnisse eine neuartige Klasse von Zika-Antiviralia vor, die wirken, indem sie ein kritisches virales Enzym in einer inaktiven Stellung „einfrieren“, statt dessen aktiven Ort direkt zu blockieren. Weil IRBM-Z-2 oral verabreicht werden kann, in strengen Mausmodellen starken Schutz zeigt und bislang ein sauberes Sicherheitsprofil aufweist, sticht es als vielversprechender Kandidat für weitere Entwicklungsstufen hervor — möglicherweise, um Schwangere, Gesundheitsfachkräfte und Reisende zu schützen, falls Zika wieder auftritt. Allgemeiner könnte die neu entdeckte allosterische Tasche ähnliche Wirkstoffe gegen verwandte Viren inspirieren und damit eine neue Front im Kampf gegen durch Mücken übertragene Krankheiten eröffnen.
Zitation: Ontoria, J.M., Torrente, E., Missineo, A. et al. An allosteric inhibitor of the Zika virus NS2B-NS3 protease with oral efficacy in mouse models. Nat Commun 17, 1439 (2026). https://doi.org/10.1038/s41467-026-68943-x
Schlüsselwörter: Zika-Virus, antivirales Medikament, Proteaseinhibitor, allosterische Modulation, durch Mücken übertragene Krankheit