Clear Sky Science · de
FCHo2, nicht Talin, ermöglicht Inside-out-Aktivierung von Integrin ɑvβ5 in gekrümmten Adhäsionen
Wie Zellen die Form ihrer Umgebung wahrnehmen
Unsere Körper bestehen aus Zellen, die ständig an ihrer Umgebung zupacken, ziehen und drücken, um sich zu bewegen, zu teilen oder an Ort und Stelle zu bleiben. Diese Studie zeigt, dass Zellen nicht nur die Steifigkeit ihrer Umgebung messen — sie lesen auch deren Form. Indem sie ein spezielles Adhäsionssystem beschreiben, das sich nur dort einschaltet, wo die Zellmembran stark gekrümmt ist, demonstrieren die Autoren, dass Zellen für flache gegenüber faserigen Umgebungen unterschiedliche innere „Griffe“ verwenden. Das hat wichtige Konsequenzen dafür, wie Gewebe entstehen und wie Krebs sich ausbreiten kann.
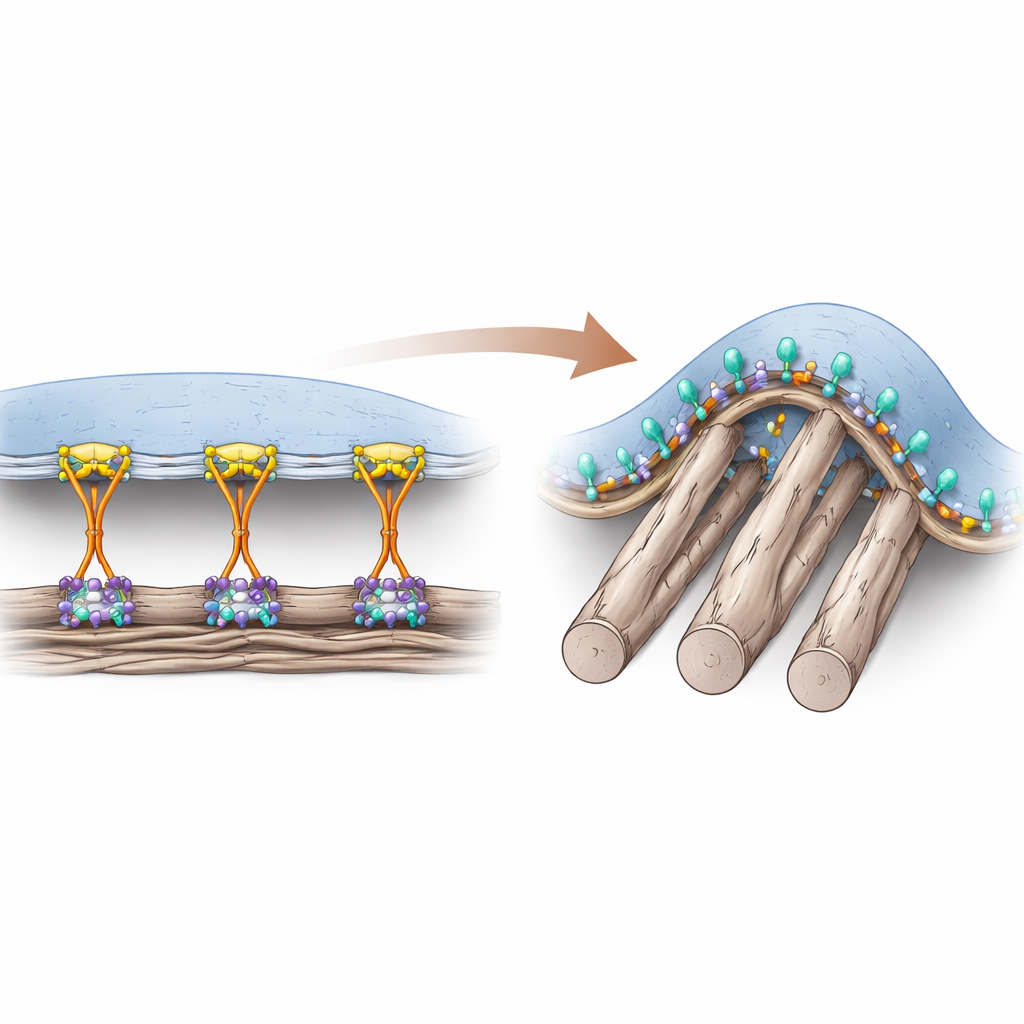
Zwei Arten, wie Zellen sich halten
Zellen heften sich an das proteinreiche Umfeld mithilfe von Oberflächenrezeptoren, den Integrinen. Lange Zeit galt das Hilfsprotein Talin als unverzichtbar, um Integrine von innen zu aktivieren und so starke Verbindungen in den klassischen Verankerungsstellen, den focal adhesions (Fokaladhäsionen), zu ermöglichen. Diese Adhäsionen bilden sich vor allem auf flachen, starren Oberflächen und übertragen große Zugkräfte über das Zytoskelett. In lebendem Gewebe sind viele der umgebenden Fasern jedoch weich und zylindrisch, sodass gekrümmte Kontaktstellen entstehen, die solche kraftintensiven Strukturen nicht leicht tragen. Die Autoren hatten zuvor eine andere Adhäsionsstruktur beschrieben — die „curved adhesion“ (gek rümmte Adhäsion) — die genau dort auftritt, wo die Membran um dünne Fasern gebogen ist und die auf ein spezifisches Integrin, αvβ5, angewiesen ist.
Gekrümmte Griffe verwenden einen anderen Helfer
In der neuen Studie zeigen die Forschenden, dass Talin zwar weiterhin vorhanden ist, aber nicht der entscheidende Aktivator von Integrin αvβ5 in gekrümmten Adhäsionen ist. Stattdessen übernimmt ein krümmungs-sensitives Protein namens FCHo2 diese Rolle. Mithilfe präzise konstruierter nano-großer Stäbchen und Säulen, die Zellmembranen kontrolliert biegen, beobachteten sie, dass αvβ5 an gekrümmten Bereichen stark klumpt — jedoch nur, wenn FCHo2 an eine sehr kurze Sequenz binden kann, ein HDRRE-Motiv, das direkt innen am β5-Schwanz liegt. Wird dieses Motiv gestört, funktioniert das Integrin weiterhin in Fokaladhäsionen, kann aber keine gekrümmten Adhäsionen mehr bilden. Ein Herunterregulieren von FCHo2 lässt die klassischen Fokaladhäsionen weitgehend intakt, beseitigt jedoch die gekrümmten Adhäsionen; das Entfernen von Talin schwächt dagegen die Fokaladhäsionen stark, während die gekrümmten Adhäsionen weitgehend unberührt bleiben.
Ein einzelner Aminosäure-Schalter als Formwähler
Ein Rätsel war, warum ein eng verwandtes Integrin, αvβ3, keine gekrümmten Adhäsionen bilden kann, obwohl sein innerer Schwanz β5 sehr ähnlich sieht. Durch Domänentausch zwischen den beiden Integrinen und gezielte Punktmutationen identifizierten die Autoren eine einzelne Schlüsselposition in der Nähe der Talin-Bindungsstelle: Die meisten β-Integrine besitzen ein Tryptophan (W), aber β5 hat einzigartig eine Tyrosinrest (Y766). Ersetzte man das Tyrosin von β5 durch Tryptophan, verlor das Integrin die Fähigkeit, an gekrümmten Adhäsionen teilzunehmen, und verhielt sich eher wie β3, das nur Fokaladhäsionen bevorzugt. Die umgekehrte Änderung — Tyrosin in die β3-ähnliche Chimäre einzubauen — stellte die Krümmungssensitivität wieder her. Weitere Experimente mit Varianten, die phosphorylierte oder nicht-phosphorylierte Zustände dieses Tyrosins nachahmen, deuten darauf hin, dass dessen chemische Modifikation das Integrin zugunsten entweder flacher, kraftintensiver Fokaladhäsionen oder gekrümmter, kraftärmerer Adhäsionen beeinflussen kann.
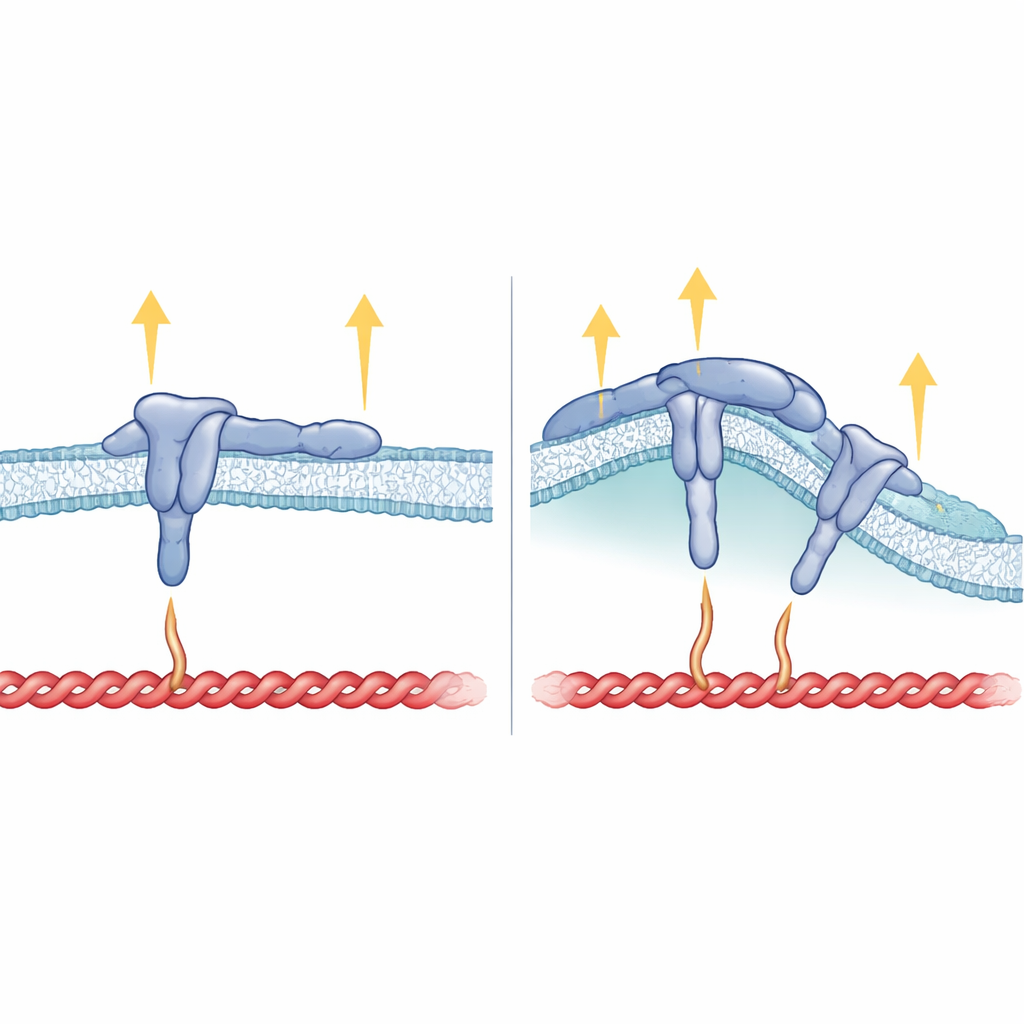
Wie Membranform, Integrinstruktur und Kraft zusammenpassen
Über den inneren Schwanz hinaus erwies sich auch der Membranteil von β5 als kritisch. Ersetzten die Forschenden das transmembrane Segment von β5 durch das von β3, konnte das resultierende Integrin zwar weiterhin Fokaladhäsionen bilden, bevorzugte aber keine gekrümmten Stellen mehr und folgte nicht mehr FCHo2. Das legt nahe, dass die Art, wie das Integrin in der Membran sitzt, das HDRRE-Motiv so ausrichtet, dass FCHo2 an gekrümmten Regionen anhaften und das ligandengebundene, aktive αvβ5 stabilisieren kann. In gekrümmten Adhäsionen scheint Talin nur einen weiter entfernten Teil des Integrinschwanzes zu berühren und trägt dort keine hohen Spannungen, was erklärt, warum andere kraftabhängige Komponenten wie Vinculin, Tensin und Kindlin dort weitgehend fehlen. Im Gegensatz dazu greift Talin in Fokaladhäsionen sowohl nahe als auch entfernte Stellen am Schwanz und an der Membran, unterstützt starke Zugkräfte und blockiert zugleich FCHo2 den Zugang zu derselben Region.
Welche Bedeutung das für das Zellverhalten hat
Für Laien ist die Botschaft dieser Arbeit, dass Zellen zwei getrennte „Greifmodi“ zur Haftung an ihrer Umgebung besitzen. Auf flachen, starren Flächen nutzen sie talingetriebene Fokaladhäsionen, die zum starken Ziehen ausgelegt sind. Auf weichen, faserigen und gekrümmten Strukturen schalten sie auf FCHo2-gesteuerte gekrümmte Adhäsionen um, die Integrin αvβ5 mit deutlich geringerer Kraft stabilisieren. Eine winzige Änderung in der Integrinsequenz — und ob diese Stelle chemisch modifiziert ist — entscheidet mit, welcher Modus verwendet wird. Dieses doppelte System erlaubt es Zellen, in dreidimensionalen Umgebungen sowohl Steifigkeit als auch Form zu interpretieren und beeinflusst, wie sie wandern, Gewebe organisieren und möglicherweise wie sie im Krankheitsfall eindringen.
Zitation: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
Schlüsselwörter: Integrine, Zelladhäsion, Membrankrümmung, FCHo2, Zytoskelett