Clear Sky Science · de
Architektonische und evolutionären Merkmale von TE-abgeleiteten TSS prägen gewebespezifische Promotoraktivität im menschlichen Genom
Versteckte Schalter in unserer DNA
Fast die Hälfte des menschlichen Genoms besteht aus mobilen DNA-Fragmenten, die lange als „Junk“ oder genetische Trittbrettfahrer abgetan wurden. Diese Studie zeigt, dass Tausende dieser Sequenzen tatsächlich als versteckte Ein-/Ausschalter fungieren und dabei helfen, Gene in bestimmten Geweben wie Gehirn, Lunge oder Hoden zu aktivieren. Zu verstehen, wie diese alten genetischen Mitreisenden als Steuerknöpfe für unsere Gene wiederverwendet werden, liefert Einsichten in die menschliche Evolution, Krankheitsmechanismen und das, was verschiedene Zelltypen einzigartig macht.
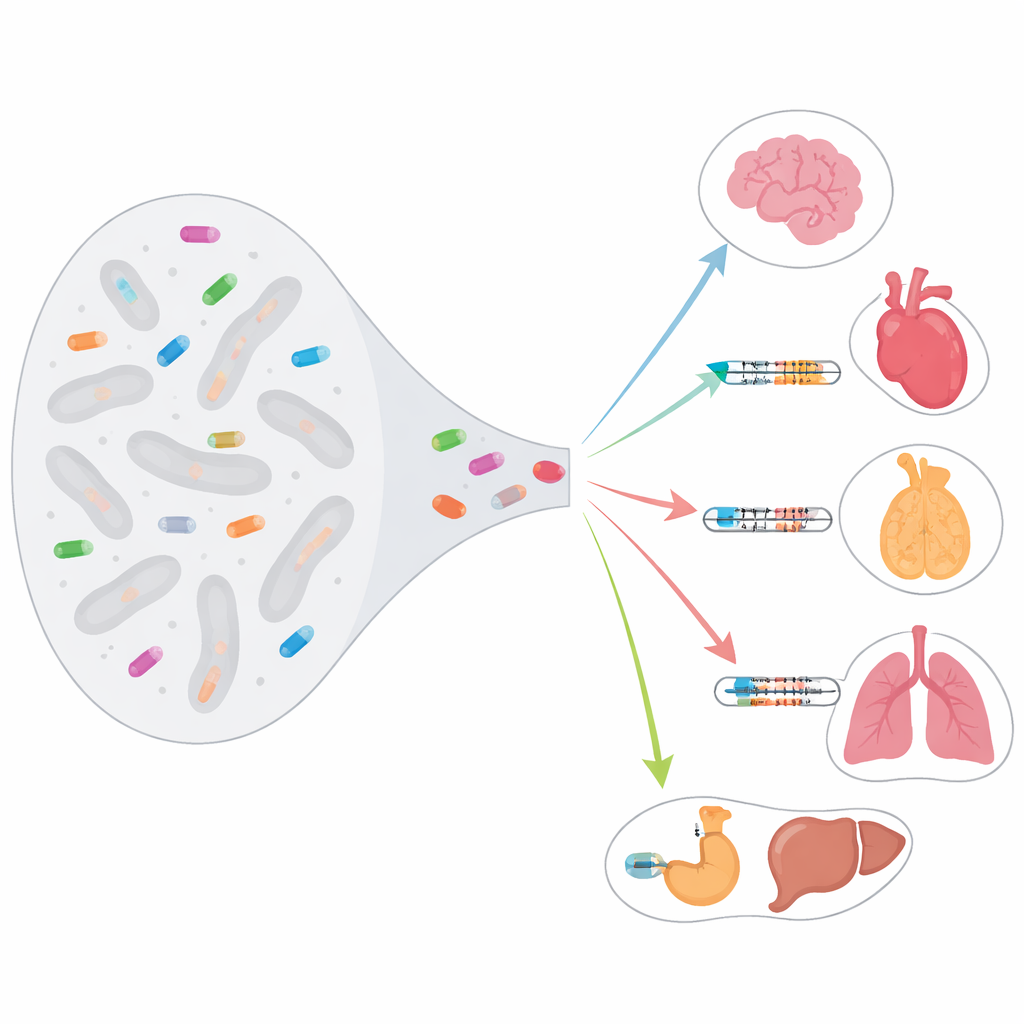
Springende Gene wurden zu Kontrollknöpfen
Transponierbare Elemente sind DNA-Abschnitte, die sich einst im Genom kopierten und an anderen Stellen einfügten. Im Laufe der Zeit wurden die meisten von der Zelle stummgeschaltet, um Schaden zu vermeiden. Dennoch wurden einige Einfügungen umgenutzt und dienen nun als Starttore für Genaktivität, sogenannte Transkriptionsstartstellen. Die Autor*innen verwendeten eine präzise Methode namens RAMPAGE, angewandt auf 115 menschliche Proben aus 87 Geweben und 28 Zelltypen, um mehr als 26.000 solcher Startstellen zu kartieren, die innerhalb transponierbarer Elemente liegen. Diese Stellen sind kein zufälliges Hintergrundrauschen: Viele sind in normale Gen-Netzwerke eingebunden und bestimmen mit, wann und wo Gene angeschaltet werden.
Gewebespezifische Schalter im ganzen Körper
Beim Vergleich der Proben quer durch den Körper fanden die Forschenden, dass transponierbare-Element-basierte Startstellen hochgradig gewebespezifisch sind. Mehr als die Hälfte taucht nur in einer einzigen Probe auf, und die Gene, die sie nutzen, werden tendenziell stark, aber nur in bestimmten Geweben exprimiert. Im Gehirn stehen diese Schalter mit Genen in Verbindung, die an Synapsen beteiligt sind; in der Lunge mit Immunabwehr; im Hoden mit Genen, die die kontraktile Maschinerie der Zelle formen; und in der Milz mit Immun- und Transportfunktionen. Bei vielen Genen sind diese Stellen keine marginalen Extras: In etwa einem Viertel der betroffenen Gene liefern sie mindestens die Hälfte der Promotoraktivität und fungieren damit effektiv als zentrales Zündpunkt für die Transkription.
Spezielles DNA-Design für präzise Kontrolle
Die Studie zeigt außerdem, dass diese Startstellen einen charakteristischen architektonischen Stil teilen. Im Vergleich zu Standardpromotoren beim Menschen bilden sie häufiger schmale Initiationsspitzen, das heißt die Transkription beginnt an einer sehr präzisen Base statt über eine breite Region verteilt zu sein. Sie sind angereichert für ein klassisches „TATA-Box“-Muster unmittelbar stromaufwärts der Startstelle und liegen tendenziell in DNA-Regionen ohne CpG-Inseln, ein Merkmal, das meist mit schalterartiger, gewebespezifischer Kontrolle assoziiert ist. Biochemische Tests bestätigen, dass viele dieser Stellen starke Genaktivität eigenständig antreiben können, besonders wenn sie als einzigartiger oder dominanter Promotor für ein Gen fungieren.
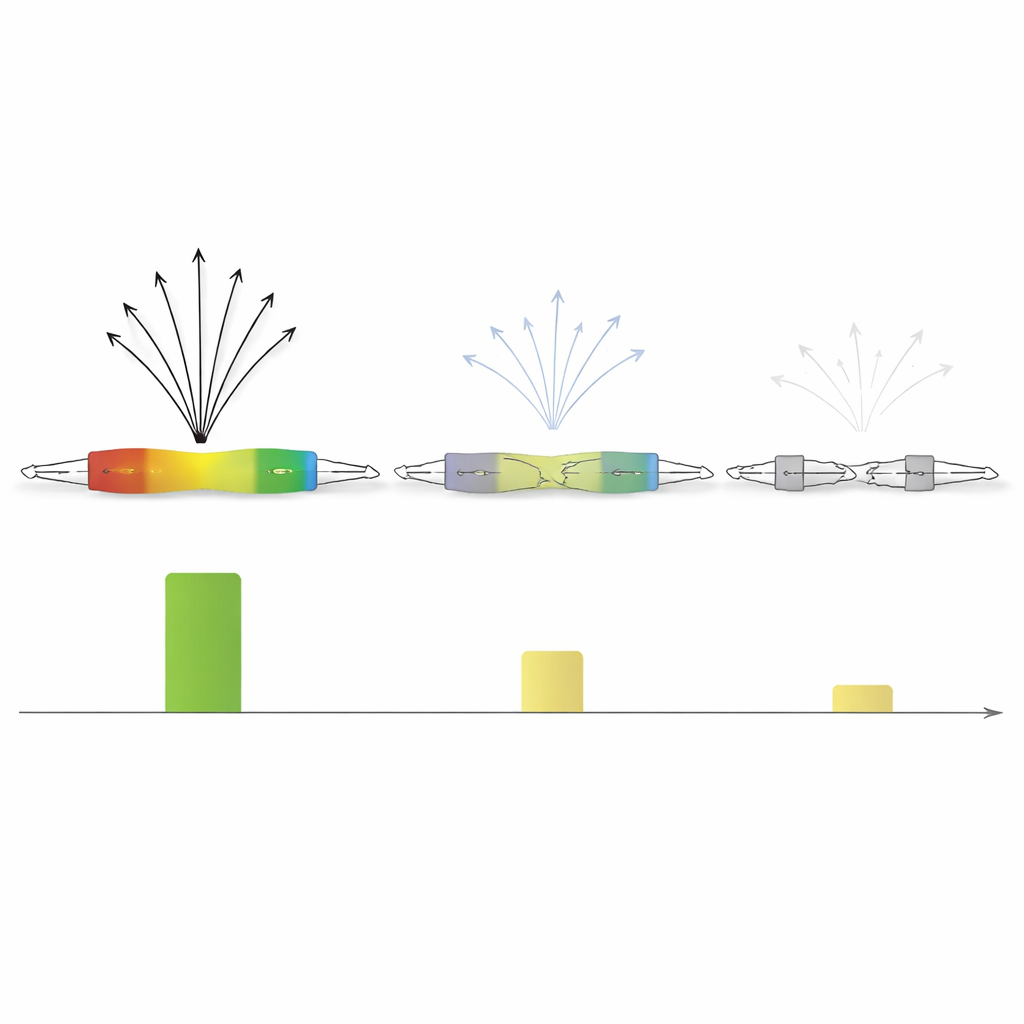
Jüngere Elemente, schärfere Schalter
Da transponierbare Elemente zu unterschiedlichen Zeiten in das Genom eingegangen sind, konnten die Autor*innen sie als eine Art evolutionäre Zeitreihe betrachten. Sie fanden, dass jüngere Familien von Elementen, besonders solche, die für Primaten und Menschenaffen einzigartig sind, oft intakte promotorähnliche Motive bewahren. Diese jüngeren Kopien zeigen starke intrinsische Aktivität und hochfokussierte Startpunkte für die Transkription. Ältere Familien hingegen akkumulieren Mutationen und strukturelle Brüche. Ihre Transkriptionsstartstellen werden schwächer und verstreuter, verlieren die scharfe Fokussierung jüngerer Gegenstücke und sind zunehmend auf den umgebenden genomischen Kontext angewiesen.
Wie mobile DNA menschliche Merkmale mitprägte
Indem die Studie gewebespezifische Genkontrolle mit Alter und Struktur mobiler DNA-Fragmenten verknüpft, legt sie nahe, dass Schübe transponierbarer Elemente ein Toolkit potenzieller Schalter hinterlassen haben, das die Evolution rekrutieren konnte. Junge, noch intakte Elemente bieten leistungsfähige, präzise Kontrollpunkte, von denen einige in Bahnen für Gehirnfunktion, Immunität, Stoffwechsel und Fortpflanzung eingespeist wurden, insbesondere bei Primaten und Hominiden. Vereinfacht ausgedrückt wurden Fragmente einst umherziehender DNA recycelt zu fein abgestimmten Schaltern, die mitbestimmen, was unsere Zellen tun, und möglicherweise zu Merkmalen beigetragen haben, die Menschen und unsere nächsten Verwandten unterscheiden.
Zitation: Zhang, Y., Fan, Y., Wu, H. et al. Architectural and evolutionary features of TE-derived TSSs shape tissue-specific promoter activity in the human genome. Nat Commun 17, 2219 (2026). https://doi.org/10.1038/s41467-026-68934-y
Schlüsselwörter: transponierbare Elemente, Genregulation, Promotoren, Gewebespezifität, menschliche Evolution