Clear Sky Science · de
Ein experimentell informierter Polymermodell enthüllt die hochauflösende Organisation genomischer Loci
Wie die DNA-Faltung die Zellidentität formt
Jede Zelle in Ihrem Körper trägt im Wesentlichen dieselbe DNA, dennoch verhalten sich Nervenzellen, Hautzellen und Stammzellen sehr unterschiedlich. Ein wesentlicher Grund ist, wie diese DNA im Zellkern gefaltet und verpackt ist. Diese Studie stellt eine neue Methode vor, diese Faltung in bemerkenswertem Detail zu «sehen» und die physische Anordnung der DNA damit in Beziehung zu setzen, ob wichtige Gene ein- oder ausgeschaltet sind. Durch die Kombination von Experimenten mit physikbasierten Computersimulationen zeigen die Autorinnen und Autoren versteckte Klumpen genetischen Materials, die offenbar als grundlegende Bausteine der Genomorganisation fungieren.
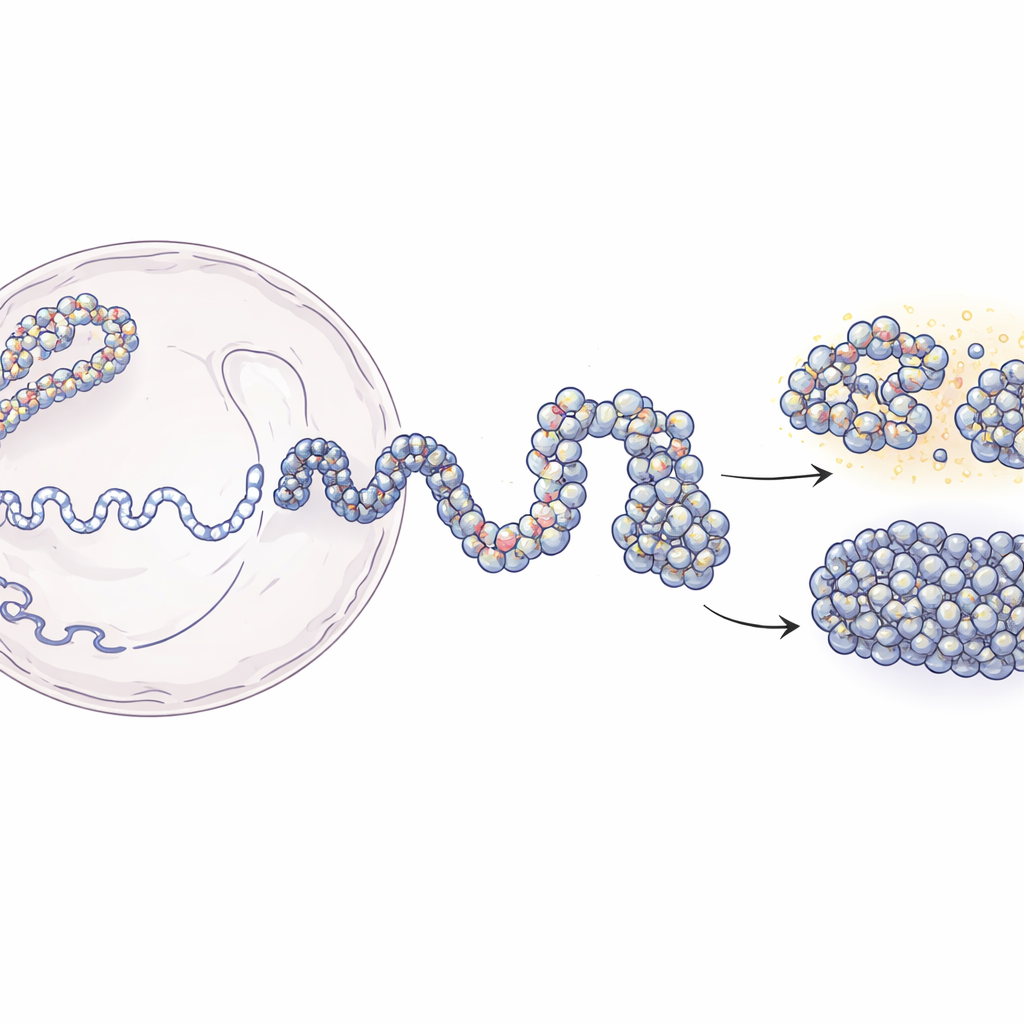
Von langen DNA-Fäden zu 3D-Genomkarten
Im Zellkern ist DNA um Proteinspulen gewickelt, die Nukleosomen genannt werden, und bildet so eine Perlen-auf-einer-Schnur-Struktur, das Chromatin. Moderne Techniken wie Hi-C und Micro-C können uns zeigen, welche DNA-Stücke im 3D-Raum nahe beieinander liegen, bieten aber meist verschwommene, populationsdurchschnittliche Momentaufnahmen. Dagegen liefern Experimente, die einzelne Nukleosomen lokalisieren, scharfe lokale Details, aber wenig Eindruck von der größeren Struktur. Diese Arbeit schließt diese Lücke. Die Autorinnen und Autoren starten mit niedrigauflösenden Kontaktkarten, die zeigen, wie oft weit entfernte DNA-Segmente in Kontakt kommen, und kombinieren diese mit experimentellen Karten der Nukleosom-Positionen. Mit Prinzipien der Polymerphysik bauen sie simulierte 3D-Ensembles des Chromatins, die die experimentellen Daten reproduzieren und gleichzeitig Strukturen bis hinunter zu wenigen Dutzend DNA-Basenpaaren auflösen.
Eine zweistufige Strategie zum Wiederaufbau des Chromatins
Der Modellierungsansatz erfolgt in zwei Hauptschritten. Zuerst verwendet das Team Hi-C-Daten, um viele mögliche großskalige Formen eines 200.000 Basenpaare langen DNA-Abschnitts zu erzeugen, wobei das Chromatin als flexibler Kettenzug behandelt wird, in dem 5.000-Basenpaare-Segmente sanft gelenkt werden, um Kontakte herzustellen oder zu vermeiden, wie sie in den Experimenten beobachtet wurden. Diese groben Strukturen erfassen das allgemeine Faltungsmuster, das durch Proteine in der Zelle mitgestaltet wird. Im zweiten Schritt wird jede große Perle durch eine wesentlich feinere Kette aus einzelnen Nukleosomen und den kurzen DNA-Verbindungsstücken zwischen ihnen ersetzt. Die Positionen dieser Nukleosomen stammen aus einer enzymbasierten Kartierungsmethode (MNase-seq), die aufzeigt, wo sie typischerweise entlang des Genoms sitzen. Die fein aufgelösten Ketten dürfen sich dann falten, während sie weiterhin die übergeordnete Architektur respektieren. Wenn die Forschenden ihre hochauflösenden Modelle wieder auf die experimentellen Auflösungen „verwischen“, reproduzieren sie sowohl Hi-C- als auch Micro-C-Kontaktkarten mit hoher Genauigkeit.
Entdeckung von Nukleosom-Blobs als Struktureinheiten
Beim Hineinzoomen in ihre simulierten Strukturen zeigte sich ein auffälliges Muster: Nukleosomen waren nicht gleichmäßig verteilt, sondern sammelten sich in unregelmäßigen Clustern, die die Autorinnen und Autoren Nukleosom-Blobs nennen. Diese Blobs ähneln den klumpigen Strukturen, die zuvor in Superauflösungsmikroskopie-Aufnahmen realer Zellen beobachtet wurden. Durch die Analyse von vielen Tausenden simulierten Schnappschüssen zeigte das Team, dass diese Blobs eher länglich als kugelförmig sind und typischerweise mehrere eng gepackte Nukleosomen enthalten. Entscheidend ist, dass Kontakte innerhalb dieser Blobs eng mit den domänenähnlichen Interaktionsblöcken in experimentellen Daten übereinstimmen, was darauf hindeutet, dass Blobs keine zufälligen Artefakte, sondern fundamentale 3D-Einheiten der Chromatinorganisation sind. Die Simulationen sagen sogar zusätzliche subtile Domängrenzen voraus, die experimentell schwer zu erkennen sind, und legen nahe, dass dieses physikalische Modell feinkörnige Merkmale in verrauschten Daten aufdecken kann.
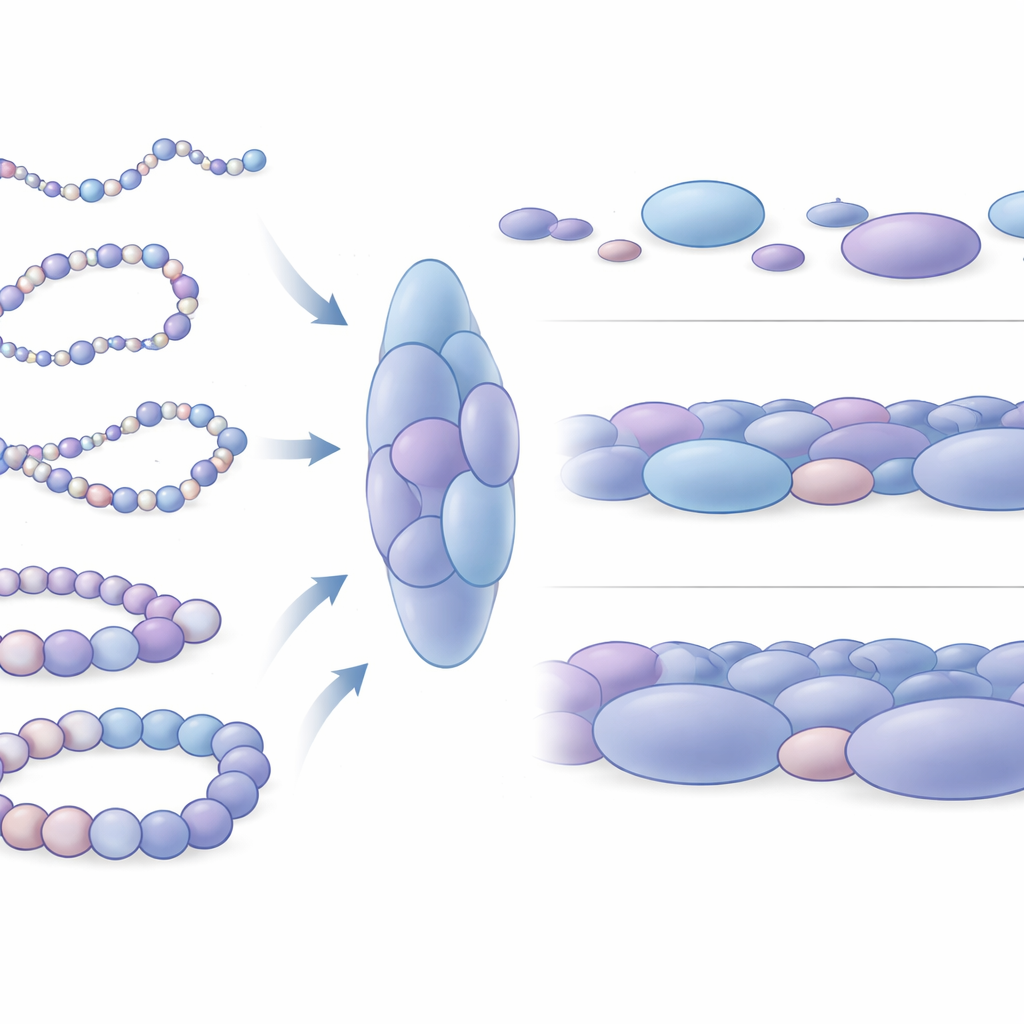
Wie Packungsunterschiede Genaktivität widerspiegeln
Die Forschenden untersuchten dann, wie sich diese Blobs um aktive versus stille Gene unterscheiden. Sie konzentrierten sich auf vier gut untersuchte Abschnitte menschlicher DNA, darunter zwei Gene, die Stammzellen in einem flexiblen, undifferenzierten Zustand halten (Nanog und Lin28A), und zwei Entwicklungsregulationsgene (HoxB4 und HoxA13), die in denselben Zellen abgeschaltet sind. Um die inaktiven Gene herum waren die Blobs im Mittel größer und dichter gepackt, wobei die Nukleosomen vollständigere geschlossene lokale Anordnungen bildeten. Im Gegensatz dazu waren Blobs in der Nähe aktiver Gene kleiner, etwas lockerer und variabler. Auf größerer Skala durchprobte die DNA um aktive Gene viele mehr verschiedene Formen und war mechanisch biegsamer, während die Regionen um stille Gene sich wie steifere Chromatinsegmente verhielten. Dieser mechanische Unterschied beeinflusst vermutlich, wie leicht entfernte regulatorische DNA-Elemente aufeinandertreffen und mit Genumschaltern zusammenwirken können.
Warum das für das Verständnis der Genkontrolle wichtig ist
Zusammengefasst zeichnen die Ergebnisse ein Bild, in dem das Genom aus dynamischen Nukleosom-Clustern aufgebaut ist, deren Größe, Form und Abstand mitbestimmen, ob nahegelegene Gene zugänglich oder verschlossen sind. Das neue Modell verknüpft experimentelle Kontaktdaten, Nukleosomkarten und physikalische Prinzipien zu einem einzigen Rahmen, der erklärt, wie Stammzellgene flexibel und interaktiv bleiben können, während Entwicklungsgene in steiferen, kompakteren Nachbarschaften abgeschirmt sind. Für Nichtfachleute ist die Kernidee, dass Genaktivität nicht nur von der DNA-Sequenz abhängt; sie ist auch davon bestimmt, wie diese DNA in dreidimensionale Strukturen gefaltet ist. Indem es Nukleosom-Blobs als grundlegende Bausteine dieser Faltung offenlegt, bietet diese Arbeit einen wirkungsvollen Weg, mikroskopische Genomarchitektur mit großmaßstäblichen Prozessen wie Entwicklung, Zellidentität und Krankheit zu verbinden.
Zitation: Mittal, R., Heermann, D.W. & Bhattacherjee, A. An experimentally-informed polymer model reveals high resolution organization of genomic loci. Nat Commun 17, 2338 (2026). https://doi.org/10.1038/s41467-026-68928-w
Schlüsselwörter: Chromatin-Faltung, Nukleosom-Cluster, 3D-Genomorganisation, Genregulation, Polymermodellierung