Clear Sky Science · de
Nitroreduktase‑ausgelöste Indazol‑Bildung
Einfache Zutaten in wertvolle Medikamente verwandeln
Viele moderne Arzneimittel basieren auf einer Handvoll verbreiteter molekularer »Gerüste«, die gut an biologische Ziele binden. Eines dieser Gerüste, das Indazol, kommt in Wirkstoffen gegen Krebs und bei schwerer Übelkeit zum Einsatz. Bisher erforderte die Herstellung von Indazolen oft aggressive Chemikalien, hohe Temperaturen und Metalle, die umweltschädlich sind. Diese Studie zeigt, wie Wissenschaftler natürliche Enzyme dazu bringen können, Indazole schonend in Wasser zu bilden und so den Weg für umweltfreundlichere Produktionsweisen wichtiger Arzneistoffe zu ebnen.
Warum diese ringförmigen Moleküle wichtig sind
Arzneimitteldesigner verwenden häufig bestimmte ringförmige Strukturen, weil sie zuverlässig mit Proteinen im Körper interagieren. Indazole sind eine solche beliebte Struktur und finden sich in zugelassenen Medikamenten gegen Krebs und chemotherapy‑induzierte Übelkeit. Chemiker kennen bereits mehrere Syntheserouten zu Indazolen, doch die Standardverfahren beruhen auf reaktiven Bausteinen, starken Basen oder Säuren und Metallkatalysatoren wie Kupfer und Palladium. Diese Methoden funktionieren zwar, erzeugen aber Abfall, verbrauchen Energie und bergen Sicherheitsrisiken – ein Widerspruch zum wachsenden Bestreben nach nachhaltiger Herstellung in der Pharmaindustrie.
Enzyme als sanfte Bauarbeiter
Anstatt Atome mit Hitze und starken Reagenzien zusammenzuzwingen, nutzen die Autoren die Biokatalyse – also Enzyme, die als natürliche Katalysatoren Reaktionen in Wasser bei Raumtemperatur ermöglichen. Ihr Fokus liegt auf sogenannten Nitroreduktasen, die normalerweise Zellen dabei helfen, nitrohaltige Verbindungen schrittweise zu entgiften. Das Team argumentierte, dass ein bestimmtes Zwischenprodukt in diesem Reduktionsweg, wenn es im richtigen Moment freigesetzt wird, sich spontan falten und das charakteristische Indazol‑Ringsystem bilden könnte. Mit zwei verschiedenen Nitroreduktasen demonstrieren sie, dass einfache 2‑Nitrobenzylamine als Ausgangsstoffe unter milden, wässrigen Bedingungen effizient in Indazole umgewandelt werden – oft mit über 99 % Umsatz.
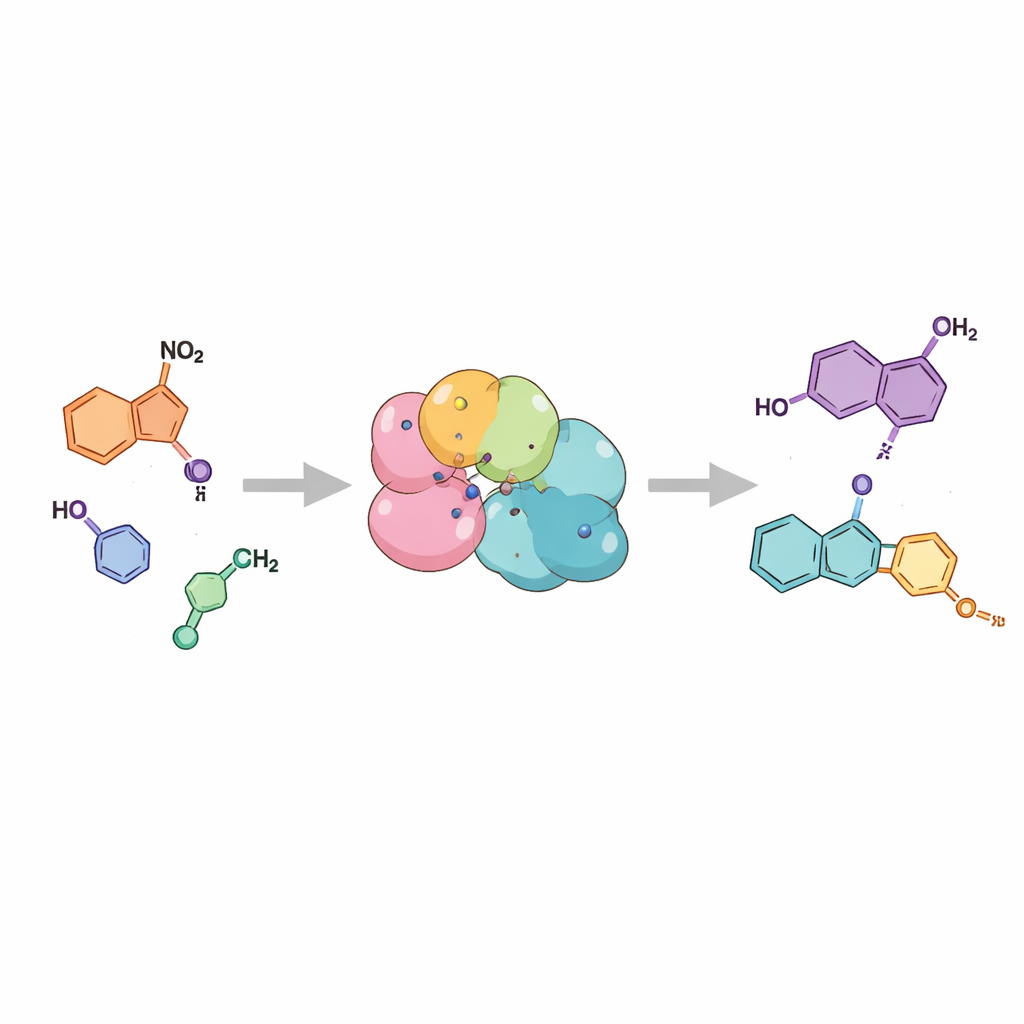
Aufzeigen der Reaktionsbreite der Enzyme
Um zu prüfen, wie allgemein die Strategie anwendbar ist, fütterten die Forschenden die Enzyme mit einer Reihe verwandter Ausgangsmaterialien, die verschiedene Seiten‑ und Positionssubstituenten am aromatischen Ring trugen. Sie fanden heraus, dass beide Enzyme eine große Bandbreite an chemischen Varianten tolerierten – von kleinen Gruppen wie Methyl bis hin zu größeren Ringsystemen und unterschiedlichen Chlor‑, Brom‑ und Methoxy‑Substituenten. In vielen Fällen liefen die Reaktionen sauber zum gewünschten Indazol ab, mit isolierten Ausbeuten, die praktisch nutzbar sind. Die Art der Substitution am Ausgangsstoff bestimmte zudem, welche von zwei eng verwandten Indazol‑Formen entstand – ein wichtiges Merkmal, da beide Formen in der Arzneimittelentwicklung relevant sein können. Das Prinzip ließ sich sogar auf einen größeren Indazol‑Verwandten, die Cinnoline, ausdehnen und unterstreicht so die Vielseitigkeit des Ansatzes.
Aufbau einer zweistufigen enzymatischen Fertigungsstraße
Die Indazole in dieser Arbeit stammen nicht direkt aus spezialisierten Startmaterialien; stattdessen bauten die Autoren eine kurze enzymatische Fertigungsstraße aus preiswerten Bausteinen auf. Im ersten Schritt verbindet eine andere Enzymklasse, eine Imine‑Reduktase, ein einfaches Aldehyd mit einem Amin, um das benötigte 2‑Nitrobenzylamin zu erzeugen. Im zweiten Schritt wandelt die Nitroreduktase dieses Zwischenprodukt in den Indazolring um. Durch sorgfältiges Abstimmen der Enzymmengen und des Cofaktor‑Recyclings führten die Autoren diese zwei‑Enzym‑Kaskade im präparativen Maßstab durch, ausgehend von 50 Milligramm Aldehyd in Wasser. Sie erhielten mehrere Indazolprodukte in guten Gesamtausbeuten, darunter Beispiele mit verschiedenen Seitenketten, die sich später weiter für die Wirkstoffforschung modifizieren lassen.
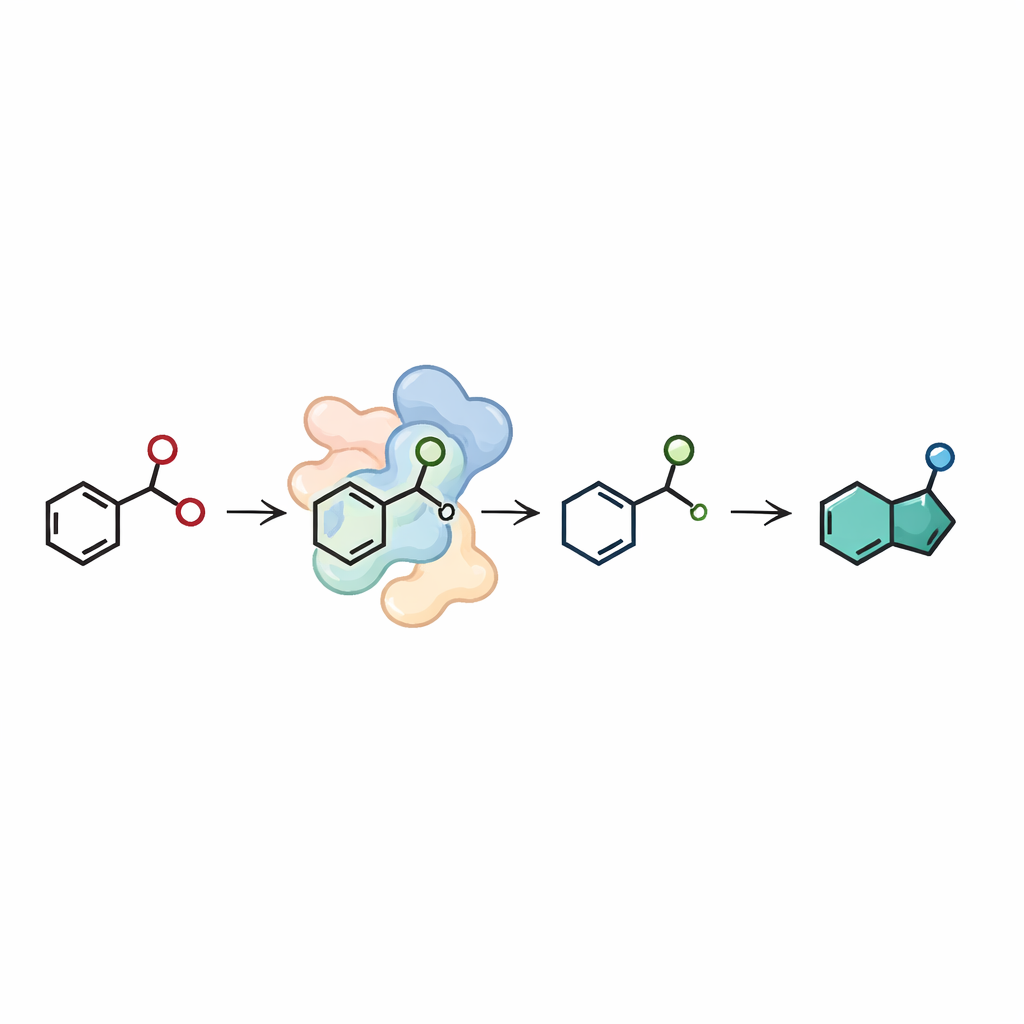
Ein sauberer Weg zu komplexen Bausteinen für Medikamente
Für nicht‑Fachleute lautet die Kernaussage: Die Forschenden haben natürliche Katalysatoren so eingesetzt, dass ein medizinisch wichtiges Ringsystem auf eine Weise zusammengesetzt wird, die sowohl für Menschen als auch für die Umwelt schonender ist. Ihr enzymbasierter Weg vermeidet gefährliche Stickstoff‑Stickstoff‑Reagenzien und edle Metallkatalysatoren, arbeitet in Wasser bei moderaten Temperaturen und lässt sich mit anderen Enzymen zu einer effizienten Mini‑Fabrik kombinieren. Diese Arbeit erweitert das Werkzeug‑Repertoire der Chemiker um eine leistungsfähige, nachhaltige Methode und bringt die umweltfreundliche Herstellung einen Schritt näher, während sie der Pharmawelt vielseitige Indazol‑Bausteine für zukünftige Medikamente liefert.
Zitation: Terholsen, H., Medema, L., Chernyshova, E. et al. Nitroreductase-triggered indazole formation. Nat Commun 17, 2261 (2026). https://doi.org/10.1038/s41467-026-68926-y
Schlüsselwörter: Biokatalyse, Indazol‑Synthese, Nitroreduktase, grüne Chemie, Enzymkaskaden