Clear Sky Science · de
Klonale Expansion zytotoxischer CD8⁺-T‑Zellen bei lecanemab‑assoziierter ARIA
Warum das für Menschen mit Alzheimer wichtig ist
Lecanemab ist eines der ersten Medikamente, die Amyloid aus dem Gehirn entfernen und den Gedächtnisverlust bei Alzheimer‑Krankheit mäßig verlangsamen können. Einige Patientinnen und Patienten unter dieser Therapie entwickeln jedoch Hirnschwellungen oder kleine Blutungen, Veränderungen, die in MRT‑Aufnahmen sichtbar sind und unter dem Begriff amyloid‑bezogene Bildgebungsanomalien (ARIA) zusammengefasst werden. Diese Studie stellt eine entscheidende Frage für Patienten und Familien: Was passiert im Immunsystem, wenn ARIA auftritt, und könnte eines Tages ein einfacher Bluttest helfen vorherzusagen, wer am stärksten gefährdet ist?
Versprechen und Risiko einer neuen Alzheimer‑Behandlung
Lecanemab ist ein per Infusion verabreiteter Antikörper, der sich gegen Ablagerungen des Proteins Amyloid‑beta richtet, ein Kennzeichen der Alzheimer‑Krankheit. Indem es dem Körper hilft, Amyloid zu entfernen, kann es den kognitiven Abbau mäßig verlangsamen. Dieser Nutzen geht jedoch mit einem Sicherheitsproblem einher: Manche Menschen entwickeln ARIA, das Bereiche mit Hirnschwellungen oder punktförmige Blutungen einschließen kann. Diese Nebenwirkungen erfordern häufige MRT‑Kontrollen und können einschränken, wer das Medikament erhält. Nicht alle sind gleich anfällig—Träger einer Genvariante namens APOE4 haben ein höheres Risiko—aber Gene allein erklären nicht, warum ARIA auftritt, insbesondere früh nach Therapiebeginn. Da lecanemab über den Blutkreislauf verabreicht wird, vermuteten die Autoren, dass eine genaue Untersuchung der Immunzellen im Blut frühe Warnzeichen oder sogar Mechanismen offenbaren könnte, die die Behandlung mit vaskulären Schäden im Gehirn verknüpfen. 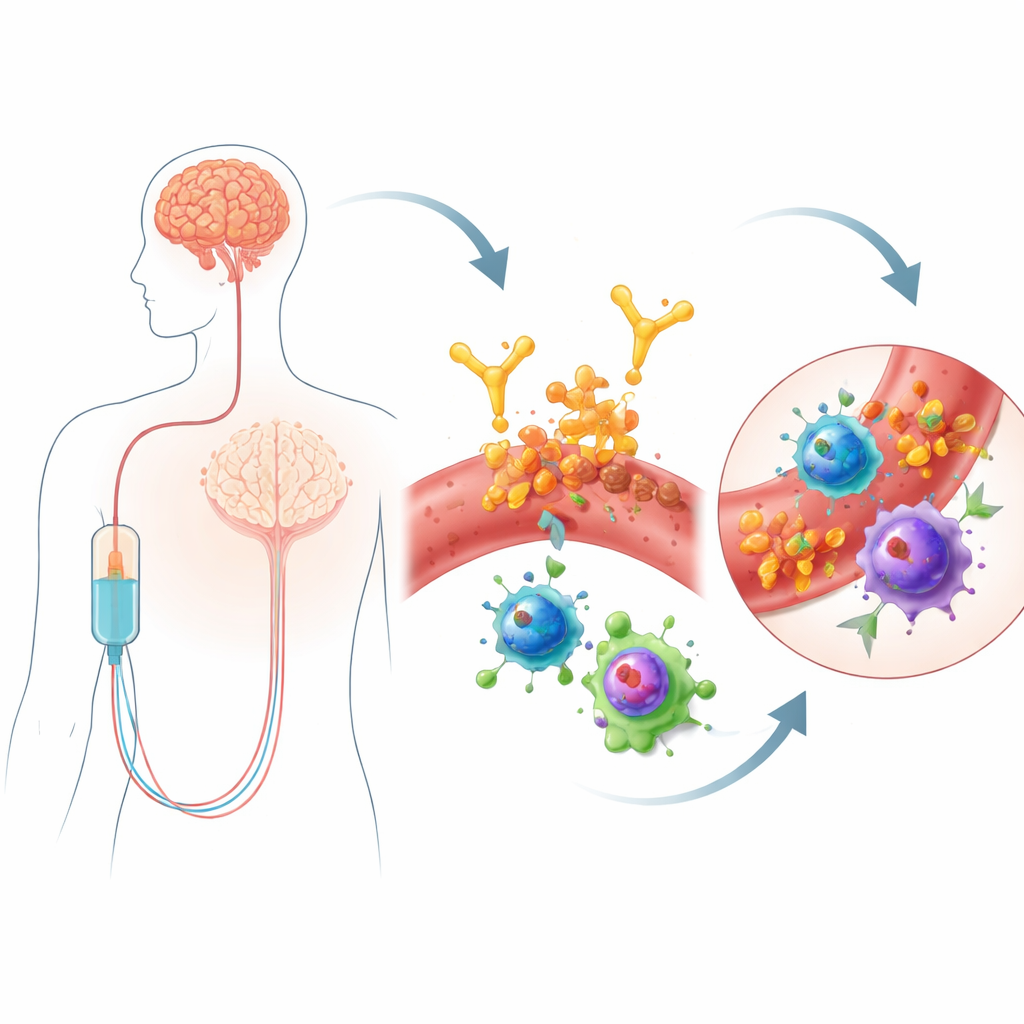
Verfolgung von Immunzellen bei Patienten mit und ohne ARIA
Die Forscher untersuchten sechs Menschen mit Alzheimer, die in einer regionalen Gedächtnisklinik mit lecanemab behandelt wurden. Drei entwickelten verschiedene Formen von ARIA, drei vergleichbare Patienten (ähnlich in Alter, Geschlecht, APOE‑Genotyp und Anzahl der Infusionen) taten dies nicht. Blut wurde unmittelbar vor den Infusionen entnommen, und das Team verwendete einen intensiven „multi‑omischen“ Ansatz: Einzelzell‑RNA‑Sequenzierung, um zu erfassen, welche Gene in Tausenden einzelner Immunzellen aktiviert waren; antikörperbasierte Markertags zur Definition von Zelltypen; Sequenzierung der T‑Zell‑Rezeptoren zur Verfolgung von Klonen; sowie zielgerichtetes Metabolomik‑Screening zur Messung hunderter kleiner Moleküle des Zellstoffwechsels. So konnten sie nicht nur feststellen, welche Zelltypen vorhanden waren, sondern auch, wie aktiv sie waren, welche Energiequellen sie nutzten und ob bestimmte T‑Zell‑Familien als Reaktion auf einen Auslöser expandierten.
Expansion hochgerüsteter Killer‑T‑Zellen
Bei den Patienten, die ARIA entwickelten, zeigte sich ein klares Muster. Im Vergleich zu Kontrollen hatten sie einen höheren Anteil an CD8‑„Killer“‑T‑Zellen und weniger CD4‑Helferzellen. Innerhalb des CD8‑Pools hoben sich zwei Subgruppen hervor: Effektormemory‑Zellen und eine terminal differenzierte Form, bekannt als TEMRA‑Zellen. Diese TEMRA‑Zellen sind wie erfahrene Soldaten—stark spezialisiert auf Angriff, mit ausgeprägter Ausrüstung zur Abtötung von Zielzellen. Bei ARIA‑positiven Patienten waren TEMRA‑Zellen zahlreicher, stärker klonal expandiert (das heißt, bestimmte T‑Zell‑Familien hatten sich vervielfacht) und trugen Genprogramme, die mit Zytotoxizität, Migration durch Blutgefäße und Zeichen chronischer Stimulation assoziiert sind. Ähnliche T‑Zell‑Zustände wurden beim Altern, bei chronischen Infektionen, Multipler Sklerose und in der Rückenmarksflüssigkeit von Menschen mit Alzheimer beobachtet, wo sie sich in der Nähe von Blutgefäßen und an der Gehirnoberfläche anreichern können.
Stoffwechselumbau und Wechselwirkung mit anderen Immunzellen
Das Team fand außerdem, dass diese CD8‑Effektor‑Zellen ihren Stoffwechsel umgestellt hatten. Anstatt hauptsächlich auf effiziente Energieproduktion in Mitochondrien zu setzen, verlagerte sich ihr Stoffwechsel hin zur Glykolyse, einem schnelleren, aber weniger effizienten Weg der Energiegewinnung, der kurzlebige, hochintensive Aktivität unterstützt. Metabolitmessungen in Blutzellen bestätigten dies: Lactat‑ und Pyruvatspiegel waren erhöht, während Schlüsselkomponenten des Zitronensäurezyklus reduziert waren—ein Muster, das typisch für entzündliche Immunzellen ist. Monozyten, eine andere Art von weißen Blutkörperchen, zeigten komplementäre Veränderungen. Bei ARIA‑positiven Patienten schalteten Monozyten Gene für Antigenpräsentation, Adhäsion an andere Zellen und Produktion von Chemokinen an—chemische Signale, die T‑Zellen anziehen. Computerbasierte Modellierung von Ligand‑Rezeptor‑Paaren deutete darauf hin, dass Monozyten stärkere aktivierende und Homing‑Signale an CD8‑Effektorzellen sendeten und so ein Umfeld schufen, das diese Killerzellen ermutigt, sich an Gefäßwände anzulagern.
Adresscodes, die T‑Zellen zu Gehirngefäßen lotsen
Da diese Studie nur Blutproben untersuchte, griffen die Autoren auf einen unabhängigen Einzelzell‑Datensatz aus Gehirnen von lecanemab‑behandelten Patienten zurück, um zu prüfen, ob dieselben T‑Zell‑Programme mit vaskulären Nischen im Gehirn verknüpft sind. Als sie ihre CD8‑Subsets auf diese Gehirnkarte projizierten, zeigten die TEMRA‑ und Effektormemory‑Zellen aus ARIA‑positiven Patienten transkriptionelle „Adresscodes“—Kombinationen von Adhäsionsmolekülen und Chemokinrezeptoren—die zu Endothelzellen (Blutgefäßzellen) im erkrankten Gehirn passten. Diese Signaturen legen nahe, dass die expandierten Killer‑T‑Zellen nicht nur hochgerüstet und metabolisch aktiviert sind, sondern auch darauf vorbereitet, zu stressbelasteten Gehirnblutgefäßen zu homing‑und mit ihnen zu interagieren, gerade an Stellen der Amyloidbeseitigung. 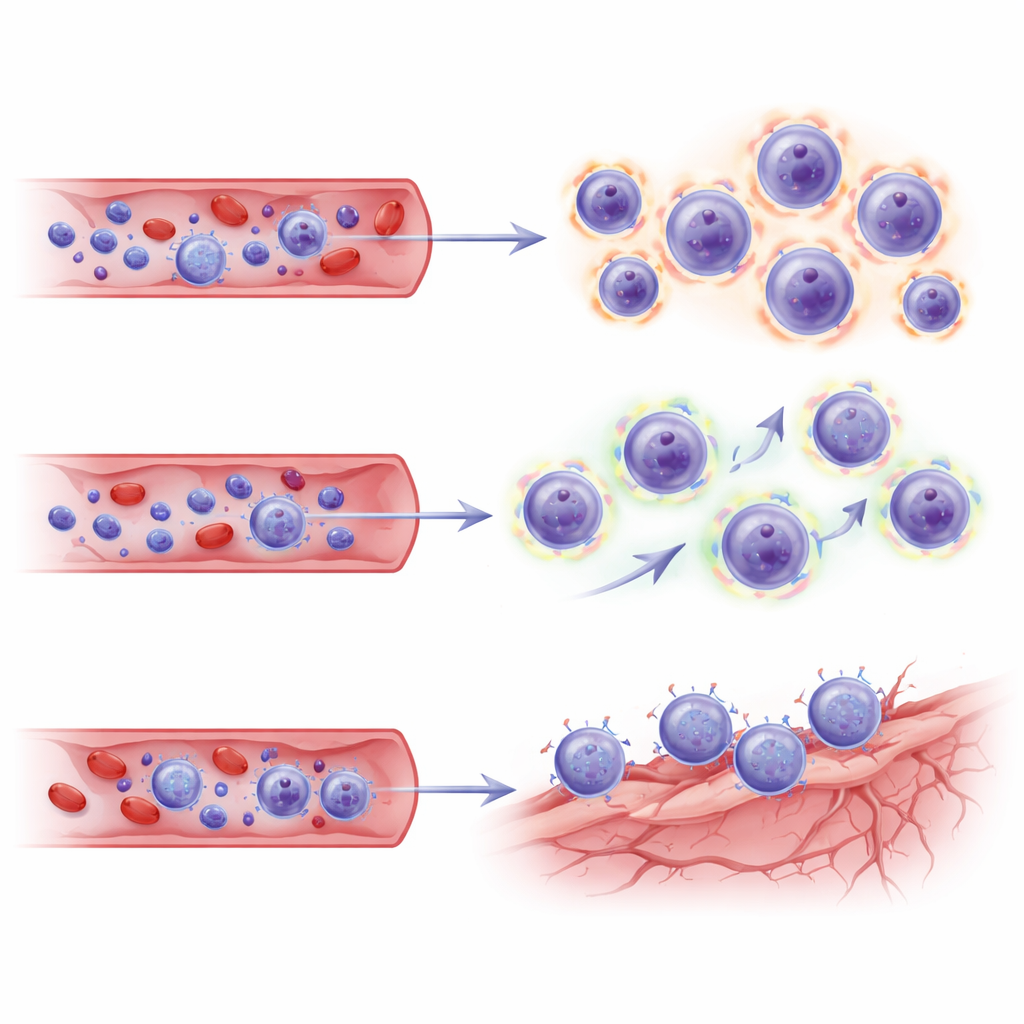
Was das für Patienten und die künftige Versorgung bedeuten könnte
Insgesamt zeichnet diese kleine, aber detaillierte Studie das Bild von ARIA als mehr als nur eine passive Nebenwirkung der Amyloidentfernung. Vielmehr scheint es mit einer koordinierten Immunantwort im Blut verbunden zu sein: Expansion und metabolische Aktivierung spezifischer Killer‑T‑Zellklone, verstärkte Signale von Monozyten und molekulare Merkmale, die die Interaktion mit Gehirnblutgefäßen begünstigen. Die Arbeit beweist nicht, dass diese Zellen ARIA verursachen—Immunveränderungen könnten auch eine Reaktion auf vaskuläre Verletzungen und nicht deren Ursache sein—aber sie liefert testbare Hypothesen und einen Fahrplan für blutbasierte Biomarker. Zukünftig könnte die Messung der Häufigkeit und des metabolischen Zustands von CD8 TEMRA‑Zellen zusammen mit Schlüssel‑Signalmolekülen helfen, Patienten mit erhöhtem ARIA‑Risiko zu identifizieren, Überwachungsintervalle zu steuern oder sogar gezielte Strategien zu entwickeln, diese Immunantwort vorübergehend abzudämpfen, ohne die Vorteile amyloidklärender Therapien zu verlieren.
Zitation: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
Schlüsselwörter: Alzheimer‑Krankheit, lecanemab, Immunzellen, Gehirnblutgefäße, Nebenwirkungen der Behandlung