Clear Sky Science · de
Molekulare Signaturen der Resilienz gegenüber Alzheimer-Krankheit in Neokortex-Layer-4-Neuronen
Warum manche Gehirnzellen Alzheimer schlagen
Die Alzheimer-Krankheit ist dafür bekannt, Erinnerung und Denkvermögen zu rauben, doch der Schaden verteilt sich nicht gleichmäßig im Gehirn. Manche Nervenzellen sterben früh, während andere selbst in fortgeschrittener Erkrankung überraschend gesund bleiben. Diese Studie stellt eine hoffnungsvolle Frage: Was macht diese robusteren Zellen anders, und lassen sich ihre Überlebensstrategien in neue Therapien übersetzen?
Die Geschichte von drei Hirnregionen
Die Forscher konzentrierten sich auf drei Bereiche des menschlichen Kortex: zwei, die früh von Alzheimer betroffen sind (präfrontaler Kortex und Precuneus, wichtig für Planung und Gedächtnis), und einen, der spät betroffen ist (der primäre visuelle Kortex, der das Sehen verarbeitet). Mit mehr als 400.000 isolierten Zellkernen aus 46 gespendeten Gehirnen bestimmten sie, welche Gene in einzelnen Zellen aktiv sind (single-nucleus RNA-Sequenzierung) und kartierten anschließend, wo diese Zellen in Gewebeschnitten liegen (räumliche Transkriptomik). Diese Kombination erlaubte ihnen, nicht nur die Zelltypen zu identifizieren, sondern genau zu sehen, wo verletzliche und resiliente Zellen innerhalb der geschichteten Struktur des Kortex sitzen.
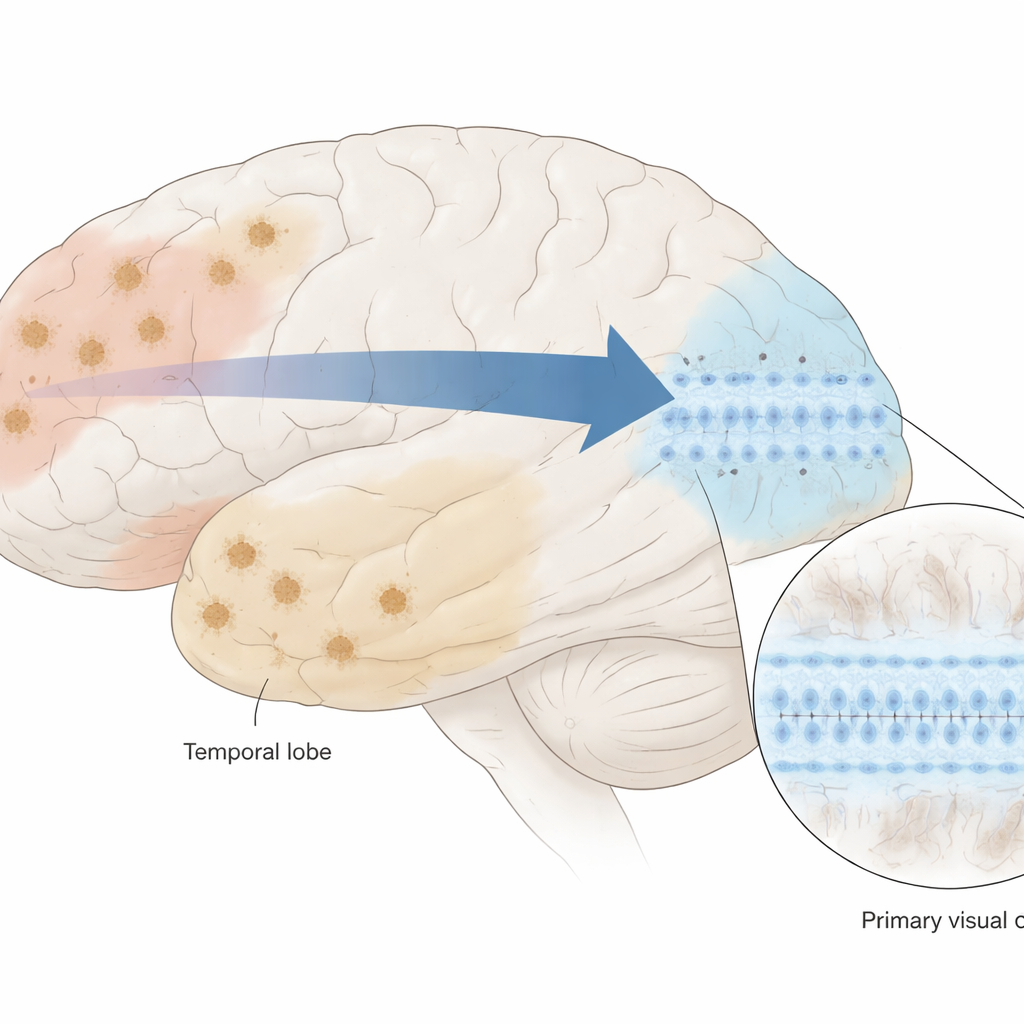
Die verborgene Stärke der Layer-4-Neuronen
Im visuellen Kortex fokussierten sie sich auf Layer 4, einen dichten Streifen kleiner Neuronen, die eintreffende sensorische Signale empfangen. Diese Schicht ist schon lange als relativ verschont bei Alzheimer beobachtet worden, selbst wenn klebrige Amyloid-Plaques vorhanden sind. Das Team entdeckte eine spezifische Gruppe exzitatorischer Neuronen in Layer 4 — in ihrer Analyse Ex5 genannt — die im primären visuellen Kortex besonders häufig vorkommt, aber auch in anderen kortikalen Regionen, wenn auch sparsamer, vertreten ist. Mit fortschreitender Alzheimer-Pathologie nahmen viele andere Neuronentypen ab, doch diese Ex5-Zellen hielten stand und machten sogar einen größeren Anteil der verbliebenen Neuronen aus, ein starkes Zeichen zellulärer Resilienz.
Früh aktivierte schützende Genprogramme
Um zu verstehen, warum Ex5-Neuronen überdauern, verglichen die Wissenschaftler die Genaktivität dieser resilienten Zellen mit der ihrer anfälligeren Nachbarn, insbesondere einer verwundbaren Gruppe oberflächlicher Schichtneuronen, die an Denken und Gedächtnis beteiligt sind. Über Krankheitsstadien und Hirnregionen hinweg schalteten Ex5-Neuronen Sets von Genen ein, die mit dem Erhalt von Synapsen, der Feinabstimmung elektrischer Signale und der strikten Regulation von intrazellulärem Kalzium verbunden sind. Viele dieser Gene sind bereits aus genetischen Studien bekannt und beeinflussen das Alzheimer-Risiko. Das Muster legt nahe, dass resiliente Neuronen früh in der Erkrankung aktiv ein Schutzprogramm hochfahren, anstatt einfach zufällig Schaden zu vermeiden.
Ein Partner-Kaliumkanal im Rampenlicht
Ein Gen, KCNIP4, hob sich als besonders starker Kandidat für die Treiberrolle der Resilienz hervor. Es kodiert ein Protein, das an Kaliumkanäle von Neuronen bindet und hilft zu kontrollieren, wie leicht sie feuern. In menschlichen Hirnproben stiegen die KCNIP4-Spiegel gezielt in resilienten Layer-4-Neuronen mit zunehmender Alzheimer-Pathologie, während sie in anfälligeren Neuronentypen später in der Erkrankung abnahmen. Das Team prüfte dann seine Wirkung direkt: Mit einem viralen Vektor steigerten sie die Mausvariante dieses Gens (Kcnip4) in kultivierten Mauskorticalneuronen und in einem Mausmodell, das genetisch so verändert wurde, dass es Alzheimer-ähnliche Veränderungen entwickelt. In Zellkulturen zeigten Neuronen mit zusätzlichem Kcnip4 weniger Kalziumburst-Aktivität, selbst wenn sie toxischen Amyloidfragmenten ausgesetzt wurden. In Mäusen dämpfte die Überexpression von Kcnip4 Marker neuronaler Überaktivität im Kortex, ohne die Amyloid-Akkumulation zu verschlechtern und mit einer moderaten Reduktion entzündlicher Mikroglia.
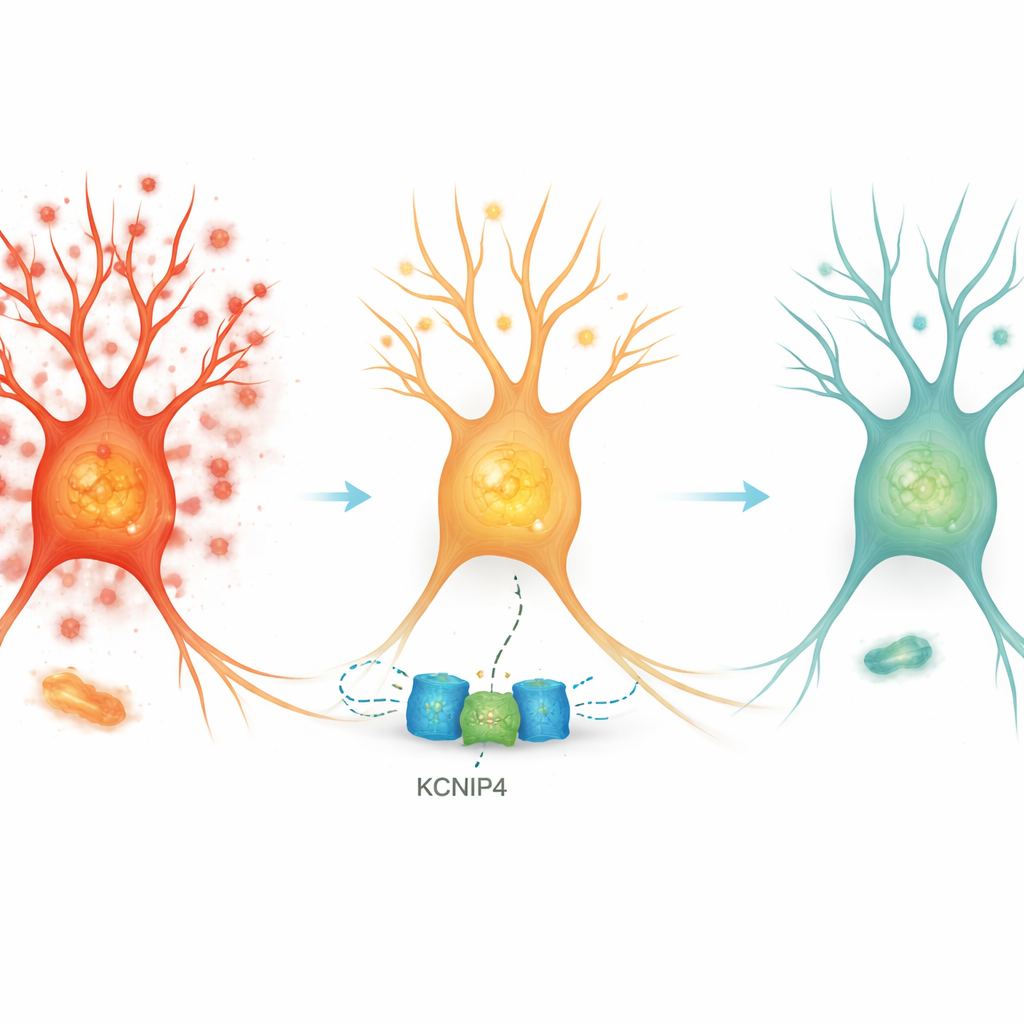
Von resilienten Zellen zu künftigen Therapien
In der Summe zeichnen die Befunde ein Bild, in dem bestimmte Neuronen des visuellen Kortex Alzheimer überleben, indem sie ein schützendes Netzwerk von Genen hochfahren, das ihre Verbindungen stabil hält und ihre elektrische Aktivität in Schach hält. KCNIP4 steht im Zentrum dieses Netzwerks und wirkt wie eine eingebaute Bremse auf hyperaktive Neuronen — ein Zustand, der zunehmend als früher Treiber von Schäden bei Alzheimer und anderen Hirnerkrankungen anerkannt wird. Zwar bleibt noch viel Arbeit, bis sich diese Einsichten in Therapien übersetzen lassen, doch die Studie liefert eine detaillierte Karte resilienter kortikaler Zelltypen und der molekularen Werkzeuge, mit denen sie überleben. Dieselben Werkzeuge — insbesondere Wege, die neuronale Erregbarkeit sicher feinzujustieren — könnten eines Tages darin helfen, verletzlichere Hirnregionen vor den Verwüstungen von Alzheimer zu schützen.
Zitation: Dharshini, S.A.P., Sanz-Ros, J., Pan, J. et al. Molecular signatures of resilience to Alzheimer’s disease in neocortical layer 4 neurons. Nat Commun 17, 2223 (2026). https://doi.org/10.1038/s41467-026-68920-4
Schlüsselwörter: Resilienz gegenüber Alzheimer-Krankheit, kortikale Layer-4-Neuronen, Einzelzell-Transkriptomik, neurale Hyperexzitabilität, KCNIP4