Clear Sky Science · de
TMEM63-Proteine wirken als mechanisch aktivierte, cholesterolmodulierte Lipid-Scramblasen und tragen zur mechano-Resilienz der Membran bei
Wie Zellen unter physikalischer Belastung intakt bleiben
Die Zellen unseres Körpers werden ständig gequetscht, gedehnt und gestoßen, sei es in schlagenden Herzen, arbeitenden Muskeln oder Tumoren, die sich durch Gewebe drücken. Diese Studie enthüllt, wie eine Familie von Membranproteinen, genannt OSCA/TMEM63, Zellen dabei hilft, solch harten mechanischen Kräften zu überstehen, indem sie die Fette in ihrer äußeren Hülle umverteilen. Das Verständnis dieses eingebauten Stoßdämpfersystems könnte neue Einblicke in Erkrankungen des Hörens, der Nervenmyelinisierung und sogar der Krebsmetastasierung liefern.
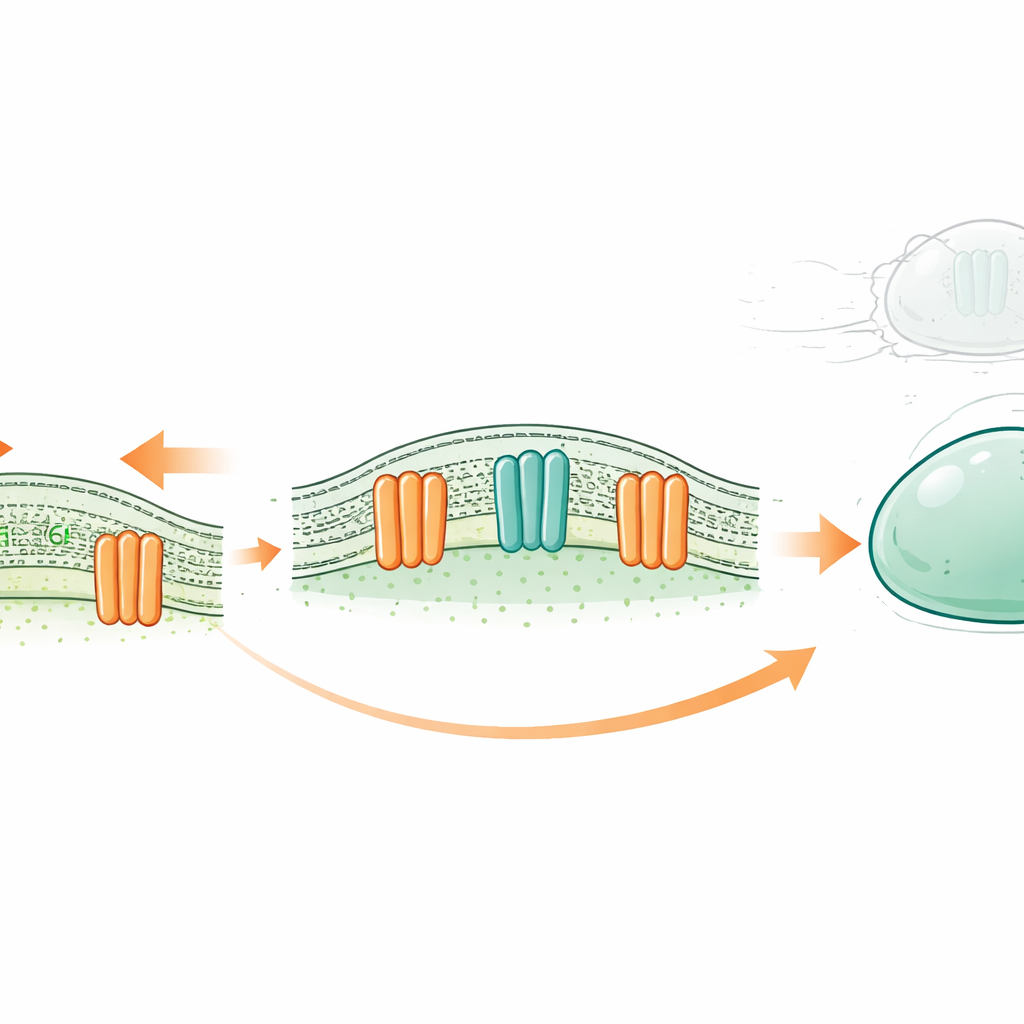
Eine neue Art zellulärer Stoßdämpfer
Jede Zelle ist von einer dünnen, ölig wirkenden Membran umgeben, die aus zwei Schichten fettähnlicher Moleküle besteht, sogenannten Lipiden. Traditionell galten bestimmte Membranproteine als reine Ionenkanäle—winzige Ventile, die geladene Teilchen als Reaktion auf Reize wie Dehnung hinein- und hinauslassen. Die OSCA/TMEM63-Familie, die von Pflanzen bis zum Menschen vorkommt, ist dafür bekannt, sich als Reaktion auf Membranspannung zu öffnen. Frühere Strukturarbeiten deuteten darauf hin, dass ihre Poren sich zum Teil aus Lipiden zusammensetzen. Das warf die provokante Frage auf: Könnten diese Kanäle auch als „Scramblasen“ wirken und Lipide zwischen der inneren und äußeren Schicht der Membran umdrehen, wenn die Zelle unter Kraft steht?
Beobachtung des Lipidflips durch die Membran
Um diese Idee zu testen, kombinierten die Autoren Computersimulationen mit reduktionistischen Laborsystemen, die aus gereinigten Komponenten aufgebaut wurden. In Simulationen wurden offene Versionen mehrerer OSCA- und TMEM63-Proteine in Modellsysteme der Membran eingebettet. Lipidmoleküle bewegten sich spontan durch eine Rinne in diesen Proteinen von einer Seite der Doppelschicht zur anderen und bildeten einen Gurt, der die beiden Blätter verband, während ein mit Wasser gefüllter Pfad für Ionen frei blieb. Parallel dazu bauten die Forscher riesige künstliche „Bläschen“ (Vesikel) mit fluoreszierenden Lipiden und spezifischen Proteinen. Wenn ein äußerer Wirkstoff die Fluoreszenz an der Außenseite löschte, konnte ein weiterer Signalabfall nur dadurch erklärt werden, dass Lipide von der inneren Lage nach außen flippten. Vesikel mit OSCA1.1, OSCA1.2, OSCA2.2 oder TMEM63A/B zeigten diesen zusätzlichen Fluoreszenzverlust, was aktives Scrambling anzeigte, während Kontrollkanäle, die keine Lipide scramblen, dies nicht taten.
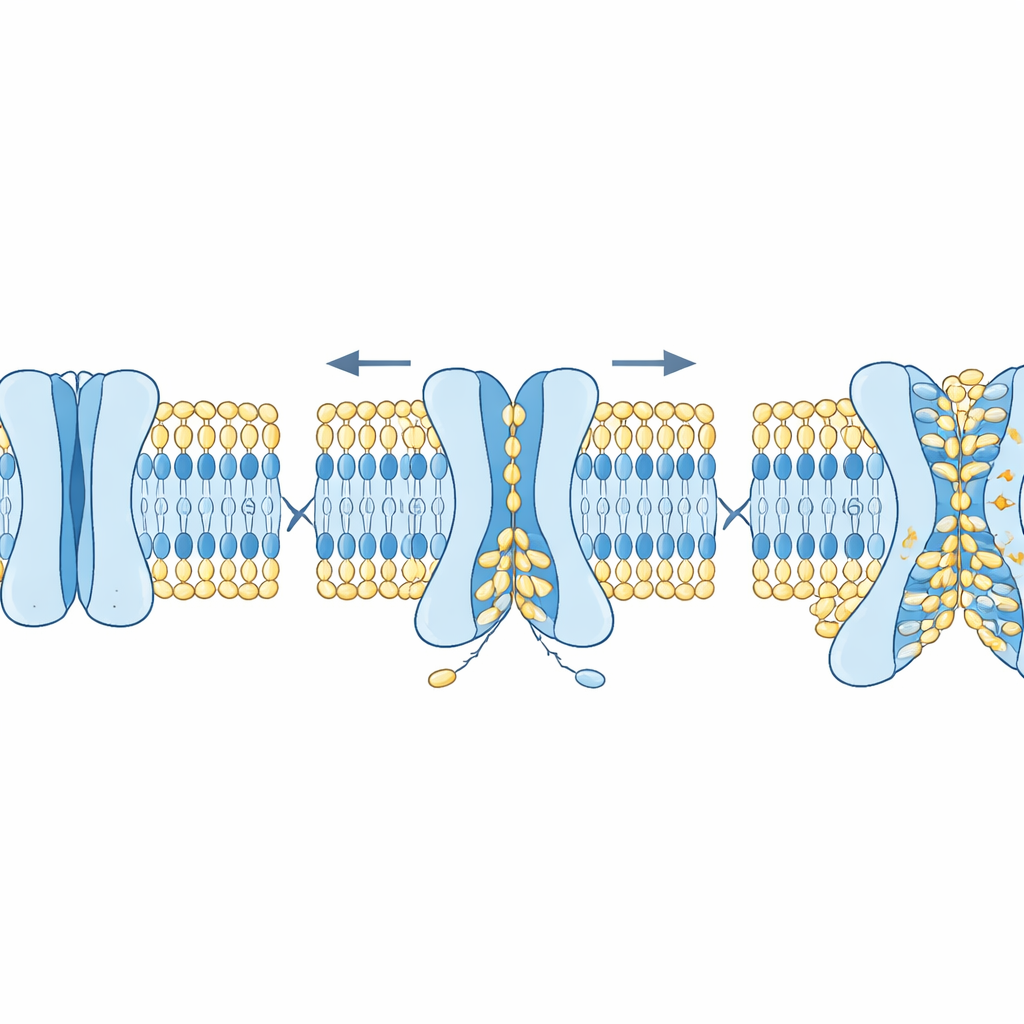
Wie Struktur und Cholesterin den Prozess abstimmen
Die Forscher fragten dann, welche Merkmale der TMEM63-Proteine dieses doppelte Verhalten steuern. Mit AlphaFold2 erzeugten sie viele plausible Formen menschlicher TMEM63-Proteine, von geschlossen bis zunehmend offen. Simulationen zeigten, dass einige wenige voluminöse Aminosäuren als „Flaschenhälse“ in der Rinne fungieren. Ein Rest begrenzt hauptsächlich den Ionenfluss, während andere die Lipidbewegung blockieren. Eine Mutation des Ionen-Flaschenhalses erhöhte die elektrische Leitfähigkeit, ohne das Lipid-Scrambling stark zu verändern, während eine Mutation des Lipidtors dazu führte, dass Lipide leichter flippten und sogar Zellen ohne weiteren Reiz „Fress-mich“-Signale auf ihrer Oberfläche zeigten. Ein weiterer wichtiger Regulator war Cholesterin, ein versteifender Bestandteil von Zellmembranen. Die Zugabe von Cholesterin zu Modellmembranen verlangsamte das Lipid-Scrambling deutlich und stabilisierte den geschlossenen Zustand von TMEM63A—sowohl in Simulationen als auch in Kryo-Elektronenmikroskopiestrukturen, in denen Cholesterin an spezifische Stellen des Proteins geschmiegt lag.
Mechanische Kraft als Einschaltmechanismus
Wenn Cholesterin das Scrambling in Zellen normalerweise dämpft, was schaltet es dann im richtigen Moment an? Das Team nutzte ringförmige Zuckermoleküle, Cyclodextrine genannt, um selektiv Lipide aus Membranen zu ziehen und so die Spannung zu erhöhen, ohne Cholesterin zu entfernen. In zellgroßen Vesikeln aktivierte die Zugabe von Cyclodextrin das Lipid-Scrambling durch TMEM63A nur in Anwesenheit des Proteins und bewies damit, dass allein mechanischer Stress das Umdrehen auslösen kann. Ähnliche Ansätze in lebenden Zellen zeigten, dass eine milde Entfernung von Cholesterin allein nicht ausreichte; eine anschließende mechanische Herausforderung war erforderlich, um starkes Scrambling zu beobachten. Wenn Zellen, die für die Expression von TMEM63A konstruiert wurden, wiederholt gedehnt wurden, zeigten sie rasch bestimmte Lipide auf ihrer Außenseite—ein Kennzeichen des Scramblings—während Zellen ohne diese Proteine deutlich weniger Veränderung zeigten.
Schutz der Zellen vor dem Aufreißen
Über das Umdrehen von Lipiden hinaus veränderte mechanisch aktiviertes Scrambling das physikalische Verhalten der Membranen unter extremen Stressbedingungen. In künstlichen Vesikeln unter hoher Kraft neigten jene ohne Scramblase zum Platzen, während Vesikel mit TMEM63A oder einer bekannten Scramblase schrumpften, dünne Tubuli bildeten und größtenteils intakt blieben. In einer menschlichen Hirnkrebs-Zelllinie, die natürlich TMEM63A und TMEM63B exprimiert, führte die Reduktion eines der beiden Proteine dazu, dass Zellen bei starker mechanischer Beanspruchung eher aufrissen. Zusammen stützen diese Befunde ein Modell, in dem OSCA/TMEM63-Proteine als Ventile wirken, die sich unter Spannung öffnen und vorübergehend die übliche Unterscheidung zwischen der inneren und äußeren Membranfläche verwischen. Indem sie Lipiden erlauben, sich schnell umzuverteilen, helfen sie, die Belastung auszugleichen und katastrophales Zerreißen zu verhindern.
Was das für Gesundheit und Krankheit bedeutet
Einfach gesagt zeigt diese Arbeit, dass einige dehnungsempfindliche Kanäle mehr tun als elektrische Signale zu leiten: Sie reorganisieren auch die äußere Haut der Zelle, um deren Überleben bei Quetschung zu unterstützen. TMEM63-Proteine treten als mechanisch aktivierte Lipid-Scramblasen hervor, deren Aktivität fein durch die Membranzusammensetzung, insbesondere Cholesterin, abgestimmt wird. Dieser Mechanismus der mechano-Resilienz könnte überall dort wichtig sein, wo Zellen großen Kräften ausgesetzt sind—von isolierenden Nervenfasern und schallwahrnehmenden Zellen im Ohr bis hin zu Krebszellen, die sich durch dichtes Gewebe bewegen. Das Verständnis und die mögliche gezielte Beeinflussung dieser doppelten Funktion als Ionenkanal und Scramblase könnten neue Wege eröffnen, schutzbedürftige Gewebe zu schützen oder umgekehrt schwer zu vernichtende Krebszellen empfindlicher zu machen.
Zitation: Lin, Y., Zhou, Z., Han, Y. et al. TMEM63 proteins act as mechanically activated cholesterol modulated lipid scramblases contributing to membrane mechano-resilience. Nat Commun 17, 2717 (2026). https://doi.org/10.1038/s41467-026-68919-x
Schlüsselwörter: mechanosensitive Ionenkanäle, Lipidscrambling, Zellmembran-Mechanik, Cholesterinregulation, TMEM63 OSCA-Proteine