Clear Sky Science · de
Ein neurotoxisches kryptisches Peptid, das durch TDP-43‑abhängiges kryptisches Spleißen von PKN1 entsteht
Verborgene Gefahren innerhalb von Gehirnzellen
Viele Erkrankungen des Gehirns, darunter die amyotrophe Lateralsklerose (ALS) und die Alzheimer‑Krankheit, sind mit Ablagerungen eines Proteins namens TDP-43 verbunden. Forschende wissen, dass Nervenzellen ohne korrekt funktionierendes TDP-43 wichtige Botschaften verlieren und schließlich zugrunde gehen. Diese Studie zeigt eine überraschendere Wendung: Das Versagen von TDP-43 kann Gehirnzellen auch dazu bringen, ein bisher unbekanntes, toxisches Mini‑Protein herzustellen, das wiederum Gedächtnisnetzwerke schädigt. Das Verständnis dieses verborgenen Akteurs könnte neue Wege für Diagnose und Behandlung verheerender Demenzen eröffnen.
Wie ein zellulärer Korrekturleser die RNA in Schach hält
Innerhalb von Neuronen wirkt TDP-43 wie ein Korrekturleser für RNA, die Zwischenbotschaften zwischen DNA und Proteinen. Es bindet an bestimmte kurze Sequenzen und blockiert das Einfügen von fehlplatzierten „Extra‑Stücken“ in diese Botschaften. Wenn TDP-43 verloren geht oder fehl lokalisiert ist, wie bei ALS und vielen Alzheimer‑Fällen, können diese Extra‑Stücke — sogenannte kryptische Exons — in die RNA hineingleiten. Bisher führten die meisten bekannten kryptischen Exons vor allem dazu, dass normales Protein verloren ging, weil die Botschaft instabil wurde und rasch abgebaut wurde. Ob solche Ereignisse auch neue, schädliche Proteine erzeugen könnten, war unklar.
Ein kryptisches Spleißereignis erzeugt ein toxisches Fragment
Die Autor*innen konzentrierten sich auf ein Gen namens PKN1, das hilft, das innere Gerüst und den Signalfluss von Neuronen zu erhalten. In Zellmodellen mit reduziertem TDP-43 entdeckten sie ein zuvor unbekanntes kryptisches Exon, PKN1‑5a1 genannt, das zwischen zwei normalen Segmenten der PKN1‑RNA eingefügt wird. Diese Einfügung führt zu einem frühen Stoppsignal und erzeugt eine verkürzte RNA. Bemerkenswerterweise entkommt ein Teil dieser fehlerhaften Botschaft der Qualitätskontrolle der Zelle und wird in ein stabiles Fragment des PKN1‑Proteins übersetzt, das nur die ersten 207 Aminosäuren enthält. Das Team nannte dieses verkürzte Produkt PKN207. Sie zeigten, dass TDP-43 diesen Fehler normalerweise verhindert, indem es an mehrere UG‑reiche Regionen grenzt, die das kryptische Exon umgeben; geht diese Bindung verloren, wird das Exon eingearbeitet und PKN207 produziert.
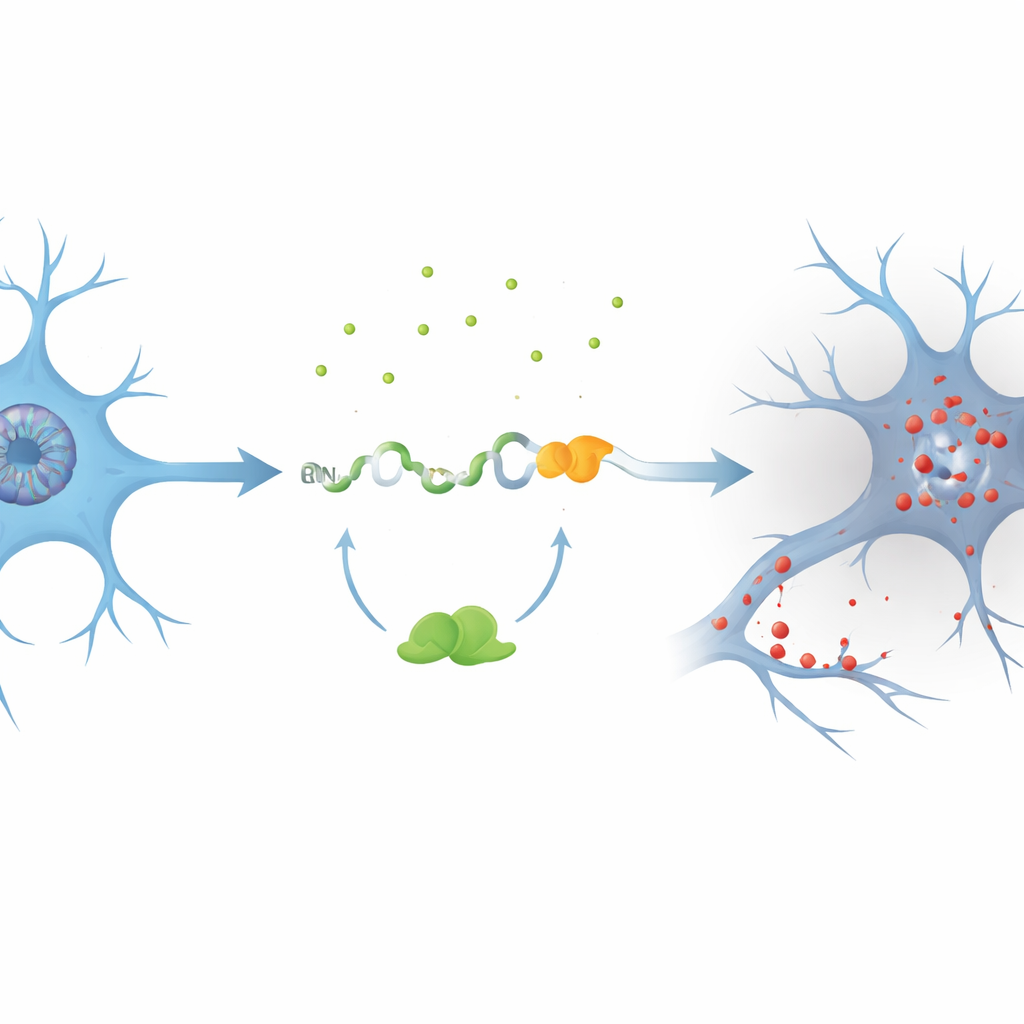
Hinweise aus Patientenhirnen und großen Datensätzen
Um zu prüfen, ob dieses Ereignis beim Menschen vorkommt, durchforsteten die Forschenden RNA‑Sequenzierungsdaten von Hunderten von ALS‑Gehirn‑ und Rückenmarksproben. Sie fanden eine weit verbreitete Aktivierung des PKN1‑5a1‑kryptischen Exons in Regionen, die für TDP-43‑Pathologie bekannt sind, wie dem Motorkortex und dem Rückenmark, jedoch nicht im relativ verschonten Kleinhirn. Dann erzeugten sie hochspezifische Antikörper, die nur den einzigartigen Schwanz von PKN207 erkennen, nicht aber das volllängige PKN1‑Protein. In hippocampalen Geweben von Alzheimer‑Patient*innen, die ebenfalls abnorme phosphorylierte TDP-43‑Befunde zeigten, detektieren diese Antikörper ein deutliches Band, das PKN207 entspricht, während ein solches Band in Kontrollgehirnen fehlte. Weitere Alzheimer‑Datensätze bestätigten, dass das kryptische Exon bereits in frühen Krankheitsstadien aktiviert ist, was darauf hindeutet, dass dieser molekulare Fehler lange vor dem Auftreten klinischer Symptome beginnen könnte.
Ein Mini‑Protein mit großem Einfluss auf das Gedächtnis
Der Nachweis von PKN207 im erkrankten menschlichen Gehirn warf die zentrale Frage auf: Ist es schädlich? Um das zu testen, nutzte das Team Viren, um entweder das normale PKN1 oder PKN207 gezielt im Hippocampus — einer für das Gedächtnis zentralen Gehirnregion — junger Mäuse zu exprimieren. Monate später zeigten beide Mäusegruppen Beeinträchtigungen beim Lernen im Morris‑Wassermaze: Sie schwammen länger, um eine verborgene Plattform zu finden. Ihr Gehirn‑Rückenmarks‑Flüssigkeit enthielt erhöhte Mengen eines Strukturproteins, Neurofilament Light Chain, ein Marker für Axonschäden. In kultivierten Neuronen löste eine erhöhte PKN207‑Expression Zellschädigung aus, gemessen als Austritt eines Enzyms, das Membranschäden anzeigt. Eine detaillierte Proteinanalyse des Hippocampus zeigte umfassende Veränderungen in Signalwegen, die mit synaptischer Stärke (Langzeitpotenzierung) und bekannten neurodegenerativen Erkrankungen verknüpft sind, mit besonders starker Störung von Molekülen, die effiziente Signalübertragung und ein gesundes Nervenfasergerüst unterstützen.
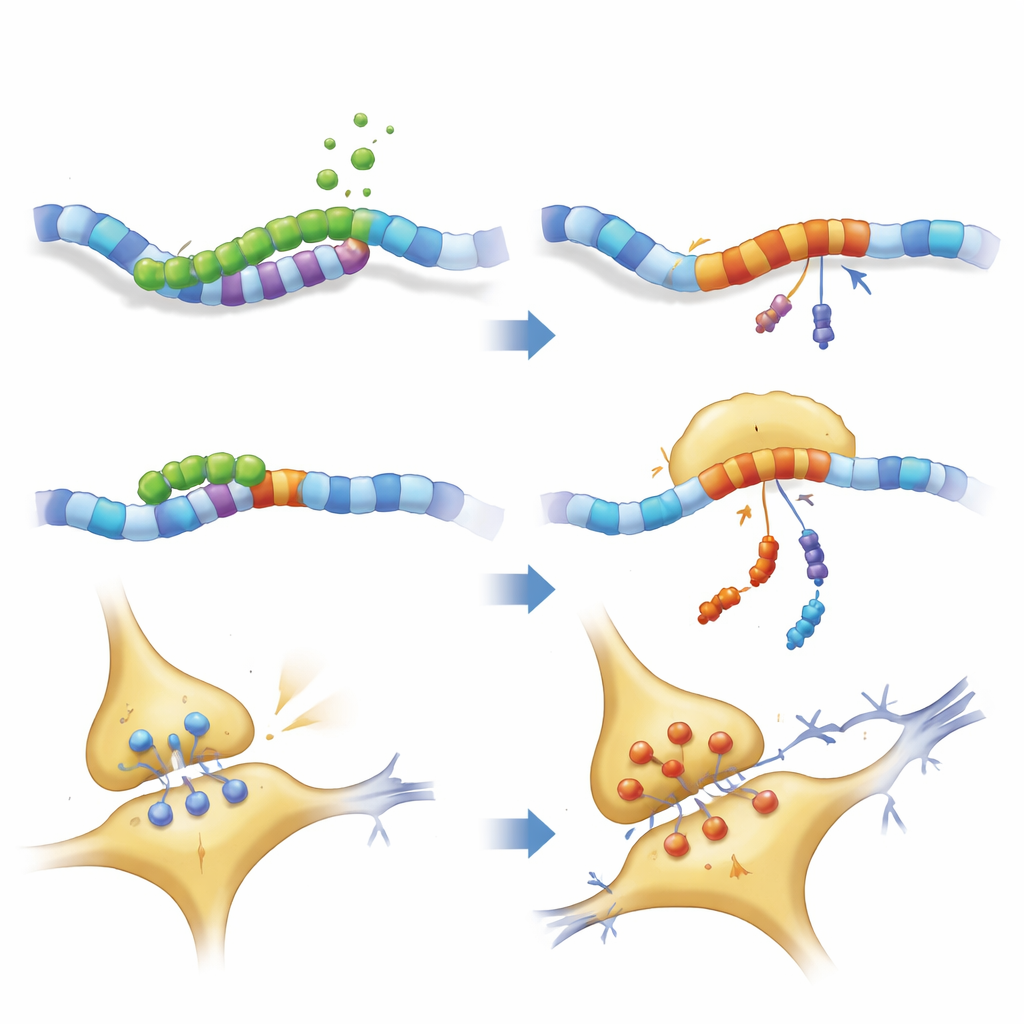
Wie das Fragment die Gehirnverdrahtung stört
Eine genauere Untersuchung der neuronalen Struktur zeigte, dass sowohl das volllängige PKN1 als auch PKN207 das Neurofilamentnetzwerk störten, das Axone in Form hält und beim Transport von Fracht hilft. Wichtige Motor‑ und Gerüstproteine waren reduziert, während einige Neurofilamentkomponenten sich anhäuften, was auf Staus im Transport und mögliche Aggregationen hindeutet. Elektrische Messungen an Hippocampus‑Schnitten bestätigten, dass Mäuse mit PKN207‑Expression eine abgeschwächte Langzeitpotenzierung aufwiesen — den Prozess, durch den Synapsen nach wiederholter Aktivität stärker werden und der als zelluläre Grundlage von Lernen und Gedächtnis gilt. Obwohl PKN207 die enzymatische Domäne von PKN1 nicht enthält, reichte seine Anwesenheit aus, um die störenden Effekte des Vollproteins nachzuahmen und in manchen Fällen zu übertreffen, was darauf hindeutet, dass die gemeinsame N‑terminale Region allein die neuronale Homöostase beeinträchtigen kann.
Warum diese Entdeckung für Hirnerkrankungen wichtig ist
Diese Arbeit fügt unserer Auffassung von TDP-43‑bezogenen Erkrankungen eine neue Ebene hinzu. Anstatt nur zum Verlust essenzieller RNAs zu führen, kann das Versagen von TDP-43 auch ein stabiles, toxisches Mikro‑Protein hervorbringen, das Synapsen und kognitive Funktionen untergräbt. Das kryptische PKN1‑5a1‑Exon und sein Peptidprodukt PKN207 heben sich nun als potenzielle Biomarker früher TDP-43‑Dysfunktion sowie als Kandidaten für Therapien hervor, die das Spleißen korrigieren oder das schädliche Fragment blockieren. Breiter betrachtet legt die Studie nahe, dass auch andere verborgene Exons möglicherweise krankheitsverursachende Peptide erzeugen und Forschende auf eine bislang übersehene Landschaft molekularer Täter in der Neurodegeneration lenken.
Zitation: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
Schlüsselwörter: TDP-43, kryptisches Spleißen, PKN1, Neurodegeneration, Alzheimer und ALS