Clear Sky Science · de
Entgegenwirkende FOX‑Proteine steuern epigenetisch das Gleichgewicht zwischen lytischem und latentem Zustand von Herpesviren
Warum verborgene Herpesviren wichtig sind
Viele Menschen tragen Herpes-simplex-Viren ein Leben lang in sich, oft ohne es zu wissen. Diese Viren können jahrelang ruhig in Nervenzellen verweilen und dann plötzlich aufflammen und Fieberbläschen, Augenerkrankungen oder bei immungeschwächten Personen schwerwiegendere Probleme verursachen. Was das Virus meist schlafen hält und was es wieder aktiviert, ist seit Langem rätselhaft. Diese Studie enthüllt einen wichtigen Teil dieses Kontrollsystems: ein Tauziehen zwischen zwei gegensätzlichen Gruppen menschlicher Proteine, die virale DNA umgestalten und darüber entscheiden, ob Herpes stumm bleibt oder neue Viren produziert.
Zwei zelluläre Teams ziehen in entgegengesetzte Richtungen
Die Autorinnen und Autoren konzentrierten sich auf eine große Familie menschlicher DNA‑bindender Proteine, die FOX‑Proteine, die normalerweise unsere eigenen Gene in Entwicklung und Stoffwechsel steuern. Durch Tests vieler FOX‑Familienmitglieder in nervenähnlichen Zellen entdeckten sie zwei klare Lager. Eine Gruppe (darunter Proteine wie FOXF1) förderte stark die Replikation von Herpes-simplex-Virus Typ 1 (HSV‑1) und mehreren verwandten „Alpha“-Herpesviren. Eine andere Gruppe (FOXK1 und FOXK2) wirkte dagegen und unterdrückte das Viruswachstum deutlich. Dieses Gleichgewicht war nicht in allen Zelltypen gleich: Nicht‑neurale Zellen und gestresste Neuronen produzierten tendenziell mehr der aktivierenden FOX‑Proteine, während ruhende Sinnesneuronen nur sehr geringe Mengen der aktivierenden, aber hohe Mengen der repressiven FOXK‑Proteine herstellten.
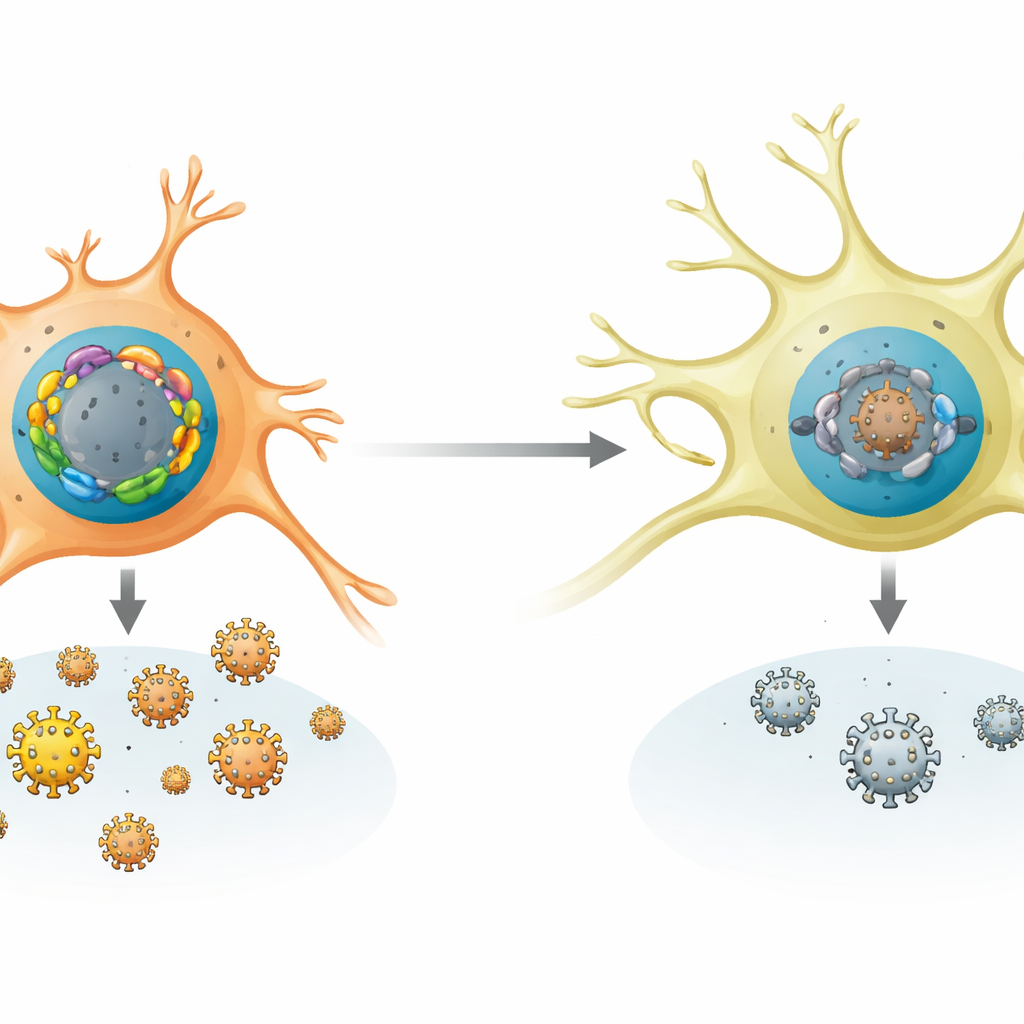
Wie Nervenzellen den ruhenden Zustand begünstigen
Das Team verglich die FOX‑Genaktivität in vielen menschlichen und murinen Zelltypen und in infizierten Tieren. Sinnesneuronen, der natürliche Aufenthaltsort für latentes HSV‑1, zeigten ein Muster, das Stille begünstigt: starke Expression von FOXK1 und FOXK2 und geringe Expression der meisten aktivierenden FOX‑Gene. Bei Mäusen erhöhten frühe Infektion und spätere Stresssignale wie Hitze oder Gewebeverletzung selektiv die Level mehrerer aktivierender Fox‑Gene, ohne die repressiven zu verringern. In kultivierten Mausneuronen und in lebenden Mäusen machte das Entfernen oder Herunterregulieren von FOXK‑Proteinen HSV‑1 leichter replizierbar und erleichterte das Aufspringen aus der Latenz. Umgekehrt reichte es aus, Neuronen dazu zu bringen, zusätzliche aktivierende FOX‑Proteine zu produzieren, um eine Reaktivierung auszulösen – selbst ohne chemische Auslöser und damit sehr anschaulich, wie empfindlich der virale Zustand auf dieses FOX‑Gleichgewicht reagiert.
Viralem DNA packen und sie öffnen oder schließen
Um den zugrunde liegenden Mechanismus zu verstehen, kartierten die Forschenden, wo FOX‑Proteine auf dem viralen Genom sitzen. Sie fanden, dass sowohl der aktivierende FOXF1 als auch der repressiv wirkende FOXK1 weit über HSV‑1‑DNA gebunden sind, nicht nur an einigen wenigen spezifischen Sequenzmotiven. Diese Bindung beruht auf einem konservierten Teil der FOX‑Proteine, der an das DNA‑Rückgrat greift statt an einzelne Basen, was ihnen erlaubt, sich nahezu überall anzuheften. Einmal gebunden, rekrutieren die beiden Proteinlager unterschiedliche molekulare Partner, die das Chromatin – die Kombination aus DNA und ihren Verpackungsproteinen – umgestalten. Aktivierende FOX‑Proteine, besonders FOXF1, assoziieren mit CBP und P300, Enzymen, die Acetylgruppen an Histone anbringen und so das Chromatin lockern. Das macht die virale DNA zugänglicher und steigert die Aktivität früher, mittlerer und später viraler Gene. FOXK1 dagegen wirkt mit Faktoren wie SIN3A und MAX zusammen, die mit Histondeacetylierung und Genrepression verknüpft sind, wodurch das virale Chromatin verfestigt und Gene abgeschaltet bleiben.
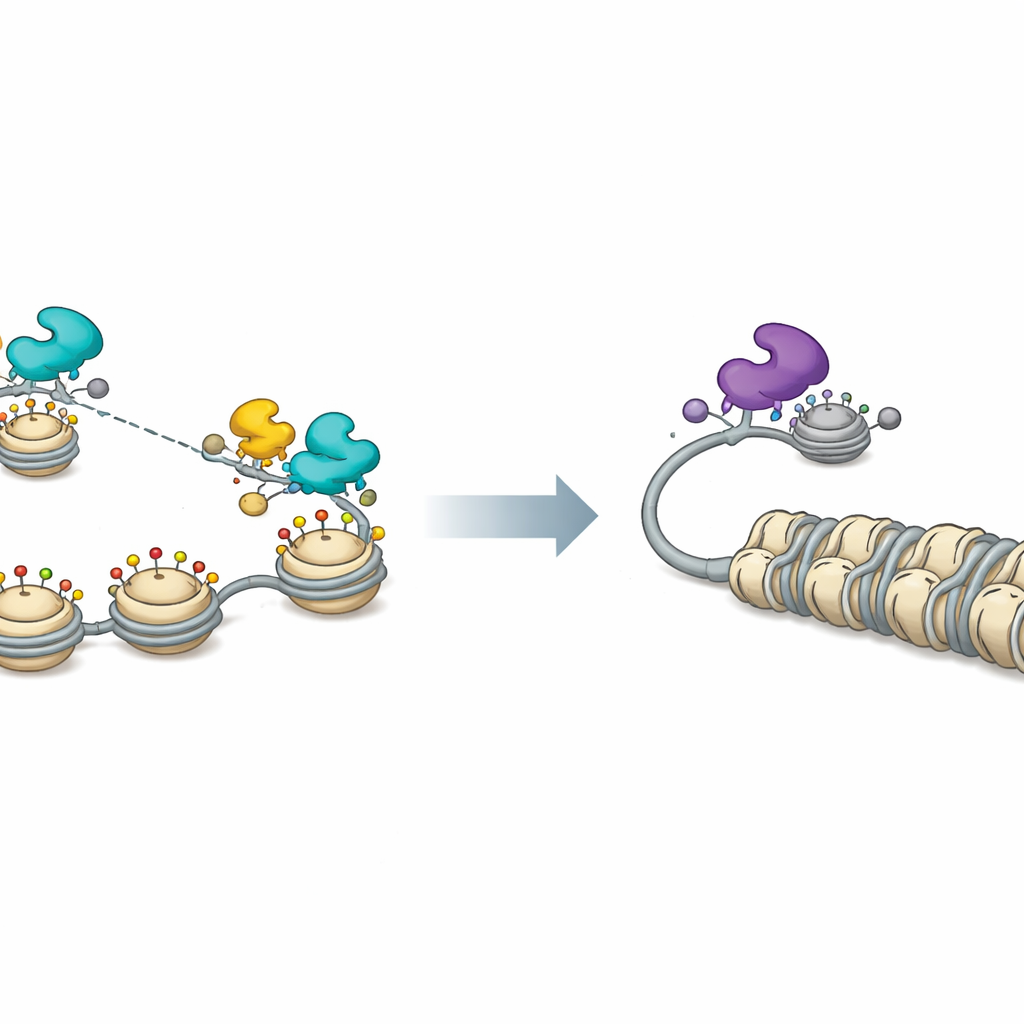
Ein Chromatinschalter für viralen Schlaf und Wachsein
Messungen am viralen Chromatin bestätigten dieses Bild. In Anwesenheit von FOXF1 waren Histone auf der viralen DNA reduziert oder chemisch markiert in einer Weise, die mit offenem, aktivem Chromatin assoziiert ist, und die allgemeine Zugänglichkeit viraler Promotoren nahm über das Genom zu. Die Expression von FOXF1 dispersierte außerdem kleine nukleare Strukturen, sogenannte PML‑Körper, die normalerweise helfen, virale DNA repressiv zu halten. Das Blockieren von CBP und P300 beseitigte viele dieser aktivierenden Effekte und reduzierte die durch FOXF1 vermittelte virale Genexpression. Auf der repressiven Seite zeigten die Forschenden, dass FOXK1‑assoziierte Partner und Histondeacetylase‑Aktivität wichtig sind, um die HSV‑1‑Replikation niedrig zu halten; die chemische Hemmung von Deacetylasen steigerte sowohl die Virusproduktion als auch die Wirksamkeit der FOXK1‑vermittelten Unterdrückung schwächte.
Welche Bedeutung das für die Kontrolle lebenslanger Infektionen hat
In der Summe deuten die Ergebnisse darauf hin, dass der aktive oder ruhende Zustand von HSV‑1 stark vom Mix der FOX‑Proteine im Wirtsneuron abhängt. Ruhende Sinnesneuronen begünstigen natürlicherweise den repressiven, von FOXK dominierten Zustand und drücken das Virus in eine tief stille, chromatinverdichtete Form. Stress oder andere Bedingungen, die aktivierende FOX‑Proteine erhöhen, können dieses Gleichgewicht kippen, das virale Chromatin öffnen und den lytischen Zyklus wieder starten. Indem die Studie dieses epigenetische Tauziehen offenlegt, weist sie auf neue Wege hin, wie Wissenschaftler eines Tages Herpesviren stärker in harmlose Latenz drängen oder umgekehrt kontrolliert aus ihrer Verborgenheit zwingen könnten, damit sie eliminiert werden können.
Zitation: Xiang, Y., Yang, X., Zhang, J. et al. Counteracting FOX proteins epigenetically control the herpesvirus lytic-latent balance. Nat Commun 17, 2256 (2026). https://doi.org/10.1038/s41467-026-68915-1
Schlüsselwörter: Latenz des Herpes-simplex-Virus, FOX-Transkriptionsfaktoren, virales Chromatin, epigenetische Regulation, virale Reaktivierung