Clear Sky Science · de
Erweiterung des DNA-schädigenden Potenzials künstlicher Metallo-Nukleasen durch Click-Chemie
Intelligentere molekulare Scheren bauen
Chemotherapie wirkt oft durch Schädigung der DNA von Krebszellen, doch die heutigen Wirkstoffe sind häufig grobe Werkzeuge, die auch gesundes Gewebe beeinträchtigen. Diese Studie untersucht eine neue Klasse hochgradig programmierbarer „molekularer Scheren“, die aus Kupfer und kleinen organischen Bausteinen bestehen, die mittels Click-Chemie zusammengefügt werden. Durch das Feintuning ihrer Form und ihrer Art, wie sie DNA greifen, wollen die Forschenden Wirkstoffe entwickeln, die genetisches Material präziser zerschneiden und so Wege zu künftigen Krebs- und antibakteriellen Behandlungen öffnen.
Zusammenstecken eines dreifach bewaffneten Cutters
Das Team verwendet kupferkatalysierte Click-Chemie, eine mit dem Nobelpreis ausgezeichnete Methode, die für ihre Zuverlässigkeit bekannt ist, um eine Molekülfamilie namens Tri-Click (TC)-Liganden zusammenzubauen. Jedes TC-Molekül ist ein dreiarmer Knotenpunkt, der drei Kupferionen gleichzeitig halten kann und so einen kompakten Cluster bildet, der die DNA angreifen kann. Durch das Austauschen verschiedener chemischer „Donor“-Gruppen an den Enden der Arme — basierend auf Stickstoff, Sauerstoff oder Schwefel — testeten die Wissenschaftler systematisch, wie subtile Strukturänderungen die Kupferbindung, die DNA-Erkennung und die biologische Aktivität beeinflussen. Unter mehreren neuen Designs hoben sich Varianten mit flachen, ringförmigen Stickstoff-Donoren als besonders vielversprechend für ein festes Greifen der DNA hervor.
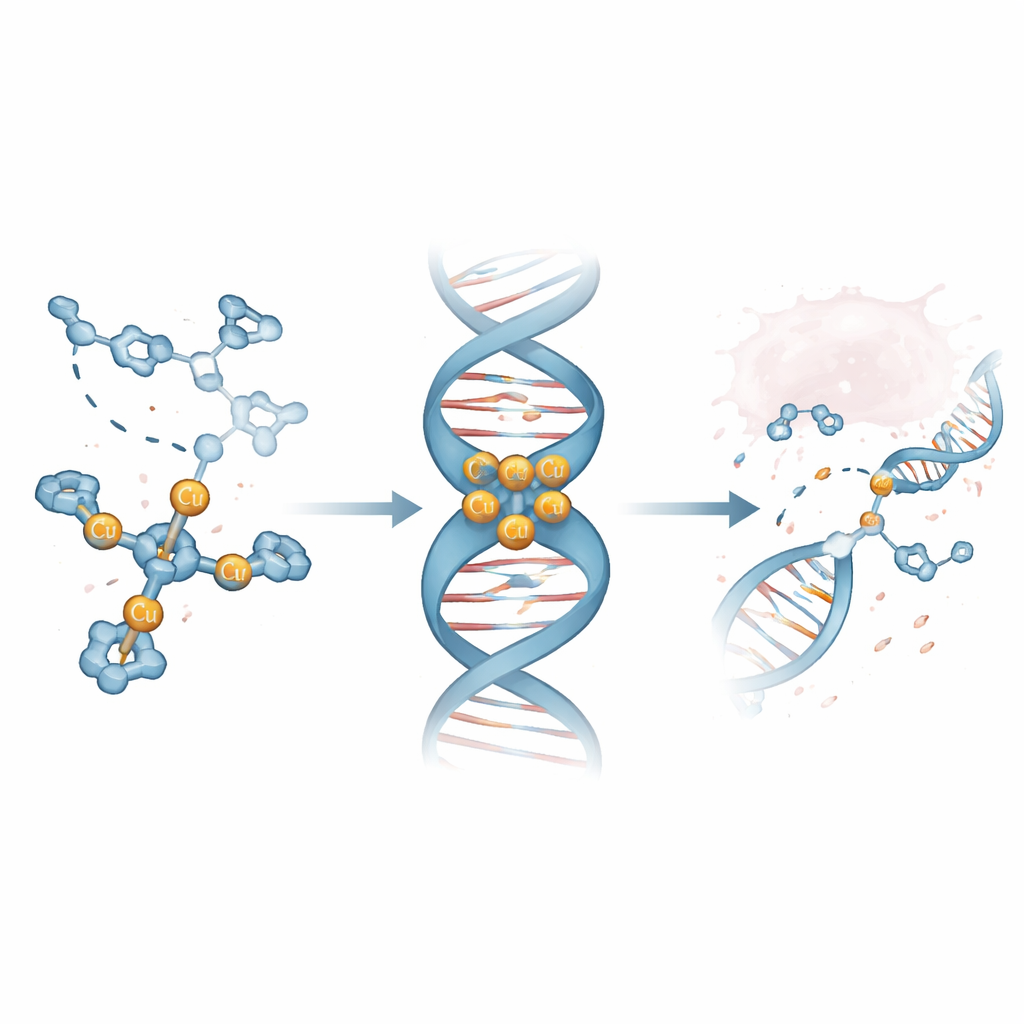
Einen Leitwirkstoff finden, der die DNA-Rillen liebt
Mithilfe von Massenspektrometrie und optischen Methoden zeigten die Forschenden, dass ein Komplex namens Cu3-TC-Py zuverlässig einen Dreifach-Kupfercluster bildet, der in Lösung stabil ist. Konkurrenzexperimente mit fluoreszierenden Farbstoffen, die an Kalbsthymus-DNA gebunden waren, ergaben, dass Cu3-TC-Py diese Farbstoffe schon bei sehr niedrigen Konzentrationen verdrängt, was auf eine starke DNABindung hinweist. Anschlussuntersuchungen an kurzen, haarnadelartig gefalteten DNA-Stücken zeigten, dass dieser Komplex es bevorzugt in die Minor-Grove — die schmalere Rinne, die sich um die DNA-Doppelhelix windet — einzunisten, und dass er besonders Bereiche mit vielen G‑ und C‑Basen bevorzugt. Hochaufgelöste Computersimulationen untermauerten dieses Bild, indem sie den dreiarigen Komplex in der Rinne zeigten, dessen positive Ladungen die negativ geladene DNA umschließen und die Helix dezent kompakter machen.
Von starker Bindung zu DNA-Kollaps und Bruch
Auf Einzelmolekülebene beobachtete das Team lange DNA-Stränge, die in nanogroßen Kanälen eingeschlossen waren, während sie mit Cu3-TC-Py interagierten. Bei niedrigen Dosen konkurrierte der Komplex mit einem Dehnfarbstoff und verdrängte ihn, während er in den Rillen band. Bei höheren Dosen begann die DNA zu schrumpfen und kondensierte schließlich vollständig, was mit starker elektrostatischer Anziehung zwischen dem Kupfercluster und dem DNA-Rückgrat übereinstimmt. Wurden Plasmid-DNA in Gegenwart eines Reduktionsmittels dem Komplex ausgesetzt, wandelten sich die Stränge von ihrer nativen gewundenen Form in entspannte und dann vollständig lineare Formen — ein Muster, das die Entstehung sowohl von Einzel- als auch Doppelstrangbrüchen signalisiert. Weitere Tests mit Radikalfängern machten kurzlebige Sauerstoffspezies — wie Superoxid, Singulett-Sauerstoff und Hydroxylradikale — als die eigentlichen Schneidwerkzeuge aus, die in der Nähe des gebundenen Komplexes erzeugt werden.
Angriff auf DNA in Krebs- und Bakterienzellen
Über gereinigte DNA hinaus untersuchten die Forschenden, wie sich Cu3-TC-Py innerhalb lebender Zellen verhält. In Panelen von Krebszellen zeigten die freien Liganden mit stickstoffreichen aromatischen Gruppen deutlich stärkere Hemmung des Zellwachstums als frühere Entwürfe, und der voll ausgebildete Kupferkomplex war noch wirksamer und tötete mehrere Krebszelllinien bei Mikromolar-Konzentrationen. Messungen des intrazellulären Kupfers ergaben, dass Cu3-TC-Py Kupfer effizient in Zellen transportiert und eine Anhäufung beschädigter DNA auslöst, wie eine reparaturgestützte Bildgebungsmethode zeigte, die Läsionen entlang gestreckter genomischer Stränge markiert. In Bakterien zeigte die Mikroskopie, dass die Behandlung rasch das kompakte bakterielle Chromosom zerstörte, DNA im ganzen Zellinneren verteilte und die starke Fragmentierung nachahmte, wie sie von einem potenten DNA-schädigenden Antibiotikum beobachtet wird — konsistent mit weitreichender genetischer Zerstörung.
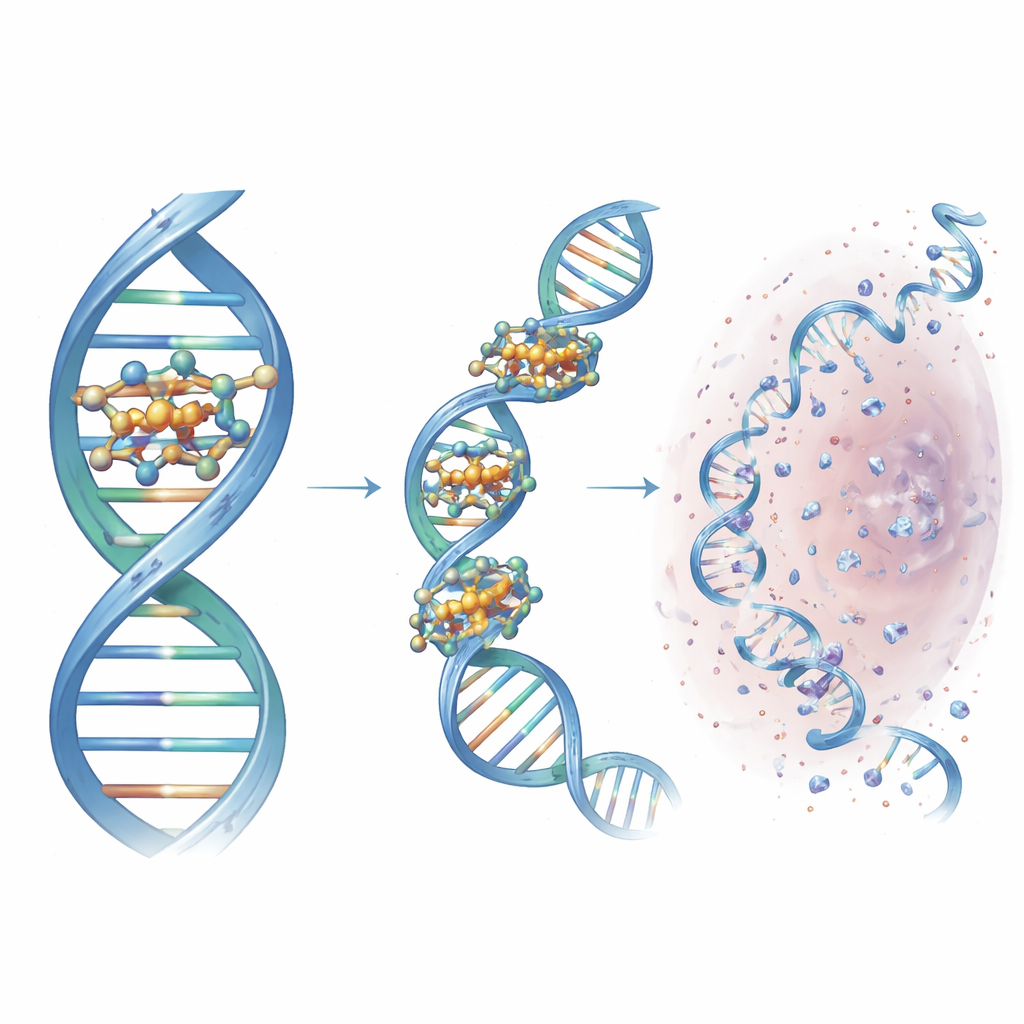
Warum diese Designer-Scheren wichtig sind
Für Nichtfachleute lautet die zentrale Botschaft, dass die Forschenden ein einfaches, modulares Click-Chemie-Gerüst in eine fein abgestimmte DNA-schneidende Maschine verwandelt haben. Durch die Wahl der richtigen ringförmigen Stickstoffgruppen schufen sie einen kompakten Kupfercluster, der in eine spezifische Rille der DNA andockt, die Stränge zusammenzieht und lokal reaktive Sauerstoffspezies erzeugt, die die Doppelhelix auftrennen. Diese Leitverbindung, Cu3-TC-Py, schädigt DNA effizient sowohl in Krebs- als auch in Bakterienzellen und zeigt, wie rationale Gestaltung die Wirkung metallbasierter Wirkstoffe schärfen kann. Obwohl vor einer klinischen Anwendung noch viel Arbeit nötig ist, legt die Studie Designregeln für die nächste Generation molekularer Scheren fest, die eines Tages gezieltere Krebstherapien und neuartige antimikrobielle Strategien ermöglichen könnten.
Zitation: Gibney, A., Sidarta, M., Delahunt, E. et al. Expanding the DNA damaging potential of artificial metallo-nucleases with click chemistry. Nat Commun 17, 2309 (2026). https://doi.org/10.1038/s41467-026-68911-5
Schlüsselwörter: Click-Chemie, DNA-Schaden, Kupferkomplexe, Antikrebsmittel, künstliche Nukleasen