Clear Sky Science · de
Evolutionäre Umwidmung eines metabolischen Thiolase-Komplexes ermöglicht die Biosynthese von Antibiotika
Wie alltägliche Mikroben ihre Chemie neu erfinden
Viele der Antibiotika und Arzneimittel, auf die wir angewiesen sind, werden stillschweigend von Bakterien hergestellt. Diese winzigen Chemiker nutzen Enzyme — molekulare Maschinen — um komplexe Abwehrverbindungen aufzubauen. Die vorliegende Studie zeigt, wie ein zentraler metabolischer Enzymkomplex, einst für grundlegende Zellfunktionen eingesetzt, in oralen Bakterien evolutionär umprogrammiert wurde, um ein wirksames Antibiotikum herzustellen. Das Verständnis dieser Umwandlung offenbart nicht nur, wie die Natur neue Chemie erfindet, sondern liefert auch Hinweise für die Entwicklung neuartiger Wirkstoffe und Biokatalysatoren.
Von Grundstoffwechsel zur chemischen Bewaffnung
Alle lebenden Zellen sind auf einen Satz konservierter Enzyme angewiesen, die ihren zentralen Stoffwechsel steuern, etwa beim Abbau von Fetten oder beim Aufbau essentieller Moleküle. Eine dieser Gruppen, die Thiolase-Superfamilie, hilft normalerweise beim Umgang mit kleinen energiereichen Verbindungen wie Acetyl-CoA und unterstützt wichtige Wege zur Synthese von Lipiden und anderen Zellbestandteilen. Die Autoren fanden heraus, dass in mehreren oralen Streptococcus-Arten ein dreiteiliger, auf Thiolase basierender Komplex — aus Proteinen verwandt mit HMGS, ACAT und einem dritten Hilfsprotein — seine ursprüngliche metabolische Rolle aufgegeben hat. Stattdessen vervollständigt dieser Komplex nun die Biosynthese eines Antibiotikums namens Reutericyclin A, das diesen Bakterien hilft, in der dicht besetzten Mundhöhle zu konkurrieren.
Eine neue Art enzymatischer Reaktion auf einem Antibiotika-Gerüst
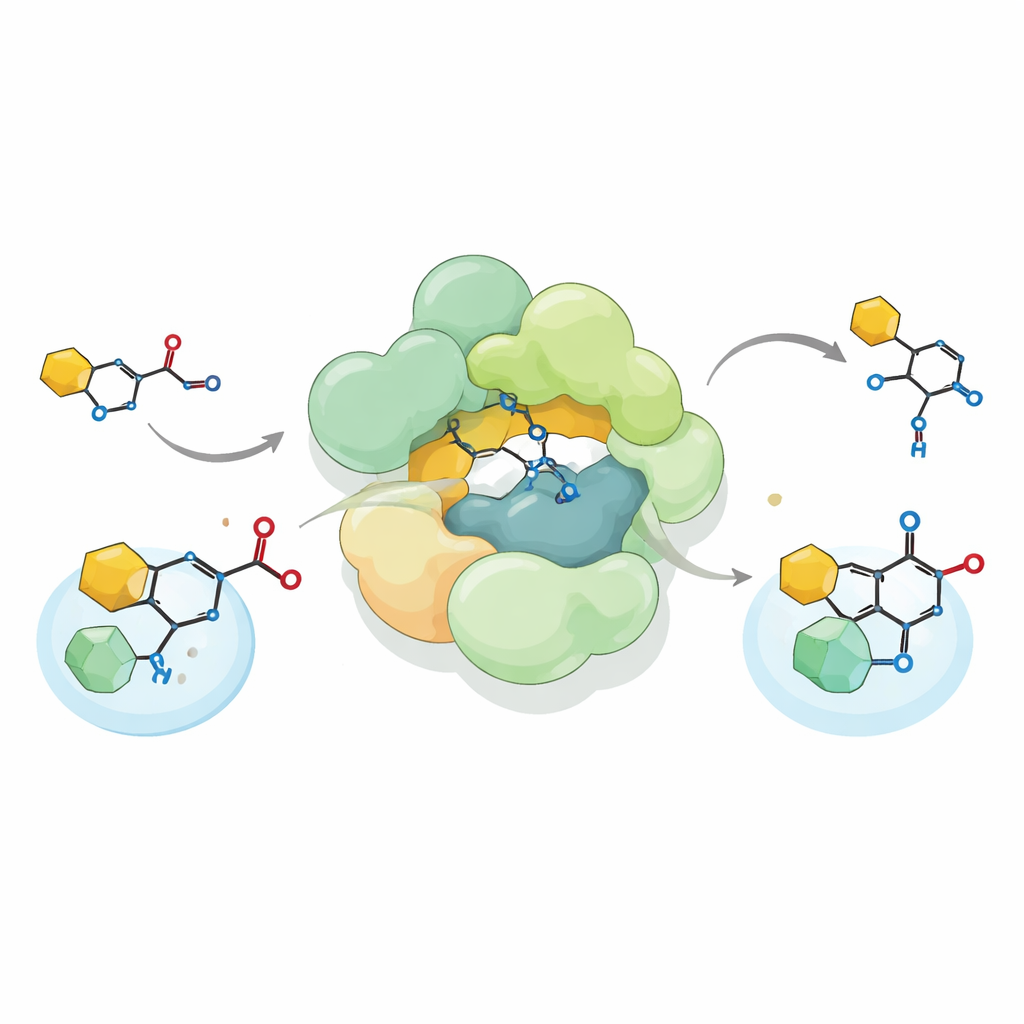
Durch das Rekonstituieren des Streptococcus-Komplexes im Labor und das Zufüttern eines chemisch synthetisierten Vorläufers von Reutericyclin A zeigten die Forschenden, dass der Komplex eine ungewöhnliche C–C-Bindungsbildende Reaktion ausführt, bekannt als Friedel–Crafts C‑Acylierung. Anstatt wie viele Enzyme eine Acetylgruppe an Sauerstoff zu binden, bringt er diese Gruppe direkt an ein Kohlenstoffatom eines Pyrrolidin-2,4-dion-Rings an — ein wichtiger Teil des Reutericyclin-Grundgerüsts. Der Komplex akzeptiert sowohl natürliche Acetyl-Donoren wie Acetyl‑CoA als auch mehrere künstliche Donoren und kann die Reaktion sogar umkehren, also die gebildete Bindung wieder spalten. Diese Flexibilität erweitert das bekannte Repertoire biologischer Acyltransferasen und deutet an, wie solche Enzyme adaptiert werden könnten, um vielfältige chemische Produkte zu bauen.
Umwidmung eines konservierten Proteingerüsts
Mithilfe hochauflösender Kryo-Elektronenmikroskopie bestimmten die Forscher die dreidimensionale Struktur des Streptococcus-Komplexes, bezeichnet als SmaATase. Trotz seiner neuen Funktion behält SmaATase eine auffällige architektonische Ähnlichkeit zu einem verwandten Komplex in Archaea, der an der Mevalonat‑Stoffwechselbahn zur Herstellung isoprenoider Lipide beteiligt ist. Beide sind große multimerische Assemblagen, aufgebaut aus sich wiederholenden Modulen, und zeigen eine gemeinsame Kavität, in der das Coenzym A binden und zwischen aktiven Zentren wandern kann. Allerdings fehlen im bakteriellen Pendant Schlüsselreste, die für die ursprüngliche metabolische Reaktion essenziell sind, oder sie sind verändert. Biochemische Tests bestätigen, dass SmaATase das ancestrale Produkt HMG‑CoA nicht mehr herstellen kann und stattdessen Acetyl‑CoA ausschließlich als Donor für seine neuen kleinmolekularen Substrate nutzt.
Eine evolutionäre Spur vom Stoffwechsel zu Antibiotika
Um zu verstehen, wie eine solche Umwidmung zustande gekommen sein könnte, verglichen die Autoren Sequenzen und Aktivitäten verwandter Komplexe über viele Bakterien und Archaea hinweg. Sie identifizierten über tausend Gencluster, die die gleiche Dreierkombination von Enzymtypen enthalten. Einige unterstützen noch klassische Thiolase-Chemie; andere, wie jene in Pseudomonas, treiben die Biosynthese anderer kleinmolekularer Antibiotika an. Ein repräsentativer Komplex aus Pseudomonas fluorescens scheint sich entlang dieses evolutionären Pfades in einem Zwischenzustand zu befinden: Seine HMGS‑ähnliche Domäne ist deaktiviert, aber seine ACAT‑ähnliche Einheit führt noch eine konventionellere Reaktion an CoA-gebundenen Substraten aus. In SmaATase und seinem Pseudomonas‑Gegenstück, das die pflanzenschutzwirksame Verbindung DAPG herstellt, haben weitere Veränderungen in der Umgebung des aktiven Zentrums die Enzyme dahingehend zugeschnitten, untypische Akzeptoren wie aromatische Ringe oder Tetraminsäure-Kerne zu erkennen.
Warum eine winzige Acetylgruppe einen großen Unterschied macht
Letztlich ist der biologische Nutzen dieser molekularen Umgestaltung eindeutig. Als das Team die acetylierten Antibiotika Reutericyclin A und DAPG gegen ein Panel grampositiver Bakterien testete, zeigten diese Moleküle starke bakterizide Aktivität, während ihre unacetylierten Vorstufen deutlich schwächer oder nahezu inaktiv waren. Diese kleine Acetylgruppe, an genau der richtigen Stelle vom umgewidmeten Enzymkomplex platziert, verwandelt ein bescheidenes Grundgerüst in eine potente Waffe und ermöglicht es Streptococcus im Mund oder Pseudomonas in der Wurzelzone, ihre Nachbarn zu übertrumpfen. Diese Arbeit zeigt, wie die Evolution bestehende Enzym‑Frameworks mit minimalen, aber gezielten Mutationen recyceln kann, um routinemäßige metabolische Maschinerie in spezialisierte Werkzeuge zur chemischen Abwehr zu verwandeln — und liefert einen Leitfaden für Ingenieure, die neue C–C-Bindungsbildende Katalysatoren für Wirkstoffforschung und synthetische Biologie entwerfen wollen.
Zitation: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
Schlüsselwörter: Enzym-Evolution, Biosynthese natürlicher Produkte, Antibiotika-Chemie, metabolische Umwidmung, Friedel–Crafts-Acylierung