Clear Sky Science · de
Plasmide mit synthetischen Replikationsursprüngen konstruieren
Warum das Neuschreiben mikrobieller DNA wichtig ist
Viele der Werkzeuge der modernen Biotechnologie, von der Insulinproduktion bis zu fortschrittlichen Gen-Schaltkreisen, beruhen auf kleinen DNA-Ringen, den Plasmiden. Diese genetischen Arbeitspferde transportieren veränderte Gene in Bakterien, doch ihr Grundaufbau hat sich seit Jahrzehnten kaum gewandelt. Die vorliegende Studie zeigt, dass das eigentliche Herz der Plasmide—die Sequenzen, die Zellen sagen, wann und wie oft sie kopiert werden sollen—komplett neu gedacht werden können. Indem die Autoren diese „Kopie‑Maschine“ von Grund auf neu aufbauen, entstehen Plasmide, die sich leichter einstellen, kombinieren und programmieren lassen und damit flexiblere Diagnostika, Bioproduktion und Anwendungen in der synthetischen Biologie ermöglichen.
Alte Werkzeuge mit verborgenen Grenzen
Plasmide haben sich natürlicherweise als mobile DNA entwickelt und helfen Bakterien, Merkmale wie Antibiotikaresistenz oder neue Wege zur Nährstoffnutzung zu teilen. Im Labor verwenden Ingenieure diese Plasmide, um nützliche Gene zu transportieren, doch die meisten nutzen wenige klassische Designs, die in den 1980er Jahren entdeckt wurden. Diese alten Konstrukte verbergen ein Geflecht überlappender genetischer Bausteine, die steuern, wie viele Kopien eines Plasmids in jeder Zelle vorhanden sind und ob verschiedene Plasmide koexistieren können. Weil diese Teile miteinander verflochten sind, kann die Änderung einer Eigenschaft unvorhergesehen eine andere beeinträchtigen. Als Folge bleiben Forschende bei einer begrenzten Auswahl an Plasmiden mit festen Kopienzahlen und eingeschränkter Kompatibilität, was die Komplexität gentechnisch entworfener Systeme limitiert.
Die Kopier‑Maschine von Grund auf neu aufbauen
Die Forschenden konzentrierten sich auf einen weit verbreiteten Replikationsursprung aus der pMB1‑Plasmidfamilie. In seiner natürlichen Form nutzt dieser Ursprung ein fein austariertes Gespräch zwischen zwei RNAs—eine, die das Kopieren der DNA startet, und eine andere, die es stoppt—um die Plasmidanzahl zu regulieren. Das Team „refaktorierte“ zunächst dieses System: sie lösten überlappende Gene, deaktivierten einen verborgenen Promoter und brachten zentrale Elemente auf separaten, sauberen Kassetten unter. Allein dadurch zeigte sich, dass die Kernfunktion des Ursprungs erhalten bleiben kann, während die Architektur vereinfacht wird, sodass aus einem chaotischen, evolutionsgeformten Bauteil ein modularerer Mechanismus mit zugänglichen Komponenten wird.
Synthetische Stellschrauben einsetzen
Mit offengelegter Steuerlogik ersetzten die Autoren diese anschließend durch komplett synthetische Regulatoren. Sie verbanden das Replikationsprimer mit konstruierten RNA‑Schaltern, die wie Dimmer funktionieren: kleine regulatorische RNAs können diese Schalter umlegen, um die Produktion des Primers entweder zu erlauben oder zu blockieren und damit das Plasmidkopieren zu steuern. Durch Auswahl verschiedener Schaltervarianten und die Kombination mit Promotern unterschiedlicher Stärke stellten sie die Kopienzahl über mehr als zwei Größenordnungen ein. Außerdem untersuchten sie verschiedene physische Anordnungen der Kontrollkassetten auf der DNA, fanden Konstellationen, die die Stabilität verbesserten, und konnten den Replikationsbereich auf einen kompakten, funktionalen Kern verkleinern, während sie natürliche Hilfssysteme integrierten, die problematische Plasmidverflechtungen verhindern.
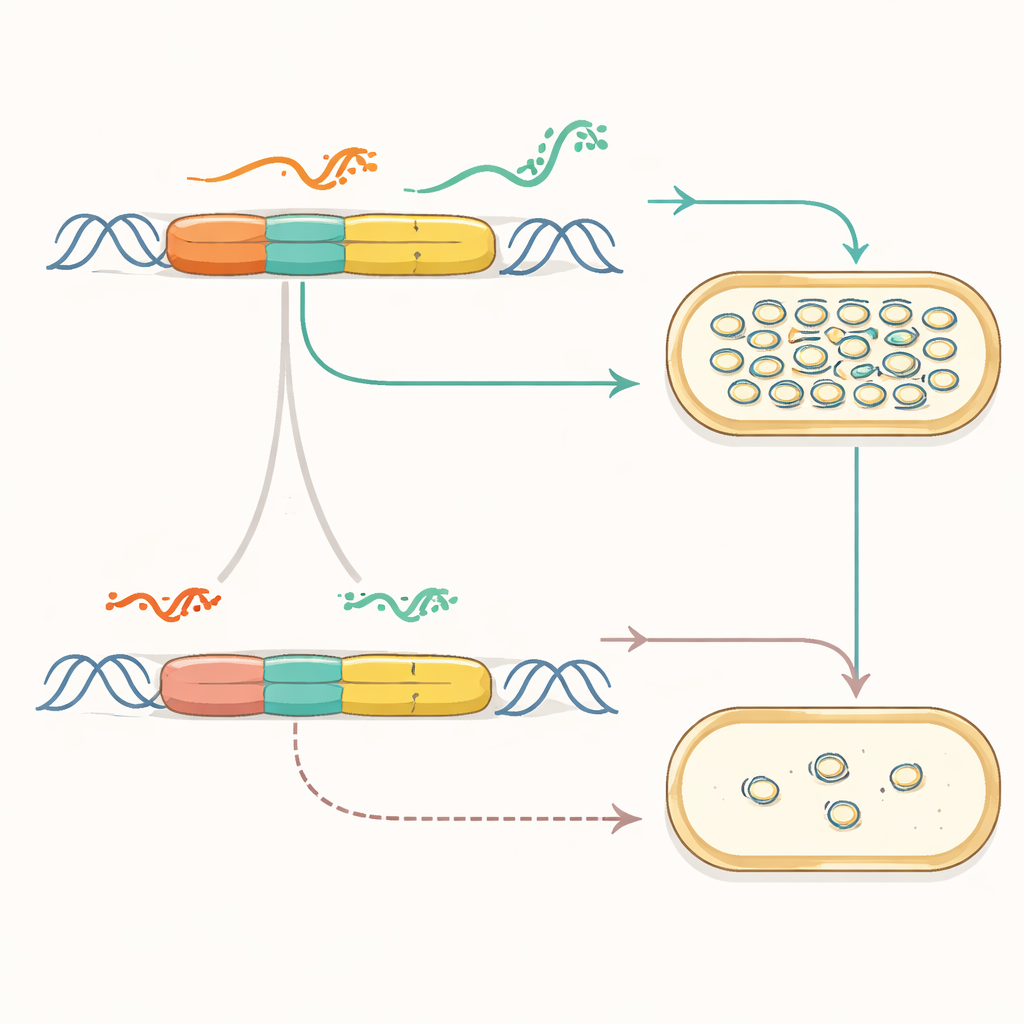
Chemische Signale in DNA‑Zahlen verwandeln
Sobald die Kopier‑Maschine modular war, demonstrierte das Team, dass sie an äußere Signale angebunden werden kann. Sie verknüpften den synthetischen Ursprung mit induzierbaren Promotern und RNA‑Strukturen, sogenannten Riboschaltern, die ihre Form als Reaktion auf kleine Moleküle verändern. In diesen neuen Plasmiden führte das Hinzufügen einer Chemikalie wie IPTG oder Cumate dazu, dass die Plasmidkopienzahl—und damit ein Reporter‑Signal—anstieg oder sank. Mehrere Signale ließen sich so kombinieren, dass eine Chemikalie das Kopieren antrieb, während eine andere es bremste. Die Forschenden bauten sogar Plasmidpaare, die jeweils auf unterschiedliche Chemikalien reagierten, und verfolgten ihre sich ändernden Kopienzahlen in derselben Zelle mittels DNA‑Sequenzierung, wodurch Plasmidzählungen effektiv zu einem Barcode der Umweltgeschichte wurden.
Viele maßgeschneiderte Plasmide in einer Zelle
Ein zentraler Test dieser Methode war, ob mehrere unabhängig gesteuerte Plasmide koexistieren können. Mithilfe einer Bibliothek orthogonaler RNA‑Regulatoren baute das Team sechs verschiedene Plasmide, jeweils mit einem eigenen synthetischen Ursprung und einem Antibiotikaresistenzmarker, und führte alle sechs gleichzeitig in E. coli ein. Vollständige Plasmidsequenzierungen über mehrere Tage bestätigten, dass alle sechs erhalten blieben, obwohl sich ihre relativen Anteile verschoben. Versuche mit sechs herkömmlichen Plasmiden schlugen fehl, was unterstreicht, dass das refaktorierte Design und die hinzugefügten Stabilitätssysteme die neuen Plasmide kompatibler und robuster machen, wenn sie sich eine einzelne Zelle teilen.
Was das für die zukünftige Biotechnologie bedeutet
Für Nicht‑Spezialisten ist die Schlussfolgerung klar: Die Autoren haben Plasmide von starren, universellen Werkzeugen in eine anpassbare Plattform verwandelt. Ihre synthetischen Replikationsursprünge verhalten sich wie Plug‑and‑Play‑Motoren, deren Geschwindigkeit, Empfindlichkeit und Eingänge nach Bedarf gewählt werden können. So lassen sich Bakterien konstruieren, die chemische Expositionen als Veränderungen der DNA‑Kopienzahl aufzeichnen, viele genetische Wege parallel testen, indem man sie auf mehrere Plasmide verteilt, oder Wachstum und Produktion in industriellen Stämmen fein austarieren. Zwar bleiben einige Stabilitätskompromisse bestehen, doch zeigt diese Arbeit, dass die Kernmechanik der Plasmidreplikation nicht länger tabu für ingenieurwissenschaftliche Eingriffe ist und so neuen Raum für Innovation in der synthetischen Biologie eröffnet.
Zitation: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
Schlüsselwörter: synthetische Plasmide, Replikationsursprung, RNA-Regulatoren, Kopienzahl-Kontrolle, synthetische Biologie