Clear Sky Science · de
Rezeptor für Succinat 1 beschränkt die Hämatopoese und verhindert das Fortschreiten von akuter myeloischer Leukämie
Wenn Zelltreibstoff außer Kontrolle gerät
Unser Blut wird ständig von einer kleinen Population von Stammzellen im Knochenmark erneuert. Diese Studie untersucht, wie ein verbreitetes Stoffwechselnebenprodukt, Succinat, und sein Sensor an der Zelloberfläche als Bremse dieses Erneuerungssystems wirken. Versagt diese Bremse, kann das Gleichgewicht zwischen gesunder Blutbildung und krebsartigem Wachstum zugunsten der akuten myeloischen Leukämie (AML) kippen, einer aggressiven Blutkrebserkrankung. Das Verständnis dieses verborgenen Kontrollschalters könnte zu präziseren Therapien führen, die die Krankheit eindämmen, indem sie die körpereigenen Schutzmechanismen wiederherstellen.
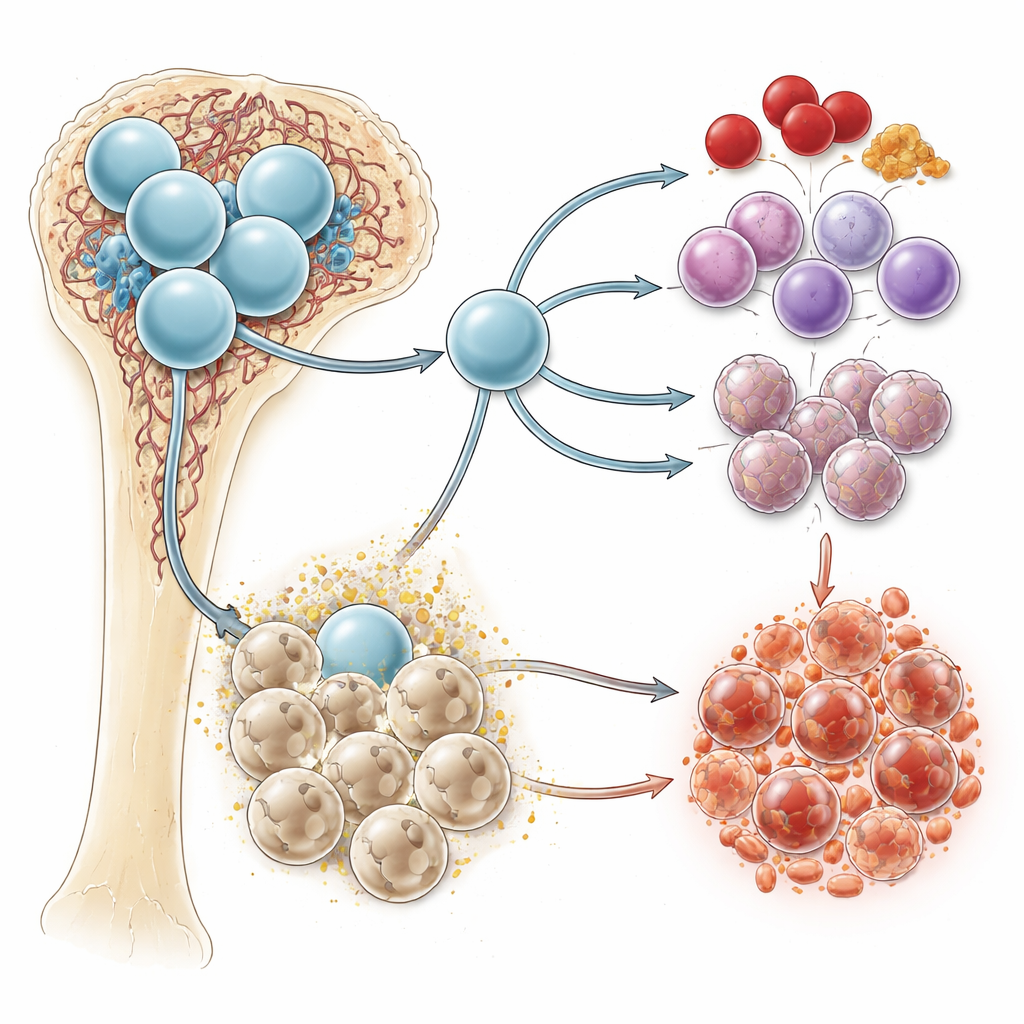
Ein chemisches Signal mit doppelter Rolle
Succinat ist ein routinemäßiges Nebenprodukt der Zellatmung, vor allem in den Mitochondrien, den Kraftwerken der Zelle. Unter sauerstoffarmen Bedingungen – wie im Knochenmark – reichert sich Succinat eher an. Es kann innerhalb von Zellen wirken, den Stoffwechsel und Entzündungsreaktionen verändern, und es kann auch nach außen gelangen, um als Signal zu fungieren. An der Zelloberfläche erkennt ein Rezeptor namens SUCNR1 Succinat und übermittelt dessen Anwesenheit ins Zellinnere. Frühere Arbeiten verbanden Succinat und SUCNR1 mit Entzündungen und krebsfördernden Umgebungen, doch ihre direkte Rolle bei der Blutbildung und der Leukämie war unklar.
Ein Warnsignal bei Leukämiepatienten
Die Forschenden analysierten Genexpressionsdaten von Hunderten AML-Patienten und stellten fest, dass die SUCNR1-Spiegel zwischen Individuen stark variieren. Patienten, deren Leukämiezellen wenig SUCNR1 produzierten, hatten eine kürzere Gesamt- und progressionsfreie Überlebenszeit, selbst nach Anpassung für Alter, Geschlecht und übliche klinische Subtypen. Bestimmte genetische Untergruppen von AML zeigten tendenziell besonders niedrige SUCNR1-Werte. Als das Team humane AML-Zellen ohne SUCNR1 in immundefiziente Mäuse transplantierte und den Tieren anschließend Bernsteinsäure (die im Körper zu Succinat wird) injizierte, nahm die leukämische Belastung im Knochenmark zu. Dies deutet darauf hin, dass in Krebserkrankungen mit niedrigem SUCNR1 zusätzliches Succinat die Krankheitsprogression eher anfachen kann, statt sie zu bremsen.
Die verborgene Bremse der Blutstammzellen
Um zu verstehen, wie SUCNR1 bei der normalen Blutbildung wirkt, nutzten die Wissenschaftler genetisch veränderte Mäuse. Wurde SUCNR1 entweder im ganzen Tier oder nur in den blutbildenden Zellen gelöscht, wurde das Knochenmark überaktiv. Stamm- und Vorläuferzellen vermehrten sich, und sowohl myeloide Zellen (wie Monozyten und Granulozyten) als auch B‑Zellen nahmen im Blut und in der Milz zu. Diese stammlingeähnlichen Zellen überlebten besser und bildeten mehr Kolonien in Laboransätzen, obwohl sie etwas weniger fähig waren, die Blutbildung wiederherzustellen, wenn sie im Wettbewerb mit normalen Zellen transplantiert wurden. Eine spezielle Reportermaus zeigte, dass nur ein Teil der Stamm- und Vorläuferzellen tatsächlich SUCNR1 exprimiert; diese SUCNR1-positiven Zellen hatten ein besonders eingeschränktes Engraftment-Potenzial. Insgesamt wirkte der Rezeptor als Einschränkung der Größe und Aktivität des Stammzellpools.
Von ausgewogener Abwehr zu entzündlichem Überdrehen
Detaillierte Genexpressionsprofile von Stamm- und Vorläuferzellen ohne SUCNR1 zeigten eine markante Verschiebung. Signaturen ruhiger, primitiver Stammzellen wurden abgeschwächt, während Gene, die mit Entzündung, reaktiven Sauerstoffspezies und ausgereiften Blutzelltypen verknüpft sind, verstärkt wurden. Zwei Moleküle hoben sich besonders hervor: S100A8 und S100A9, ein Paar von „Alarminen“, die entzündliche Signalwege verstärken. Diese Faktoren waren sowohl innerhalb der Stammzellkompartimente als auch in der umgebenden Knochenmarkflüssigkeit erhöht. Behandelten die Forschenden SUCNR1-defiziente Mäuse mit Tasquinimod, einem Wirkstoff, der die S100A9-Signalgebung blockiert, wurde die übermäßige Expansion von Stamm- und Vorläuferzellen sowie die Überproduktion von Myelozyten und B‑Zellen weitgehend rückgängig gemacht. Mit anderen Worten: Vieles des Schadens durch den Verlust von SUCNR1 ließ sich durch Unterbrechung der S100A8/S100A9-Alarmkette beheben.
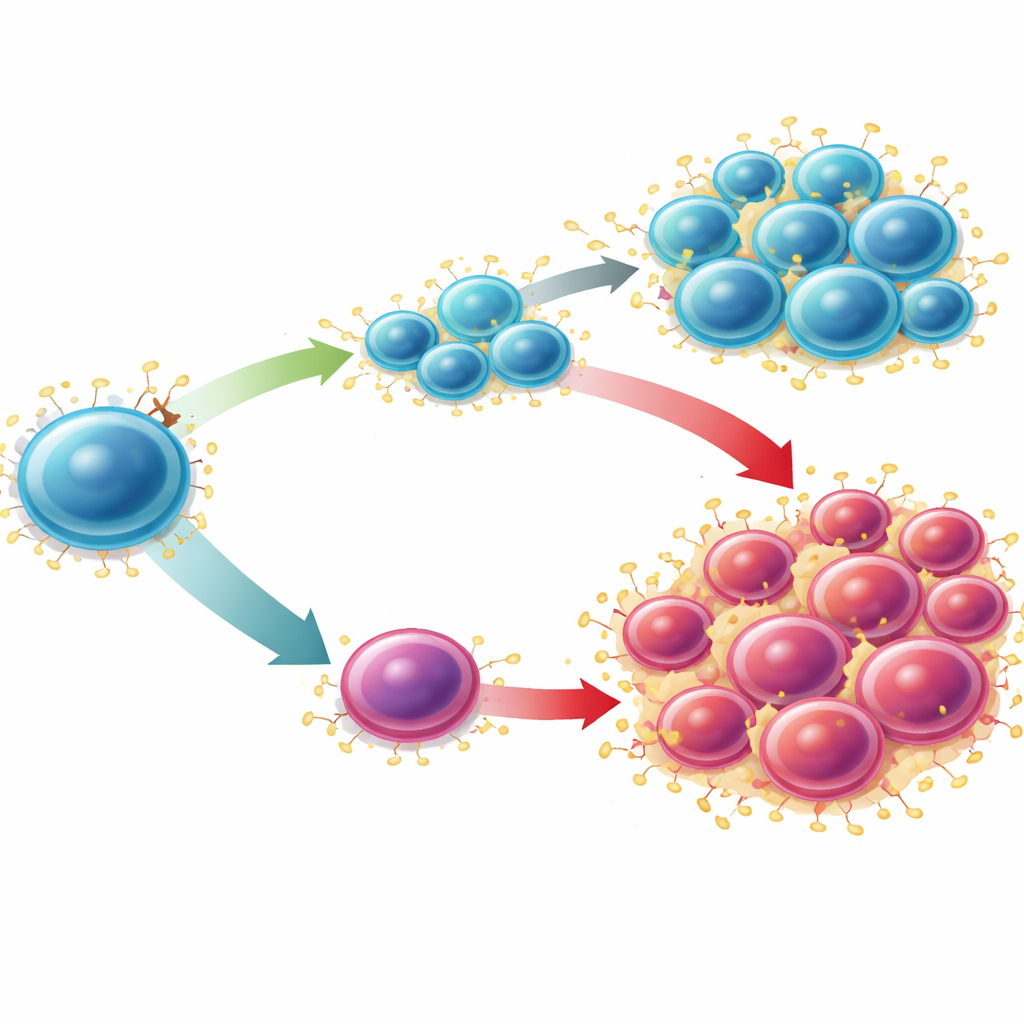
Eine Verwundbarkeit in eine Behandlungsstrategie verwandeln
Die Wissenschaftler fragten dann, ob sich dieser Signalweg therapeutisch in der AML ausnutzen lässt. In einer aggressiven Mausleukämie, die vom MLL-AF9-Mutanten getrieben wird – in der Sucnr1-Spiegel sehr niedrig sind – verringerte die Blockade von S100A9 mit Tasquinimod, insbesondere in Kombination mit einer wirksamen SUCNR1-aktivierenden Verbindung, die leukämischen stammzellähnlichen Zellen und senkte die Krankheitslast in Knochenmark und Milz. Analysen von Einzelzell-RNA-Daten aus humanen AML-Modellen, die mit dem Chemotherapeutikum Cytarabin behandelt wurden, zeigten, dass resistente Zellcluster reich an S100A8 und S100A9 waren, während SUCNR1 spärlich vorhanden war und mit einer anderen, stoffwechselaktivierten Untergruppe assoziiert war, die nach Behandlung schrumpfte. In humanen Leukämiezelllinien führte die Aktivierung von SUCNR1 zu vermehrtem chemotherapiebedingtem Zelltod und konnte bei Überexpression von SUCNR1 allein Apoptose auslösen. Zusammen positionieren diese Befunde niedrige SUCNR1-Werte nicht nur als Marker für schlechte Prognose, sondern auch als Schwachstelle: Leukämiezellen, die diese Bremse verloren haben, können stark von der S100A8/S100A9‑Achse abhängig sein und besonders empfindlich auf Strategien reagieren, die SUCNR1‑Signalgebung reaktivieren oder den nachgeschalteten Alarm blockieren.
Ein neuer Hebel zur Eindämmung der Leukämie
Für eine nichtfachliche Leserschaft lautet die zentrale Botschaft: Ein scheinbar unscheinbares Stoffwechselnebenprodukt, Succinat, und sein Rezeptor SUCNR1 bilden ein unerwartetes Sicherheitssystem in der Blutbildung. Wenn SUCNR1 vorhanden und aktiv ist, hält es die Stammzellen in Schach und verhindert ein unkontrolliertes Wachstum. Geht SUCNR1 verloren oder ist es niedrig – wie bei einigen AML-Patienten häufig beobachtet – können Succinat und entzündliche Alarmstoffe wie S100A8 und S100A9 Stamm- und Vorläuferzellen zu Übervermehrung und Leukämie treiben. Durch die Kombination von Wirkstoffen, die diesen entzündlichen Alarm dämpfen, mit solchen, die SUCNR1‑Signalgebung wiederherstellen oder nachahmen, könnte es möglich sein, das System zurück zu ausgewogener Blutbildung zu steuern und die Wirksamkeit bestehender Chemotherapien zu verbessern.
Zitation: Cuminetti, V., Boet, E., Heugel, M. et al. Succinate receptor 1 restricts hematopoiesis and prevents acute myeloid leukemia progression. Nat Commun 17, 2403 (2026). https://doi.org/10.1038/s41467-026-68906-2
Schlüsselwörter: akute myeloische Leukämie, Succinatrezeptor, hämatopoetische Stammzellen, Stoffwechsel und Krebs, inflammatorische Signalgebung