Clear Sky Science · de
Gezielt veränderte Alkohol‑Oxidasen katalysieren Transesterifizierungen in wässriger Umgebung ohne konkurrierende Hydrolyse
Warum diese Enzym‑Geschichte wichtig ist
Viele Alltagsprodukte — von Arzneimitteln und Lebensmittelaromen bis hin zu Biodiesel — beruhen auf einer einfachen chemischen Bindung, dem Ester. Ester effizient, kostengünstig und umweltfreundlich herzustellen und zu optimieren ist ein zentrales Ziel der Grünen Chemie. Das Problem: Wasser, das aus Sicherheits‑ und Nachhaltigkeitsgründen das ideale Lösungsmittel wäre, verhindert solche Reaktionen oft, indem es Ester so schnell wieder aufspaltet, wie sie gebildet werden. Die vorliegende Studie beschreibt ein gentechnisch verändertes Enzym, das Ester in wässriger Lösung aufbaut und das umgebende Wasser nahezu vollständig ignoriert — ein Wegbereiter für sauberere industrielle Chemie.
Ein bekanntes Enzym für eine neue Aufgabe umfunktioniert
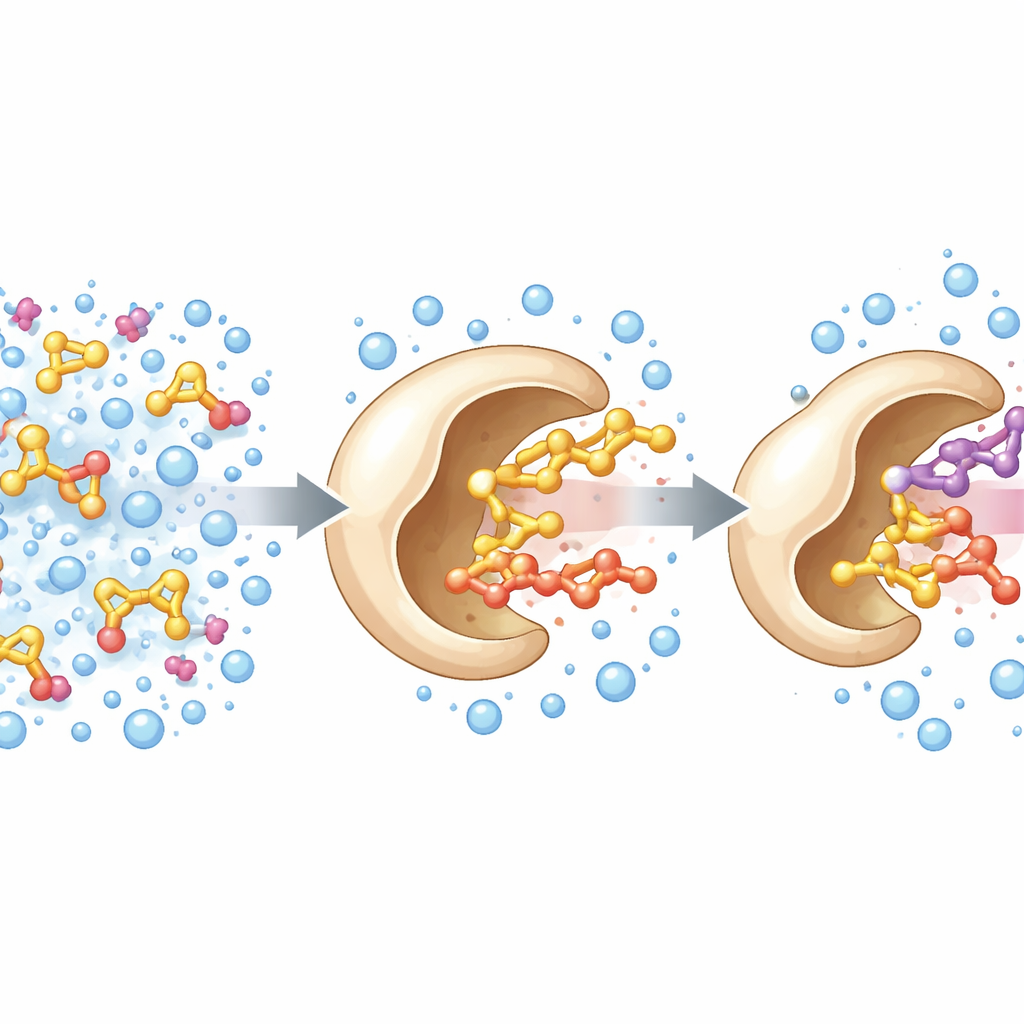
Die Forschenden begannen mit einem bekannten Enzym, einer Alkohol‑Oxidase aus einem holzabbauenden Pilz. In der Natur nutzt dieses Enzym einen Flavin‑Cofaktor, um Elektronen von kleinen Alkoholen wie Methanol abzuziehen. Das Team wollte das Substratspektrum erweitern, damit das Enzym auch sperrigere Alkohole verarbeiten kann, die für Feinchemikalien und Aromen relevanter sind. Anhand der dreidimensionalen Struktur des Enzyms konzentrierten sie sich auf drei Aminosäuren, die eine Art Pforte zum aktiven Zentrum bilden. Durch Randomisierung dieser Positionen und Screening der Varianten entdeckten sie einen Dreifachmutanten — PcAOx‑VPN genannt — der größere Alkohole wie Benzylalkohol effizient umsetzt und gleichzeitig einen Großteil seiner ursprünglichen Aktivität gegenüber sehr kleinen Substraten wie Methanol einbüßt.
Unerwartetes Talent: Esterbildung in Wasser
Bei Tests von PcAOx‑VPN in Mischungen, die ölartige Substrate lösen sollten, bemerkte das Team zusätzliche Signale in ihren Analysen. Dabei handelte es sich um acetylierte Produkte: Das Enzym übertrug eine Acylgruppe von einem aktivierten Esterdonor auf Alkohole — eine Transesterifizierungsreaktion. Bemerkenswerterweise geschah dies in wässriger Pufferlösung, wo üblicherweise starke konkurrierende Hydrolyse zu erwarten ist, bei der Wasser den Ester angreift und zerstört. PcAOx‑VPN verband Alkohol und Acylspender wie Vinylacetat effizient zu neuen Estern, oft mit Ausbeuten über 80 % und nur geringen Nebenreaktionen. Dasselbe Enzym wirkte zudem auf eine breite Palette von Alkoholen — unverzweigte, aromatische, chirale und schwefelhaltige — und zeigte in mehreren Fällen eine deutliche Bevorzugung einer Enantiomerenform.
Wasser aus dem Weg halten
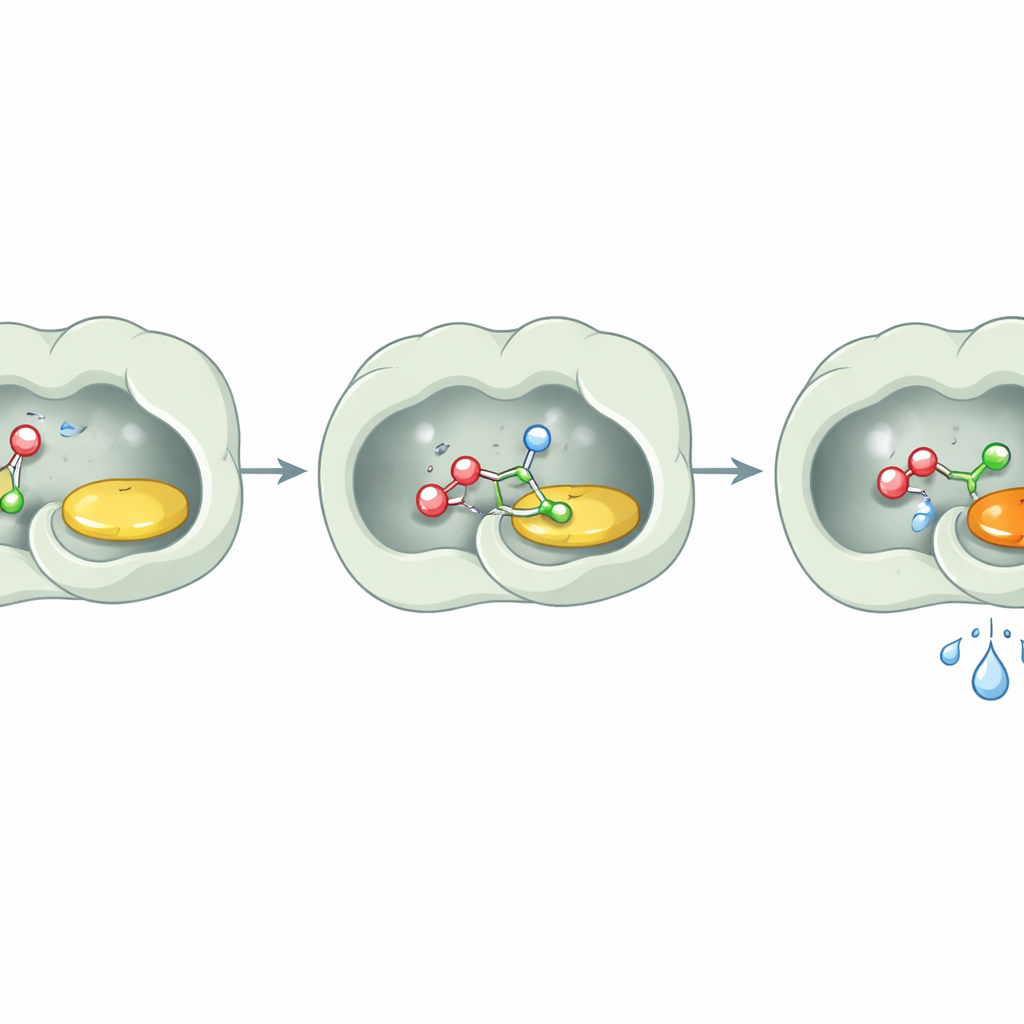
Eine zentrale Überraschung war, was das Enzym nicht tat: Es hydrolysierte Ester nicht nennenswert. Selbst nach langen Inkubationen mit Estersubstraten in Wasser blieben diese im Wesentlichen unverändert, sofern kein zusätzlicher Acylspender zugefügt wurde. Strukturelle Untersuchungen liefern eine einfache Erklärung: Das aktive Zentrum ist von überwiegend ölig‑aromatischen Aminosäuren umgeben, die eine stark hydrophobe Tasche erzeugen. Detaillierte Analysen zeigten keine Wassermoleküle in Nähe des Flavins, und rechnerische Werkzeuge bestätigten, dass auch der Kanal zum aktiven Zentrum wasserabweisend ist. Im Grunde schafft das Enzym einen winzigen trockenen Raum in einer wässrigen Umgebung. Alkohole und aktivierte Ester können eintreten und reagieren, während Wassermoleküle ferngehalten werden und somit nicht die Möglichkeit bekommen, das Produkt zu zerstören.
Wie die Reaktion vermutlich im Inneren abläuft
Mechanistische Experimente und Mutationsanalysen zeigten, dass zwei Aminosäuren — ein Histidin und eine Asparagin — sowohl für die natürliche Oxidationsfunktion des Enzyms als auch für seine neue Transesterifizierungsfähigkeit zentral sind. Das Histidin wirkt als Base, hilft, ein Proton vom eintretenden Alkohol abzuziehen und macht ihn reaktiver, während die Asparagin den resultierenden geladenen Zustand stabilisiert. Zusammen fördern sie den Nukleophilangriff des Alkohols auf den Acylspender und bilden ein kurzlebiges Intermediat, das in den gewünschten Ester umschlägt. Der oxidierte Zustand des Flavin‑Cofaktors ist ebenfalls erforderlich: Unter sauerstofffreien Bedingungen, wenn das Flavin reduziert wird, stoppt die Transesterifizierung und setzt erst nach Wiedereinführung von Luft wieder ein. Bemerkenswert ist, dass sich bei Einbringen desselben Mutations‑Trios in verwandte Oxidasen anderer Pilze ebenfalls robuste Transesterifizierungsaktivität einstellte — ein Hinweis darauf, dass sich dieses Verhalten verallgemeinern lässt.
Was das für grünere Chemie bedeutet
Für Nicht‑Fachleute lautet die Hauptbotschaft: Die Autorinnen und Autoren haben einem bekannten Enzym eine neue Fähigkeit beigebracht — nützliche Ester direkt in Wasser zu bauen und dabei die Neigung des Wassers, die Produkte wieder zu zerstören, praktisch zu ignorieren. Indem sie eine trockene, ölfreundliche Tasche im Inneren des Proteins formten und wenige Schlüsselaminos optimierten, schufen sie einen Katalysator, der Alkohole gegenüber Wasser als Reaktionspartner bevorzugt. Da das gleiche Designprinzip auch bei verwandten Enzymen funktioniert, könnte sich dieser Ansatz auf eine ganze Familie von Katalysatoren ausdehnen, die Aromen, Duftstoffe, Feinchemikalien und möglicherweise Biokraftstoffe in sichereren, nachhaltigeren Prozessen herstellen — mit weniger aggressiven organischen Lösungsmitteln und mehr Einsatz von Wasser.
Zitation: Wu, B., Ma, Y., Feng, C. et al. Engineered alcohol oxidases catalyse transesterification in aqueous media without competing hydrolysis. Nat Commun 17, 2183 (2026). https://doi.org/10.1038/s41467-026-68899-y
Schlüsselwörter: Enzymengineering, Biokatalyse, Grüne Chemie, Estersynthese, Flavoproteine