Clear Sky Science · de
Ein lattice‑sauerstofffreies Design für effiziente und stabile photothermische Methan‑Trockenreformierung
Treibhausgase in nützlichen Brennstoff verwandeln
Methan und Kohlendioxid gehören zu den stärksten Treibhausgasen, die unseren Planeten erwärmen, sind aber zugleich reich an chemischer Energie. Diese Studie zeigt, wie sorgfältig entwickelte winzige Metallpartikel Licht und Wärme gemeinsam nutzen können, um diese Gase in Syngas — eine vielseitige Mischung aus Wasserstoff und Kohlenmonoxid — umzuwandeln, und dabei die üblichen Probleme vermeiden, die solche Prozesse ineffizient und kurzlebig machen.
Warum die Methan‑Reinigung so schwer ist
Die Trockenreformierung von Methan ist eine Reaktion, die Methan und Kohlendioxid in Syngas überführt. In der Industrie verlangt sie normalerweise ofenähnliche Temperaturen von 700–1000 °C, um schnell genug abzulaufen. Bei diesen Temperaturen neigen gebräuchliche Nickel‑ und Kobalt‑Katalysatoren zum Zusammenklumpen und zur Ablagerung von Kohlenstoff, wodurch ihre Aktivität mit der Zeit verloren geht. Jüngste „photothermische“ Ansätze zielen darauf ab, konzentriertes Licht einzusetzen, um Katalysatoren schonender zu erhitzen und zusätzliche elektronische Effekte zu nutzen, doch die aktuellen Materialien verschwenden den Großteil des einfallenden Lichts und leiden weiterhin unter Kohlenstoffablagerungen und Katalysatorschäden.
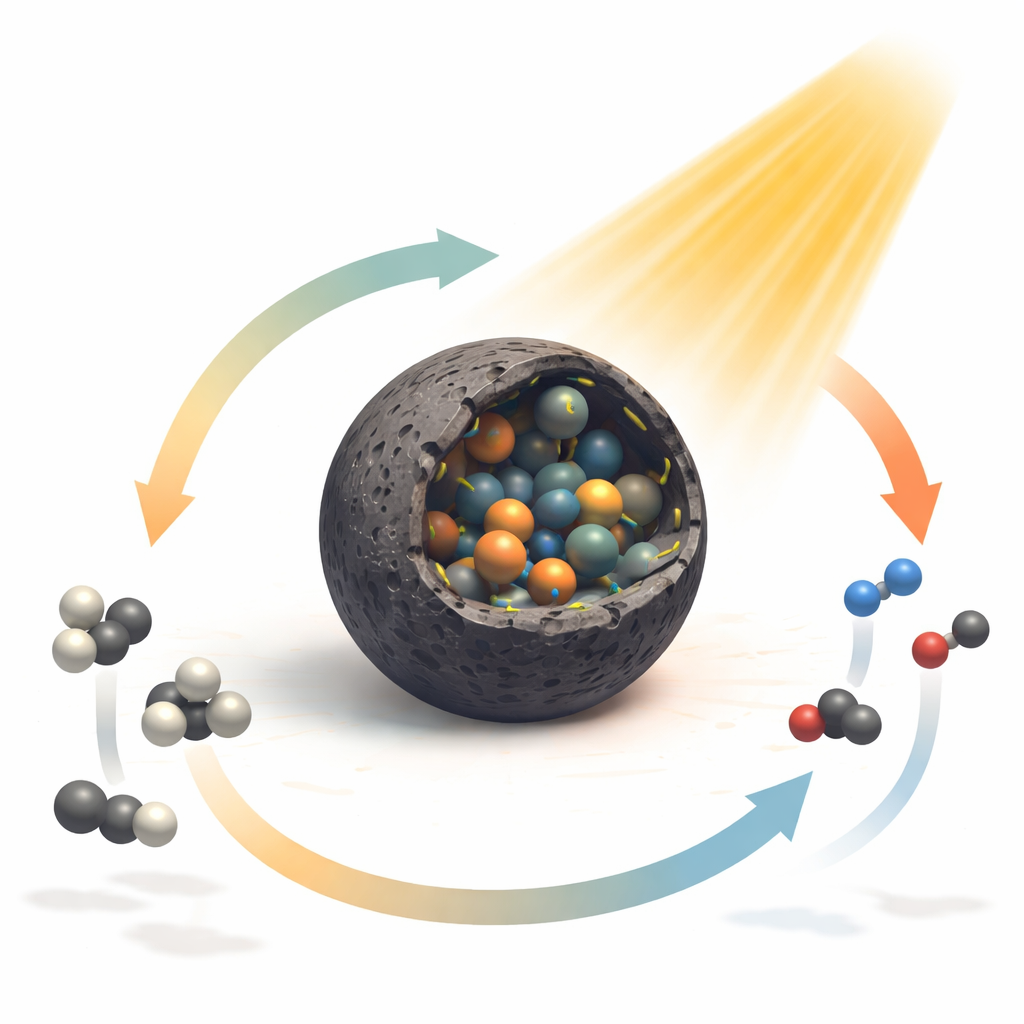
Entwurf einer neuen Art von Katalysatorschale
Die Forschenden gingen dieses Problem an, indem sie einen Katalysator aus einem Metall‑organischen Gerüst bauten — einem kristallinen Gerüst, das Metallatome und organische Linker in einem regelmäßigen Muster anordnet. Nach einer maßgeschneiderten Wärmebehandlung verwandelt sich dieses Gerüst in kugelförmige Partikel, die mit einer dünnen Schicht graphitischen Kohlenstoffs überzogen sind, in deren Innerem sehr kleine Nickel‑Kobalt‑Legierungsnanopartikel sitzen. Entscheidenderweise sind Stickstoffatome in die Kohlenstoffschale eingebettet und mit Nickel verknüpft, wodurch die Autoren sogenannte C–N–Ni‑Stellen beschreiben. Diese Stickstoff‑Nickel‑Verbindungen verändern, wie Elektronen zwischen Nickel und Kobalt sowie zwischen den Metallen und der Kohlenstoffschicht geteilt werden, belasten das Kristallgitter leicht und verwandeln die Oberfläche in eine reaktionsfreudigere Fläche für eintreffende Moleküle.
Reaktiven Sauerstoff die Arbeit übernehmen lassen
Bei traditionellen Katalysatoren für diese Reaktion spielt in das Festkörpergitter eingebauter Sauerstoff eine Schlüsselrolle beim Aufbrechen der starken C–H‑Bindungen des Methans und beim Abbau von Kohlenstofffragmenten. Gittersauerstoff ist jedoch schwer beweglich, und sein übermäßiger Verbrauch schädigt den Katalysator auf Dauer. Hier entwickelten die Forschenden einen völlig anderen Weg: Anstatt sich auf eingebauten Sauerstoff zu stützen, nutzen sie hochreaktive Sauerstoff‑ und Hydroxylspezies, die direkt aus Kohlendioxid während der Reaktion gebildet werden. Experimente und Computersimulationen zeigen, dass die stickstoffmodifizierte Nickel‑Kobalt‑Oberfläche sowohl Methan als auch Kohlendioxid stark anzieht, sie aber zu unterschiedlichen Metallatomen lenkt — Nickel spezialisiert sich auf das Spalten von Methan, während Kobalt die Aktivierung von Kohlendioxid übernimmt. Die aus Kohlendioxid gebildeten reaktiven Sauerstoffspezies oxidieren dann schnell kohlenstoffreiche Fragmente aus Methan zu Zwischenprodukten wie Formaldehyd und schließlich zu Kohlenmonoxid und Kohlendioxid, wodurch sich feste Kohlenstoffablagerungen gar nicht erst ansammeln.
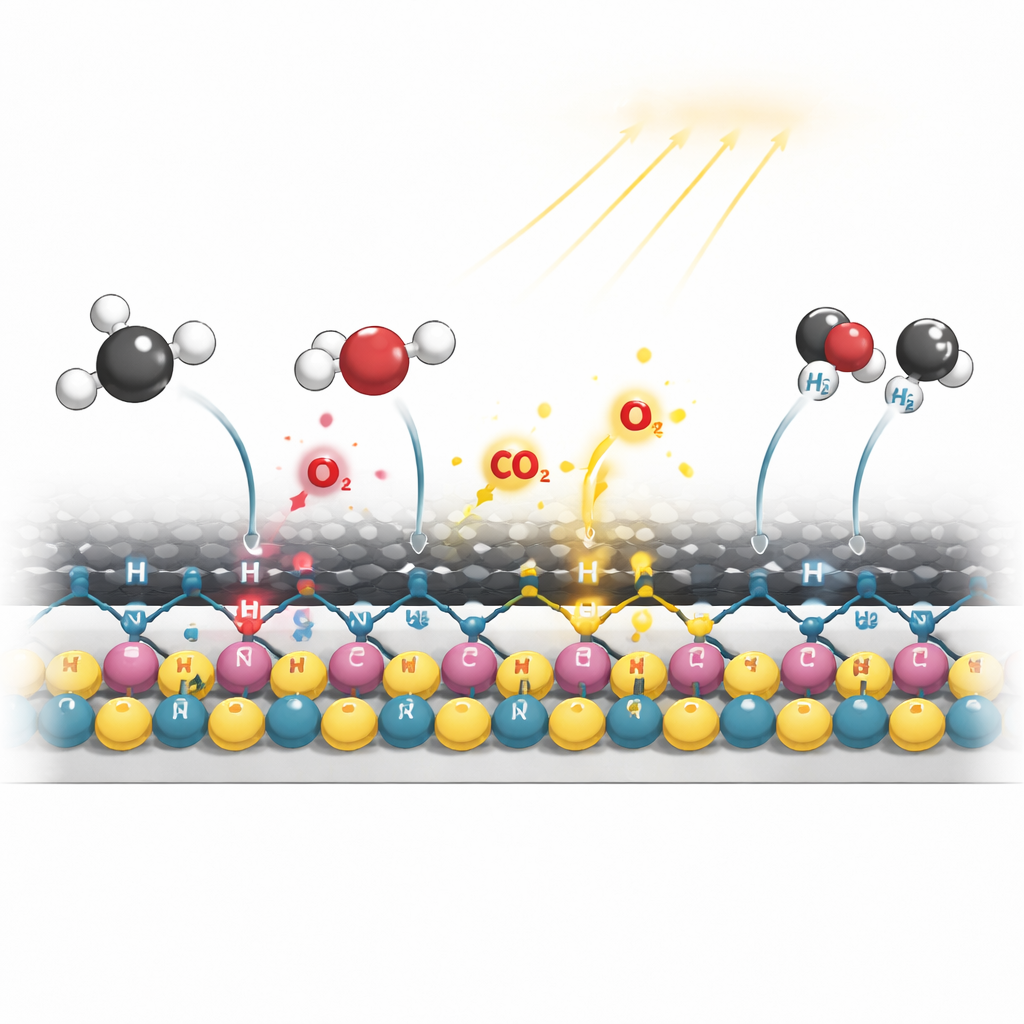
Wie Licht den Katalysator intelligenter macht
Mithilfe in situ‑Spektroskopie beobachteten die Autorinnen und Autoren, was mit dem Katalysator geschieht, während er unter dunklen und beleuchteten Bedingungen arbeitet. Ohne Licht neigen die Nickel‑ und Kobaltoberflächen zur Oxidation, und Nebenreaktionen, die Wasser bilden, werden auffälliger, wodurch die Leistung allmählich nachlässt. Unter Licht dagegen werden in der Kohlenstoffbeschichtung angeregte Elektronen entlang der C–N–Ni‑Wege zu den Metallstellen geleitet. Diese zusätzliche Elektronendichte hilft, Nickel und Kobalt in ihrem metallischen, aktiven Zustand zu halten, unterdrückt unerwünschte Nebenreaktionen und stärkt die Bildung wichtiger Zwischenprodukte wie einer oberflächengebundenen COOH‑Spezies, die in Kohlenmonoxid und Hydroxylradikale zerfällt, ohne das Metall anzugreifen. Detaillierte quantenchemische Berechnungen bestätigen, dass dieser lichtunterstützte Pfad die Energiebarrieren für die Methan‑Dehydrierung und die Oxidation von Kohlenstofffragmenten senkt, während er die Barriere für den Schritt erhöht, der sonst hartnäckige Kohlenstoffablagerungen zurücklassen würde.
Effizienz und Stabilität unter milderen Bedingungen
Der optimierte stickstoffdotierte Katalysator, mit N1 bezeichnet, lieferte Syngas mit einem nahezu idealen Wasserstoff‑zu‑Kohlenmonoxid‑Verhältnis und erreichte eine Licht‑zu‑chemischer Energie‑Effizienz von etwa 52 Prozent — konkurrenzfähig mit oder besser als viele berichtete solarbetriebene Systeme — bei einer relativ moderaten Betriebstemperatur von 540 °C. Er hielt seine Leistung über 200 Stunden kontinuierlichen Betriebs aufrecht, mit nahezu keinen Anzeichen für Katalysatorumstrukturierung oder zusätzliche amorphe Kohlenstoffbildung. Durch das Design eines lattice‑sauerstofffreien Weges, der reaktiven Sauerstoff direkt aus Kohlendioxid nutzt und Elektronen entlang präziser Stickstoff‑Nickel‑Pfadlinien lenkt, weist diese Arbeit auf eine neue Familie langlebiger, lichtunterstützter Katalysatoren hin, die sowohl Treibhausgase recyceln als auch wertvolle Brennstoffe effizienter produzieren könnten.
Zitation: Pan, T., Xu, W., Deng, H. et al. A lattice oxygen-free design for efficient and stable photothermal methane dry reforming. Nat Commun 17, 2151 (2026). https://doi.org/10.1038/s41467-026-68898-z
Schlüsselwörter: Methan‑Trockenreformierung, photothermische Katalyse, NiCo‑Katalysator, Syngas‑Produktion, Umwandlung von Treibhausgasen