Clear Sky Science · de
Potentialabhängige Polaronbildung aktiviert TiO2 für die Wasserstoffentwicklungsreaktion
Aus rostähnlichen Materialien saubere Brennstoffproduzenten machen
Das Spalten von Wasser zu Wasserstoff als Brennstoff beruht meist auf teuren Edelmetallen. Diese Studie zeigt, dass ein verbreiteter, stabiler Oxidwerkstoff, Titandioxid (TiO2), durch simples Verstellen der angelegten elektrischen Spannung von träge zu hochaktiv geschaltet werden kann. Entscheidend ist die Bildung winziger, reversibler Ladungstaschen, sogenannter Polaronen, an der Oberfläche, die neue, effiziente Reaktionswege für die Wasserstoffbildung eröffnen.
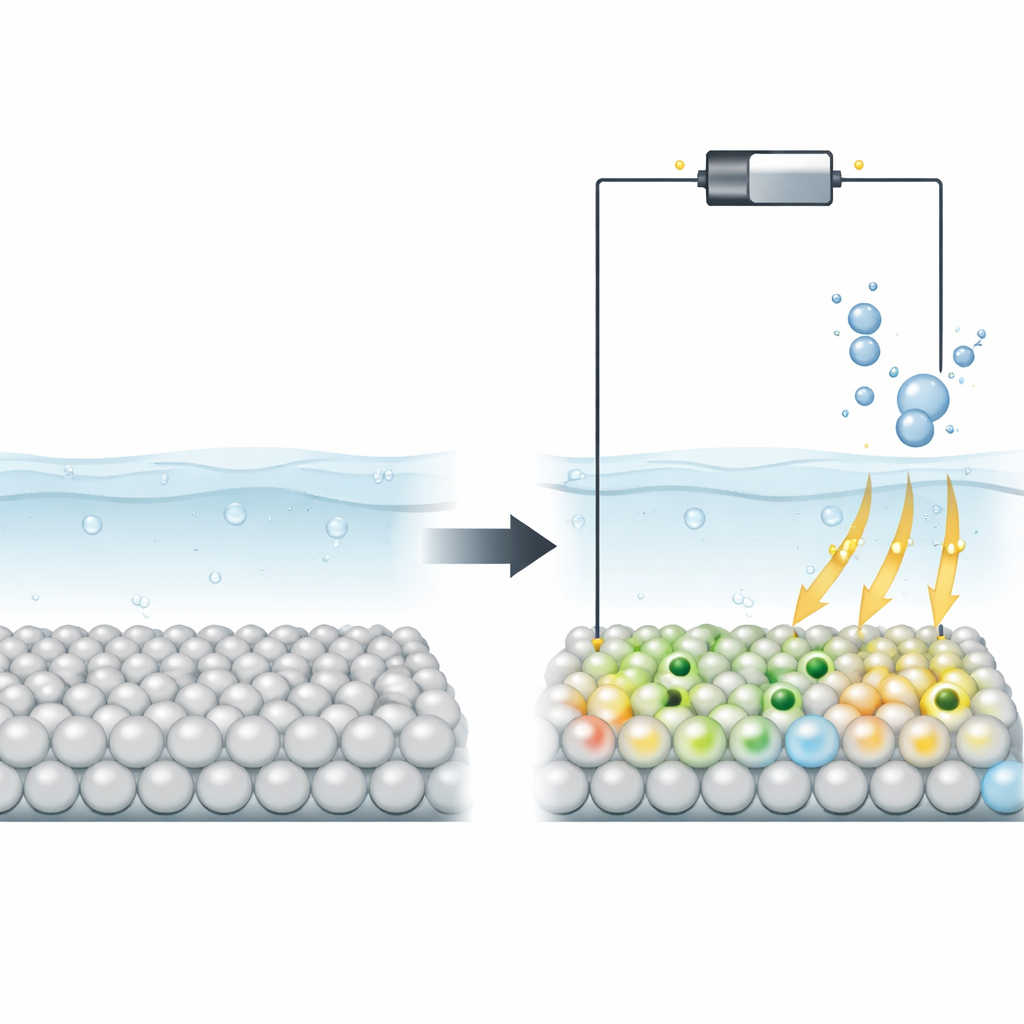
Warum Halbleiter kämpfen und wie Defekte helfen
Halbleiter wie TiO2 sind für saubere Energietechnologien attraktiv, weil sie günstig, weit verbreitet und bereits in Solar- und Photokatalyseanwendungen etabliert sind. In makelloser Form leiten sie jedoch schlecht und binden Reaktionszwischenprodukte oft entweder zu stark oder zu schwach, weshalb sie als Katalysatoren nur mäßig leistungsfähig sind. Forschende haben lange versucht, dies durch das Einbringen von Defekten — fehlende Atome oder Gitterverzerrungen — während der Synthese zu beheben. Solche dauerhaften Änderungen können die Leistung verbessern, sind aber schwer präzise zu kontrollieren, und auf atomarer Ebene war lange unklar, wie Defekte die Oberfläche so verändern, dass Reaktionen wie die Wasserstoffentwicklung beschleunigt werden.
Schaltbare Ladungstaschen mit Spannung erzeugen
Die Autorinnen und Autoren schlagen eine andere Strategie vor: die Betriebsspannung selbst zu nutzen, um die elektronische Struktur von TiO2 in Echtzeit zu formen. Bei ausreichend negativen Potentialen ändern einige Titanionen an der Oberfläche ihren Ladungszustand und fangen zusätzliche Elektronen in lokalisierten Regionen ein, den Polaronen. Mithilfe fortgeschrittener quantenmechanischer Konstantpotenzial-Rechnungen zusammen mit in situ spektroskopischen Messungen zeigt das Team, dass diese Polaronen nur unter reduzierenden Bedingungen entstehen, auf die oberste atomare Schicht beschränkt sind und beim Durchlaufen des Potentials reversibel erscheinen und verschwinden. Das bedeutet, die aktive Oberfläche des Katalysators kann während des Betriebs dynamisch eingestellt werden, statt fix während der Herstellung zu sein.
Defekte, bewegliche Ladungen und schnellere Wasserstofffreisetzung
Die Studie geht weiter und untersucht, was passiert, wenn die TiO2-Oberfläche bereits Sauerstoffvakanzstellen enthält — fehlende Sauerstoffatome, wie sie in realen Materialien häufig vorkommen. Diese Vakanzstellen begünstigen, dass zusätzliche Elektronen in der Nähe bestimmter Titanatome verweilen, wodurch sich Polaronen schon bei weniger negativen Spannungen leichter bilden. Simulationen zeigen, dass sich mehrere Polaronen zu Ketten ausrichten und zwischen benachbarten Atomen hüpfen können, was die Oberflächenleitfähigkeit stark erhöht. Experimente, die magnetische Signale und Ladungsübertrag verfolgen, bestätigen, dass defektes TiO2 mehr dieser Ladungstaschen akkumuliert und Elektronen leichter transportiert als makelloses TiO2. Infolgedessen treiben Elektroden mit Sauerstoffvakanzstellen die Wasserstoffentwicklungsreaktion bei deutlich geringeren Überpotentialen und mit deutlich höheren Strömen voran.
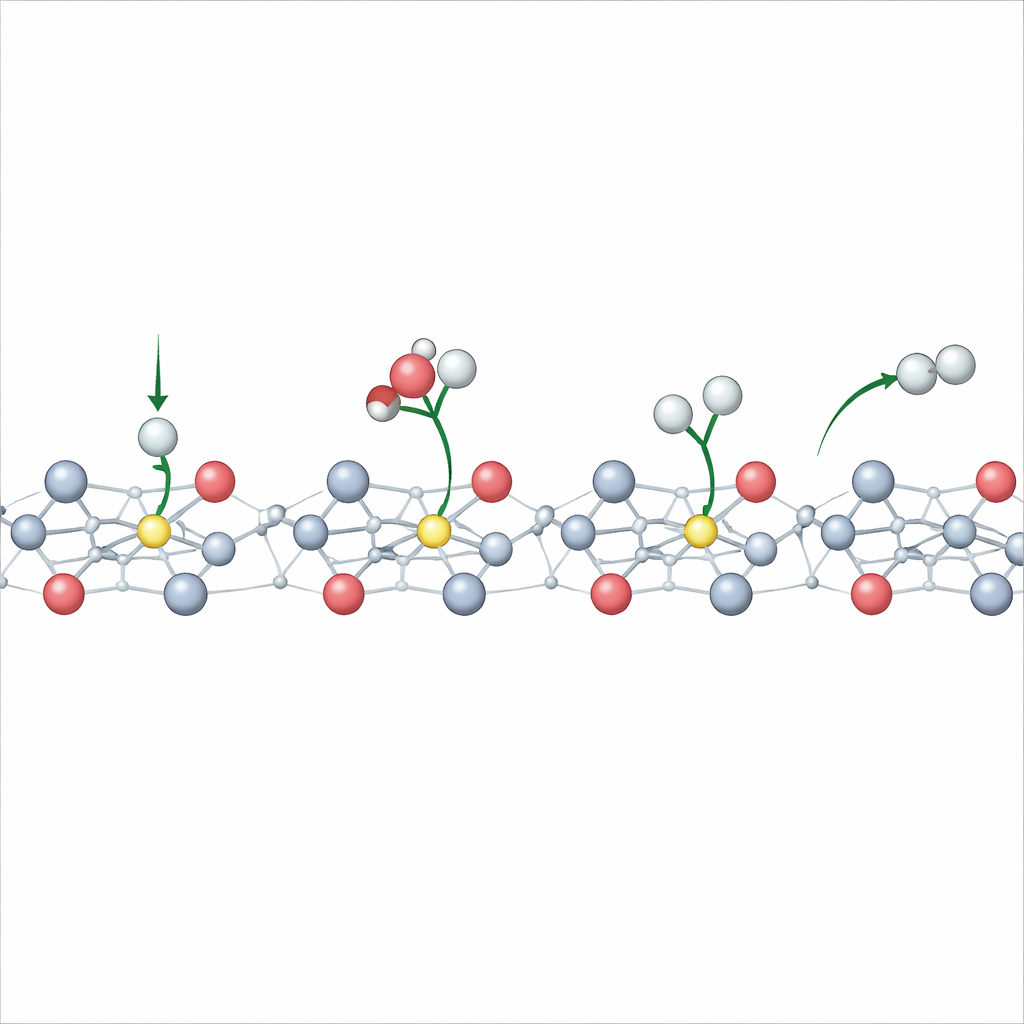
Einfachen Regeln für Reaktionsenergien neu denken
Auf Metallelektroden verlassen sich Chemikerinnen und Chemiker oft auf einfache lineare Regeln, die Reaktionsenergien, Aktivierungsbarrieren und angelegtes Potential verknüpfen. Die Autorinnen und Autoren zeigen, dass diese Regeln bei TiO2 zu versagen beginnen, sobald Polaronen ins Spiel kommen. Die Energie für die Adsorption von Wasserstoff an der Oberfläche verändert sich dann nicht mehr glatt mit dem Potential; stattdessen treten Knicke und Biegungen auf, wenn neue Polaronzustände zuschalten. Überraschenderweise gilt trotz des Scheiterns dieser einfachen Spannung–Energie-Kopplung weiterhin eine allgemeinere Beziehung, die Reaktionsbarrieren an Reaktionsenergien bindet. Das bedeutet, dass man, bei sorgfältiger Berücksichtigung wann und wo Polaronen erscheinen, weiterhin vorhersagen kann, wie schnell Wasserstoff auf diesen Halbleiteroberflächen gebildet wird.
Schlaue, einstellbare Katalysatoren entwerfen
In der Summe zeichnen die Ergebnisse das Bild von TiO2 als einem Katalysator, dessen Leistungsfähigkeit nicht allein durch seine Zusammensetzung festgelegt ist, sondern aktiv durch das Betriebspotential einstellbar ist. Durch die Kombination eingebauter Defekte wie Sauerstoffvakanzstellen mit spannungsgesteuerter Polaronbildung lässt sich die Oberfläche in ein dichtes Netzwerk hochaktiver, leitfähiger Stellen für die Wasserstoffentwicklung verwandeln. Für die interessierte Laienleserin bzw. den interessierten Laien lautet die Kernbotschaft: Günstige Halbleitermaterialien können mit Edelmetallen konkurrieren, wenn man lernt, diese winzigen Ladungstaschen während des Betriebs „einzuschalten“ und zu steuern — und so neue Wege zu effizienter, skalierbarer Wasserstoffproduktion und anderen sauberen elektrochemischen Technologien öffnet.
Zitation: Wu, T., Guo, X., Zhang, G. et al. Potential-dependent polaron formation activates TiO2 for the hydrogen evolution reaction. Nat Commun 17, 2104 (2026). https://doi.org/10.1038/s41467-026-68892-5
Schlüsselwörter: Wasserstoffentwicklungsreaktion, Titanoxid, Polaronen, Halbleiter-Elektrokatalyse, Sauerstoffvakanzstellen