Clear Sky Science · de
Hemmung der TGF-β-Signalübertragung in Mikroglia fördert die adulte Neurogenese im Hippocampus und reduziert angstähnliches Verhalten bei erwachsenen Mäusen
Warum Immunzellen im Gehirn für Stimmung und Gedächtnis wichtig sind
Die meisten von uns denken bei Immunzellen an Patrouillen im Körper, nicht daran, dass sie unsere Gedanken und Gefühle formen. Diese Studie hinterfragt diese Sichtweise, indem sie zeigt, dass Mikroglia – die Immunzellen, die im Gehirn wohnen – die Entstehung neuer Neuronen im Hippocampus, einer Region, die für Gedächtnis und Emotion wichtig ist, maßgeblich beeinflussen können. Durch das Abschalten eines spezifischen Signalwegs in Mikroglia erwachsener Mäuse steigerten die Forschenden die Produktion und das Überleben neuer Neuronen und beobachteten messbare Veränderungen im angstähnlichen Verhalten.
Die stille Kinderstube neuer Neuronen im Gehirn
Bei erwachsenen Säugetieren werden weiterhin neue Neuronen in einigen spezialisierten „Kinderstuben“ gebildet. Eine der wichtigsten ist die subgranuläre Zone des Hippocampus, die hilft, ähnliche Erinnerungen zu trennen, Lernen unterstützt und zur Stimmungskontrolle beiträgt. Unter normalen Bedingungen sterben viele dieser Neuzellen, bevor sie vollständig ausreifen. Ihre Zahl kann durch Bewegung, bereichernde Umgebungen, Stress, Schlaganfälle oder Epilepsie zunehmen oder abnehmen. Mikroglia überwachen dieses Umfeld ständig, aber ob ihr reaktiver, „entzündlicher“ Zustand die adulte Neurogenese fördert oder hemmt, war bisher unklar.
Ein zentraler Bremsmechanismus in Mikroglia ausschalten
Das Team konzentrierte sich auf ein Signalmolekül namens TGF‑beta, das Mikroglia normalerweise in einem ruhigen, homöostatischen Zustand hält. Mithilfe genetisch veränderter Mäuse schalteten sie die TGF‑beta-Signalübertragung in Mikroglia selektiv im Erwachsenenalter aus – entweder durch Entfernen des TGF‑beta‑Liganden selbst oder der Rezeptoren (ALK5 oder TβRII), die ihn wahrnehmen. Dadurch traten Mikroglia in ein reaktives, pro‑inflammatorisches Profil, ohne großflächigen Neuronenverlust zu verursachen. In diesem Zustand vermehrten sich Mikroglia und veränderten ihre Form, was auf Aktivierung hindeutet, während benachbarte Stützellen wie Astrozyten weitgehend unbeeinflusst blieben.
Mehr neue Neuronen, besseres Überleben und veränderte Angst
Wurde die TGF‑beta-Signalübertragung in Mikroglia abgeschaltet, produzierte die hippocampale Kinderstube eine Welle unreifer Neuronen, die durch das Protein DCX markiert sind. Dieser Anstieg trat etwa drei Wochen nach dem genetischen Eingriff auf und führte Wochen später zu einer anhaltenden Zunahme vollständig ausgereifter Neuronen. Die sorgfältige Verfolgung teilender Zellen zeigte, dass der Haupteffekt in einem verbesserten Überleben der Neuzellen lag, nicht nur in schnellerer Zellteilung. Die vollständige Entfernung der Mikroglia mit einem Medikament ahmierte diesen Effekt nicht nach, was darauf hindeutet, dass nicht das Fehlen der Mikroglia entscheidend ist, sondern das spezifische reaktive Profil, das durch die Abschaltung von TGF‑beta entsteht. Verhaltensmäßig verbrachten Mäuse mit TGF‑beta‑defizienten Mikroglia mehr Zeit in den offenen Armen erhöhter Labyrinthe, ein gängiges Zeichen für vermindertes angstähnliches Verhalten oder Enthemmung. Diese Veränderungen schwächten sich in einigen Modellen ab, wenn Mikroglia später wieder einen normaleren Zustand annahmen, blieben aber in anderen bestehen, in denen Mikroglia reaktiv blieben.
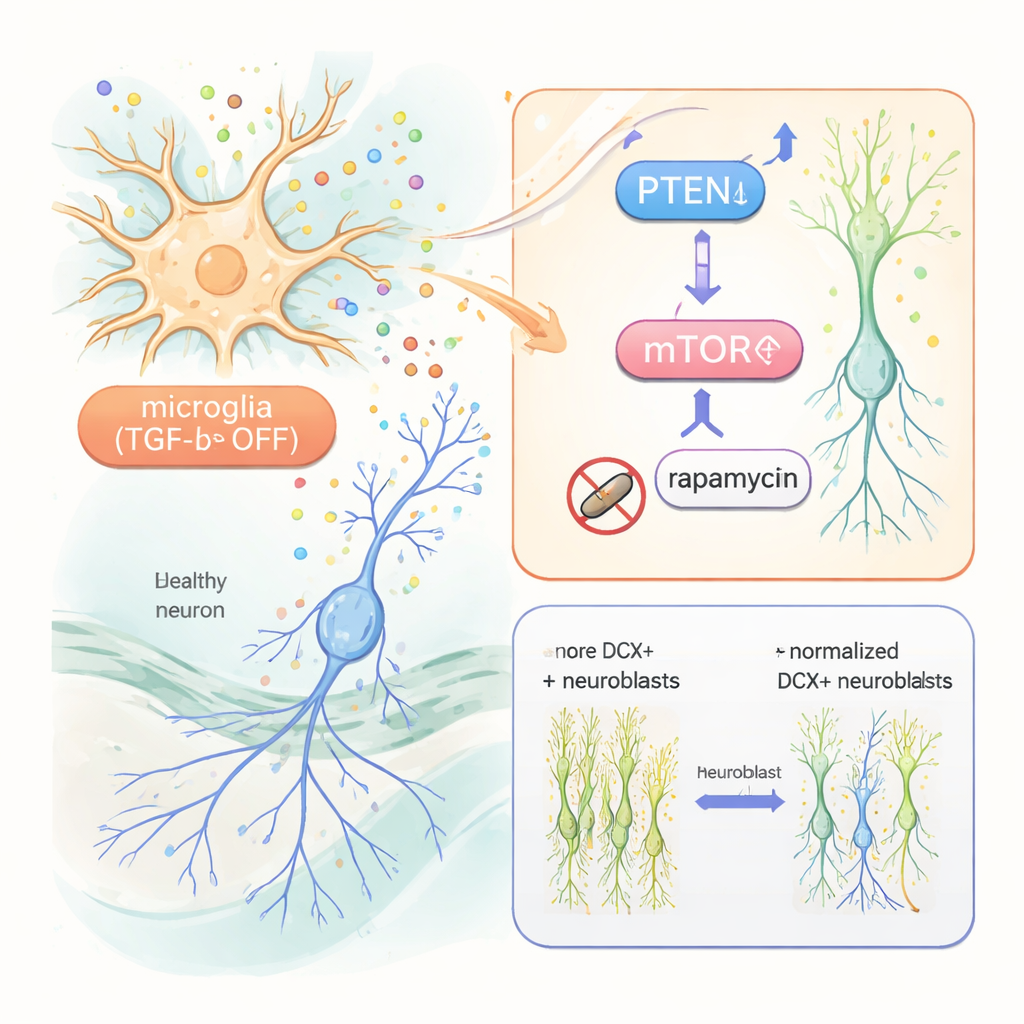
Aufspüren des Wegs in den Neuzellen
Um zu verstehen, wie veränderte Mikroglia mit Neuzellen kommunizieren, nutzten die Forschenden Einzelzell‑RNA-Sequenzierung an hippocampalen Zellen. Sie fanden umfassende Veränderungen der Genaktivität nicht nur in Mikroglia, sondern auch in unreifen Neuronen. Zentral war dabei eine Reduktion von PTEN, einem Protein, das normalerweise Zellwachstum bremst, sowie Hinweise auf eine gesteigerte Aktivität des mTOR‑Wegs, der Überleben und Wachstum fördert. Überraschenderweise erwiesen sich bekannte Wachstumsfaktoren wie IGF‑1 und TNF‑alpha, obwohl in reaktiven Mikroglia erhöht, als nicht erforderlich: Selbst wenn diese genetisch entfernt wurden, blieb die Steigerung der Neurogenese erhalten. Im Gegensatz dazu normalisierte die Behandlung der Mäuse mit Rapamycin, einem mTOR‑Blocker, die Überzahl an unreifen Neuronen und ihr übermäßiges Verzweigen. Neuzellen zeigten zudem erhöhte Werte eines downstream mTOR‑Markers, den Rapamycin verringerte.
Was das für die Gehirngesundheit bedeuten könnte
In der Summe deuten die Befunde darauf hin, dass Mikroglia bei Abschalten der TGF‑beta‑Signalübertragung einen reaktiven Zustand einnehmen, der das Überleben und die Integration neugeborener hippocampaler Neuronen über einen PTEN–mTOR‑Weg in diesen Neuronen fördert. Das steht in Verbindung mit vermindertem angstähnlichem Verhalten bei Mäusen, kann aber auch Veränderungen in Lernen und Gedächtnis mit sich bringen. Für Laien lautet die zentrale Botschaft: Die Immunzellen des Gehirns können feinsteinstellen, wie viele neue Neuronen unsere Gedächtnisschaltkreise erreichen – und eine gezielte Beeinflussung dieses Systems könnte eines Tages helfen, nützliche Neurogenese zu fördern oder schädlich übermäßig sprossende Neuronen bei Erkrankungen wie Epilepsie oder nach Hirnverletzungen einzudämmen.
Zitation: Ware, K., Peter, J., Yazell, J. et al. Inhibition of TGF-β signaling in microglia stimulates hippocampal adult neurogenesis and reduces anxiety-like behavior in adult mice. Nat Commun 17, 1440 (2026). https://doi.org/10.1038/s41467-026-68885-4
Schlüsselwörter: adulte Neurogenese, Mikroglia, Hippocampus, Angstverhalten, TGF‑beta-Signalübertragung