Clear Sky Science · de
Entdeckung des labyrinthartigen Netzwerks der Glabridin-Biosynthese
Warum Lakritze mehr bewahrt als nur süße Erinnerungen
Lakritz‑wurzel wird seit Langem in traditionellen Heilmitteln und hochwertigen Hautpflegeprodukten geschätzt wegen einer natürlichen Verbindung namens Glabridin, die für ihre antioxidativen, entzündungshemmenden und aufhellenden Eigenschaften bekannt ist. Heutzutage wird Glabridin meist durch Extraktion aus wilden Lakritzpflanzen gewonnen — ein langsamer und verschwenderischer Prozess, der empfindliche Trockenökosysteme schädigen kann. Diese Studie legt auf molekularer Ebene offen, wie Lakritze Glabridin herstellt, und zeigt, wie diese komplexe Chemie in Bäckerhefe nachgebaut werden kann, was den Weg zu einer nachhaltigeren Produktion wertvoller, pflanzenbasierter Inhaltsstoffe weist.
Von einfachen Bausteinen zu einem chemischen Labyrinth
Pflanzen produzieren eine erstaunliche Vielfalt an Flavonoiden — über 9.000 verschiedene Moleküle — aus nur wenigen grundlegenden Ausgangsverbindungen. Ein Großteil dieser Vielfalt entsteht durch „Veredelungs“-Schritte, bei denen nach dem Aufbau des Grundgerüsts kleine chemische Gruppen angehängt oder entfernt werden. Für Glabridin nutzten die Autorinnen und Autoren zunächst rechnerische Werkzeuge, um ausgehend von seiner Struktur rückwärts zu arbeiten und bekannte Enzymreaktionen zu durchsuchen. Sie kartierten alle plausiblen Wege von einer gemeinsamen Aminosäure, L‑Phenylalanin, zu Glabridin und kürzten dieses riesige Netzwerk anschließend mithilfe realer Stoffwechseldaten aus Lakritzwurzeln. Das Ergebnis war ein Labyrinth aus 13 möglichen Pfaden mit vielen Verzweigungen, was nahelegt, dass die Biosynthese von Glabridin kein einfacher linearer Fließbandprozess ist, sondern ein flexibles Netzwerk mit mehreren Routen zum gleichen Endprodukt. 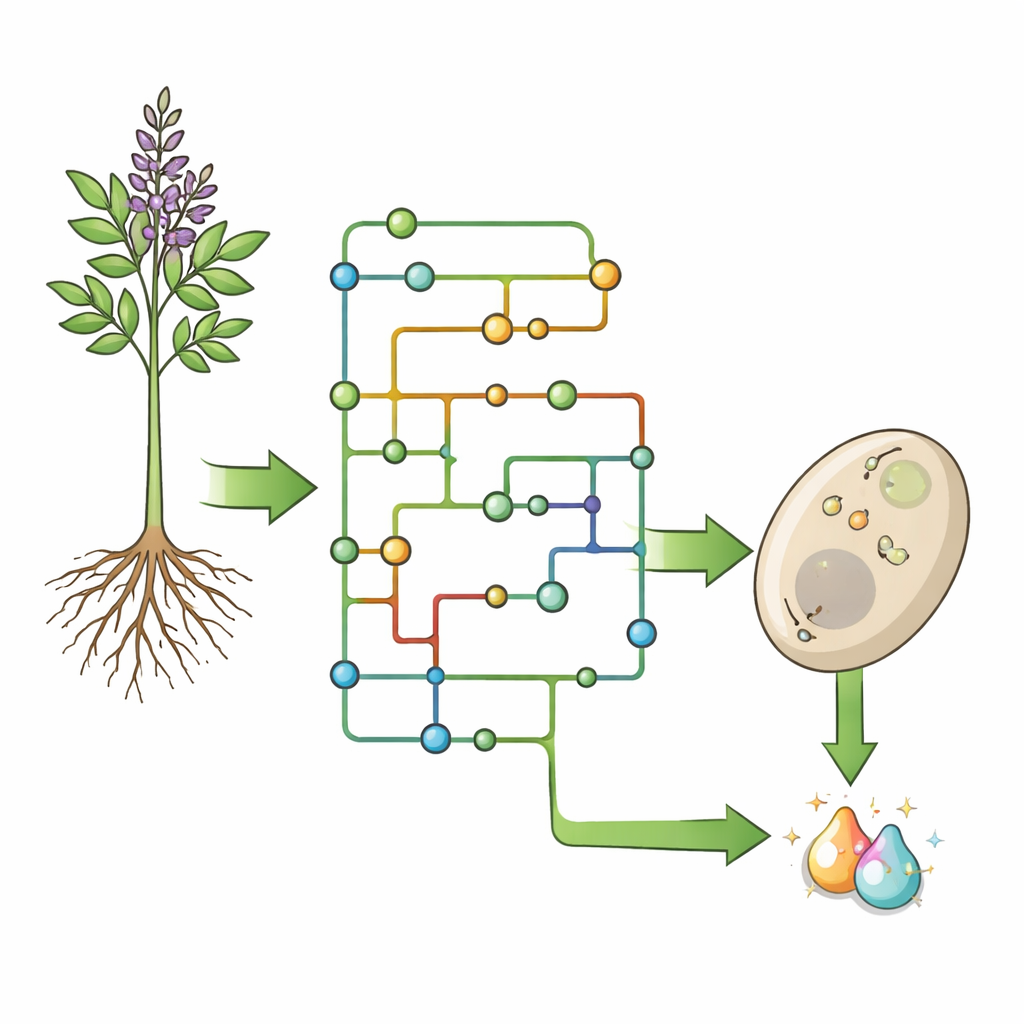
Auf der Suche nach den wichtigsten molekularen Arbeitern in Lakritze
Um herauszufinden, welche Enzyme Glabridin tatsächlich in der Pflanze aufbauen, erstellte das Team ein Chromosomen‑niveau‑Genom von Glycyrrhiza glabra und kombinierte es mit 183 Transkriptomen — Momentaufnahmen der aktiven Gene in verschiedenen Organen, Arten, Jahreszeiten und Wachstumsstadien. Durch die Kombination von Sequenzähnlichkeit, evolutionären Beziehungen und Koexpressionsmustern reduzierten sie Tausende von Genen auf ein fokussiertes Werkzeugset: sieben Kandidaten für Reduktasen, achtzehn Prenyltransferasen, neununddreißig oxidative Cyclasen und sechs Demethylasen. Viele dieser Gene sind auf bestimmten Chromosomen gehäuft und in Wurzeln am aktivsten, wo Glabridin akkumuliert. Der Vergleich dreier verwandter Lakritzarten zeigte, dass G. glabra, die wichtigste natürliche Glabridin‑Quelle, diese Schlüsselenzyme tendenziell stärker exprimiert, was mit dem deutlich höheren Glabridin‑Gehalt in ihren Wurzeln übereinstimmt.
Den Weg Reaktion für Reaktion wiederaufbauen
Die Forschenden testeten anschließend jede Kandidaten‑Enzymfunktion in Hefe und in gereinigter Form, um herauszufinden, was das Enzym tatsächlich bewirkt. Sie identifizierten eine potente Reduktase (GgPTR1), die einen Ring in einem Isoflavan‑Vorläufer öffnet, eine spezialisierte Prenyltransferase (GgPT1), die eine fettige Seitenkette anfügt, eine oxidative Cyclase (GgOC1), die einen neuen Ring schließt, und eine vielseitige Pflanzen‑Demethylase (GgDMT1), die Methylgruppen von mehreren Zwischenstufen entfernen kann. Gemeinsam wandeln diese vier Schritte den Pterocarpan Medicarpin über mehrere miteinander verknüpfte Routen in Glabridin um. Ein auffälliges Merkmal des Netzwerks ist ein wiederkehrender „Schutz–Entschutz“-Zyklus: Methylierung lenkt reaktive Zwischenstufen in effiziente Bahnen und verbessert deren Kompatibilität mit Enzymen, und spätere Demethylierung stellt die finale aktive Form wieder her. Räumliche Trennung innerhalb der Zelle — einige Enzyme im endoplasmatischen Retikulum, andere im Cytoplasma — sowie saisonale Verschiebungen in der Genaktivität stimmen außerdem ab, wann und wo jeder Schritt stattfindet.
Hefe zu einer kleinen Lakritz‑Fabrik machen
Mit diesem Enzymset rüstete das Team Bäckerhefe so aus, dass sie Glabridin aus einfachem Zucker herstellen kann. Zunächst bauten sie ein „Kernmodul“ aus vierzehn Enzymen, das Glucose in Medicarpin, das zentrale Gerüst, umwandelt. Anschließend fügten sie ein „Veredelungsmodul“ mit der Lakritz‑Reduktase, Prenyltransferase und Oxidase hinzu sowie entweder die pflanzliche Demethylase GgDMT1 oder eine Pilz‑Demethylase NhPDA1. Anstatt einen einzigen starren Weg vorzuschreiben, nutzten sie Enzym‑Promiskuität — die Fähigkeit, auf mehrere Zwischenstufen zu wirken — und schufen so ein leiterartiges Netzwerk paralleler Zweige. Experimente und Computermodelle zeigten, dass dieses Mehrwege‑Design robuster und produktiver ist als ein vereinfachter Einlinien‑Pfad, teilweise weil es den Verlust von Zwischenprodukten verringert, die sonst aus der Zelle entweichen würden.
Was das für Hautpflege und nachhaltige Chemie bedeutet
Indem die Autorinnen und Autoren das biosynthetische Labyrinth von Glabridin vollständig aufkartierten und in Hefe nachbauten, liefern sie einen Bauplan, um diesen hochpreisigen kosmetischen Inhaltsstoff zu produzieren, ohne große Mengen wild wachsender Lakritze zu entwurzeln. Ihre Arbeit zeigt außerdem ein allgemeineres Prinzip: Pflanzenwege zur Herstellung spezialisierter Moleküle beruhen möglicherweise auf reversiblen „Ein–Aus“-chemischen Verzierungen und redundanten Verzweigungen, um flexibel und widerstandsfähig zu bleiben. Die Nutzung solcher labyrinthartiger Netzwerke in Mikroben könnte die Produktion nicht nur von Glabridin, sondern auch vieler anderer komplexer pflanzlicher Naturstoffe erleichtern, um eine umweltfreundlichere Fertigung zu unterstützen und den Druck auf gefährdete Pflanzenarten zu verringern. 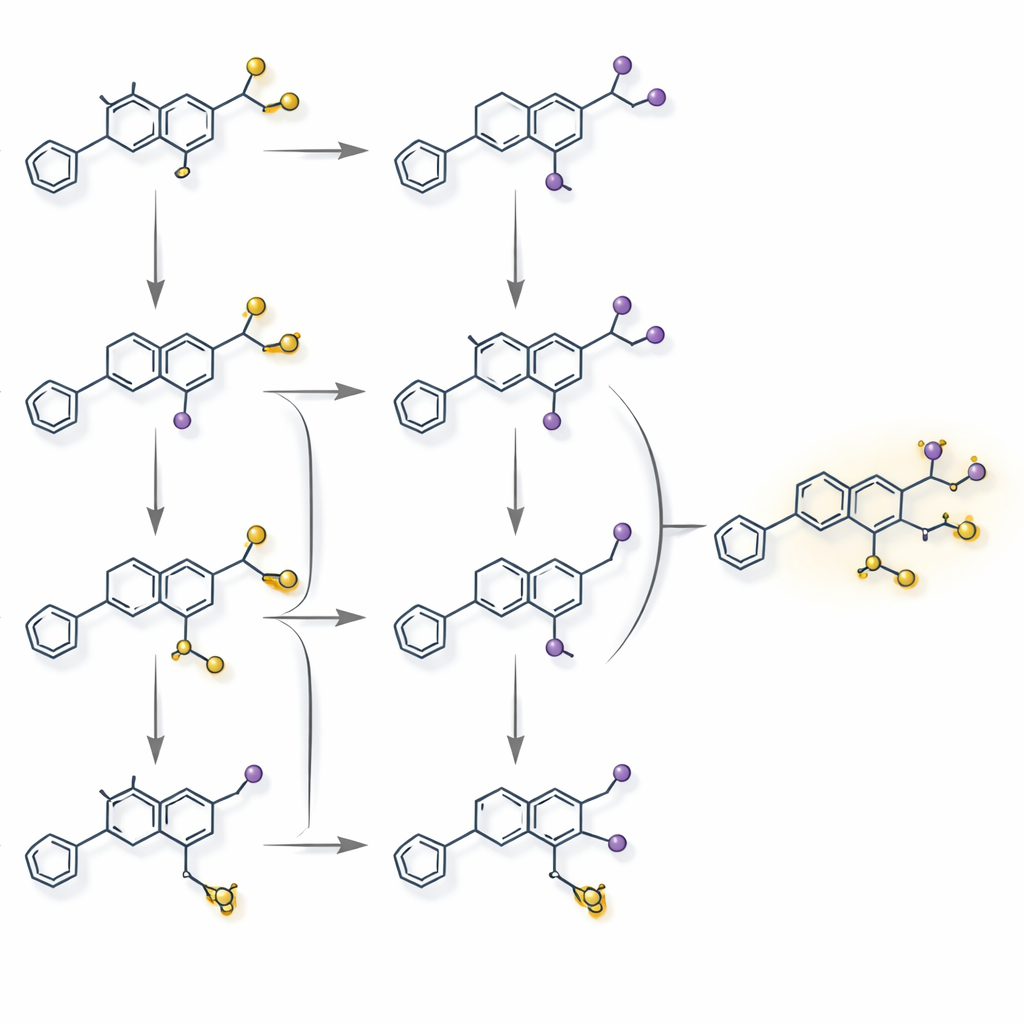
Zitation: Zhang, Z., Li, W., Meng, F. et al. Discover the maze-like network for glabridin biosynthesis. Nat Commun 17, 2215 (2026). https://doi.org/10.1038/s41467-026-68881-8
Schlüsselwörter: glabridin, lakritze, mikrobielle Biosynthese, metabolisches Engineering, Flavonoide