Clear Sky Science · de
Charakterisierung von Verarbeitungsbedingungen, die die Transkriptome menschlichen Gehirngewebes artefaktisch verzerren
Warum die Handhabung des Gehirns nach dem Tod wichtig ist
Viele der wichtigsten Erkenntnisse zu Alzheimer, Parkinson und anderen Hirnerkrankungen stammen aus der Untersuchung von Hirngewebe, das nach dem Tod gespendet wurde. Doch die Art und Weise, wie dieses Gewebe in den Stunden nach dem Tod behandelt wird, kann subtil — und manchmal dramatisch — verändern, welche Gene als aktiv erscheinen. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Wenn wir die molekularen „Botschaften“ im Autopsiegewebe lesen, wie viel von dem, was wir sehen, spiegelt die Biologie der Person wider und wie viel ist eine Nebenwirkung von Zeit und Temperatur nach dem Tod?
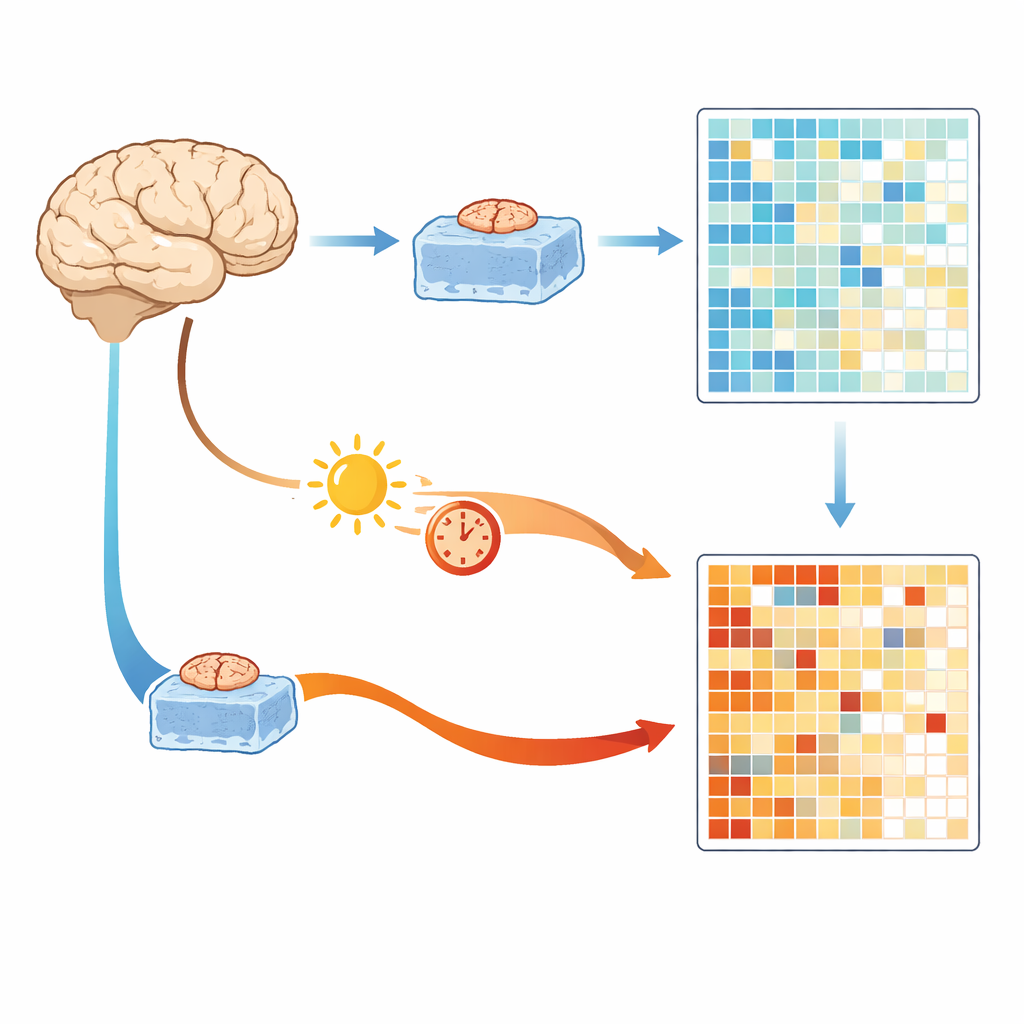
Vergleich von schnell eingefrorenem OP-Gewebe mit Autopsiegewebe
Die Forschenden begannen mit einem seltenen Vorteil: Zugang zu kleinen Stücken gesund aussehenden Hirngewebes, das während Tumoroperationen entnommen und innerhalb von etwa einer halben Stunde gekühlt und eingefroren werden kann. Diese Proben liefern eine nahe Momentaufnahme der Genaktivität im lebenden Gehirn. Das Team verglich sie mit Hirngewebe aus großen Autopsiebanken, das nach entweder kurzer Verzögerung von etwa sechs Stunden oder langer Verzögerung von etwa 36 Stunden gesammelt wurde. Alle Proben wurden auf dieselbe Weise aufbereitet und sequenziert, um technische Unterschiede zu vermeiden. Über Tausende von Genen hinweg war der wichtigste Trennfaktor nicht das Alter oder Geschlecht der Spender, sondern ob das Gewebe aus schnell eingefrorenen OP-Proben oder verzögerten Autopsieproben stammte.
Verborgene Stresssignale und das Auftreten von Artefaktgenen
Sowohl kurz- als auch langverzögerte Autopsieproben zeigten im Vergleich zum unmittelbar eingefrorenen OP-Gewebe starke Veränderungen der Genaktivität. Viele der erhöhten Gene standen im Zusammenhang mit Stressreaktionen, Energieproduktion in den Mitochondrien und Entzündungswegen. Die Autorinnen und Autoren bezeichnen diesen gemeinsamen Gencluster als „Brain Artifact Genes“ oder BAGs, weil sie offenbar durch Bedingungen nach dem Tod und nicht durch die Krankheit selbst aktiviert werden. Selbst eine relativ kurze Verzögerung von sechs Stunden reichte aus, um Tausende von Änderungen hervorzurufen, darunter Gene, die an der Kommunikation zwischen Nervenzellen beteiligt sind. Das legt nahe, dass einige scheinbare „Krankheitssignale“ in früheren Studien teilweise widerspiegeln könnten, wie lange das Gehirn vor der Konservierung gelegen hat.
Untersuchung der Rollen von Zeit, Temperatur und Zelltyp
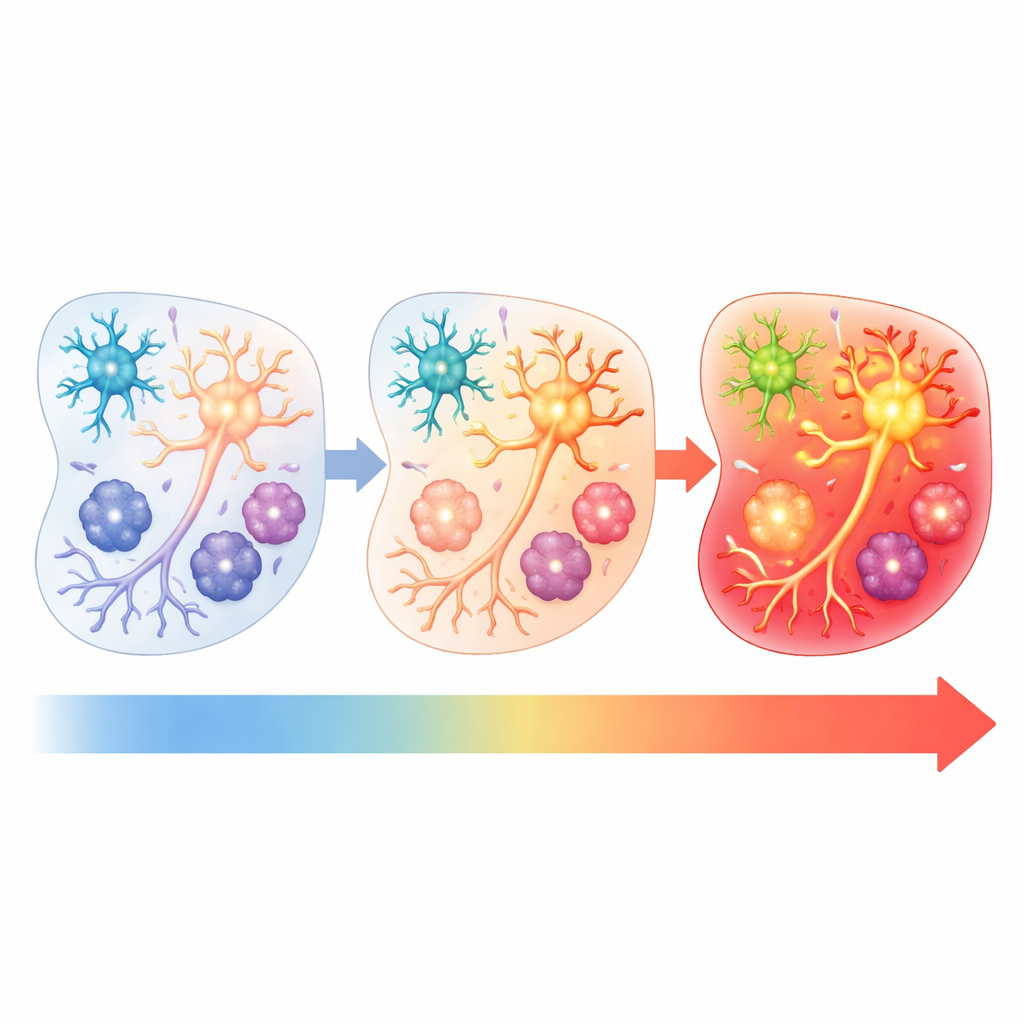
Um zu klären, welche postmortalen Faktoren am wichtigsten sind, hielten die Forschenden Stücke des OP-geheriten Gewebes gezielt entweder bei Kühlschranktemperatur oder Raumtemperatur für unterschiedliche Zeitspannen, bevor sie sie einfrieren ließen. Anschließend maßen sie erneut die Genaktivität. Gewebe, das kurz im Kühlschrank gelagert wurde, ähnelte am meisten den sofort eingefrorenen Proben, während längere Zeiten und höhere Temperaturen eine stärkere und weiter verbreitete BAG-Aktivierung verursachten. Durch die Analyse einzelner Zellkerne fanden die Forschenden außerdem heraus, dass verschiedene Hirnzelltypen in unterschiedlichen Stadien reagierten: Glutamaterge Neurone waren die frühesten „Responder“ nach mehreren Stunden bei Raumtemperatur, während Oligodendrozyten und Mikroglia die stärksten Artefaktsignaturen nach etwa einem Tag zeigten. Das bedeutet, dass Messungen spezifischer Zellpopulationen zeitabhängig verzerrt sein können.
Aufbau eines molekularen Qualitätswerts mit maschinellem Lernen
Da keine Gehirnbank alle Details der postmortalen Handhabung perfekt kontrollieren kann, wandten sich die Autorinnen und Autoren dem maschinellen Lernen zu, um ein praktisches Qualitätsprüfungswerkzeug zu entwickeln. Anhand von Genaktivitätsmustern aus Gewebe, das bekannten Kombinationen aus Zeit und Temperatur ausgesetzt war, trainierten sie ein Modell, drei grobe „Domänen“ von Verarbeitungsbedingungen zu erkennen. Aus Tausenden von Genen destillierte das Modell eine kleinere Signatur, die sie TTRUTH nennen (Time and Temperature Response genes Underlying Transcriptional Heterogeneity). Der resultierende TTRUTH-Score schätzt, wie stark eine gegebene Gehirnprobe zeit- und temperaturbedingte Artefakte trägt. Bei Anwendung auf mehrere unabhängige Autopsie-Datensätze aus anderen Studien fielen die meisten Proben in eine Domäne, die mit moderater Artefaktbelastung vereinbar ist, während eine Minderheit Muster zeigte, die eher idealer Handhabung oder starkem Stress ähneln — ein Hinweis auf reale Variabilität zwischen Spendern und Zentren.
Was das für die Hirnforschung bedeutet
Für Nichtfachleute lautet die Kernbotschaft: Hirngewebe „erinnert“ sich daran, wie es nach dem Tod behandelt wurde, und diese Erinnerungen können sich als Krankheitssignale ausgeben. Diese Arbeit liefert eine Roadmap und ein offen verfügbares Online-Tool, mit dem Forschende ihre eigenen Datensätze auf versteckte Handhabungseffekte prüfen, biologische Signale von technischem Rauschen unterscheiden und Proben besser für die Analyse gruppieren können. Indem diese Artefakte erkannt und korrigiert werden, können Wissenschaftlerinnen und Wissenschaftler letztlich verlässlichere Schlussfolgerungen darüber ziehen, wie das menschliche Gehirn in Gesundheit und Krankheit funktioniert — und mit größerer Zuversicht Fortschritte bei neuen Behandlungen erzielen.
Zitation: Yaqubi, M., Thomas, M., Talbot-Martin, J. et al. Characterising processing conditions that artifactually bias human brain tissue transcriptomes. Nat Commun 17, 2848 (2026). https://doi.org/10.1038/s41467-026-68872-9
Schlüsselwörter: Gehirn-Biobanken, postmortales Gewebe, Genexpression, RNA-Sequenzierung, maschinelles Lernen