Clear Sky Science · de
Anti-TLR2-Immuntherapie moduliert die neuron-zu-Oligodendrozyten-Ausbreitung von α-Synuclein in Maus- und Humanmodellen
Warum diese Forschung wichtig ist
Die multiple Systematrophie (MSA) ist eine seltene, aber rasch fortschreitende Gehirnerkrankung, die Parkinson-ähnliche Bewegungsstörungen mit Gleichgewichts- und autonomen Ausfällen, etwa Blutdruckabfällen, verbindet. Ärztinnen und Ärzte können Symptome lindern, derzeit aber die Krankheit selbst nicht verlangsamen. Diese Studie enthüllt, wie ein fehlgefaltetes Protein zwischen Gehirnzellen verbreitet wird und die „Isolierung der Verdrahtung“ des Gehirns schädigt, und zeigt, dass eine gezielte Antikörperbehandlung diesen Prozess in Tier- und Zellmodellen unterbrechen kann. Die Arbeit verweist auf eine konkrete, medikamentenähnliche Strategie, die eines Tages den Verlauf der MSA ändern könnte, statt nur ihre Symptome zu behandeln.
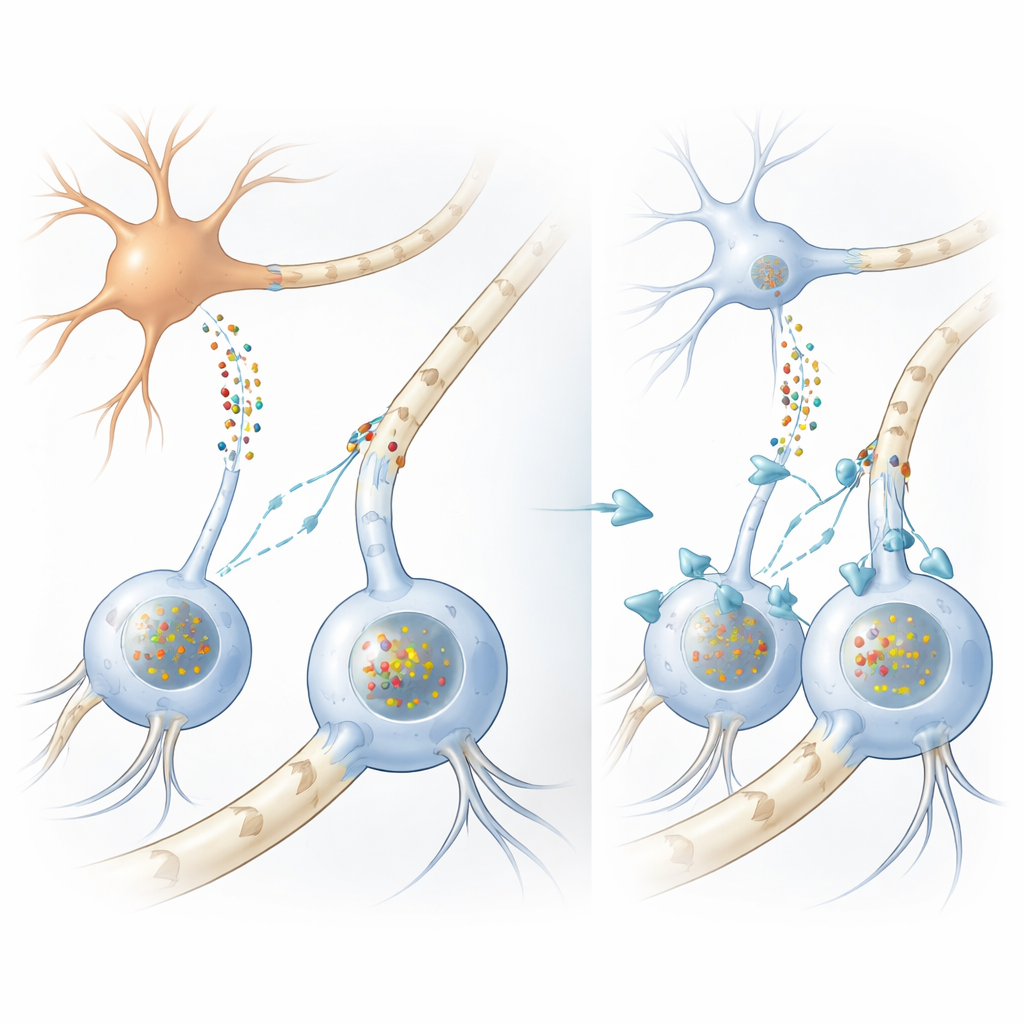
Wie die Gehirnverdrahtung fehlgeht
Bei vielen Bewegungsstörungen, einschließlich der Parkinson-Krankheit, sammeln sich Aggregate eines Proteins namens Alpha-Synuclein in Nervenzellen an. Bei MSA bilden sich jedoch besonders auffällige Aggregate in Stützzellen, den Oligodendrozyten, die normalerweise Nervenfasern mit fetthaltigen Myelinscheiden umhüllen und so die Weiterleitung elektrischer Signale beschleunigen. Merkwürdigerweise produzieren Oligodendrozyten selbst sehr wenig Alpha-Synuclein, was ein lange bestehendes Rätsel aufwirft: Woher stammen die massiven Proteinablagerungen in diesen Zellen? Die Autorinnen und Autoren bestätigten zunächst mit menschlichen Gehirnproben und umfangreichen RNA-Analysen, dass Oligodendrozyten tatsächlich deutlich weniger Alpha-Synuclein herstellen als Neurone, und stützten damit die Idee, dass das schädliche Protein von außen kommt.
Protein von Neuron zu Stützzelle übertragen
Um das zu prüfen, entwickelten die Forschenden mehrere ergänzende Modelle. In Zellkulturen züchteten sie aus neuralen Stammzellen menschliche, oligodendrozytenähnliche Zellen und setzten diese in Flüssigkeit, die von neuronalen Zellen gesammelt worden war und große Mengen Alpha-Synuclein freisetzte. Die Stützzellen nahmen dieses Protein auf und bildeten Aggregate, die den glialen Einschlüssen in MSA-Gehirnen stark ähnelten, einschließlich gleicher chemischer Markierungen und Helferproteine. In einer Mauslinie, die menschliches mutiertes Alpha-Synuclein ausschließlich in Neuronen produziert, fanden die Forschenden erneut menschliche Proteinaggregate in Oligodendrozyten der weißen Substanz, obwohl diese Zellen das menschliche Gen nicht exprimierten. Zusammengenommen zeigen diese Experimente, dass Alpha-Synuclein von Neuronen in Oligodendrozyten gelangen und dort krankheitsähnliche Einschlüsse bilden kann.
Das Tor auf der Zelloberfläche
Als Nächstes fragten die Wissenschaftler, wie das Protein in Oligodendrozyten eindringt. Frühere Arbeiten hatten den Immunrezeptor Toll-like receptor 2 (TLR2) auf Zelloberflächen als Andockstelle für Alpha-Synuclein in Neuronen und Mikroglia identifiziert. Beim Auswerten von Genexpressions-Datensätzen aus MSA-Gehirnen stellten die Forschenden fest, dass Oligodendrozyten von Betroffenen im Vergleich zu Kontrollen ungewöhnlich hohe TLR2-Spiegel aufwiesen und dass höhere TLR2-Werte mit niedrigeren Expressionen myelinbezogener Gene wie dem Myelin-Basisprotein verbunden waren. Diese Beziehung zeigte sich in mehreren unabhängigen Parkinson-Datensätzen nicht, was nahelegt, dass die Empfindlichkeit von Oligodendrozyten gegenüber Alpha-Synuclein über TLR2 ein charakteristisches Merkmal der MSA ist und nicht allgemein für alle Synuclein-Erkrankungen gilt.
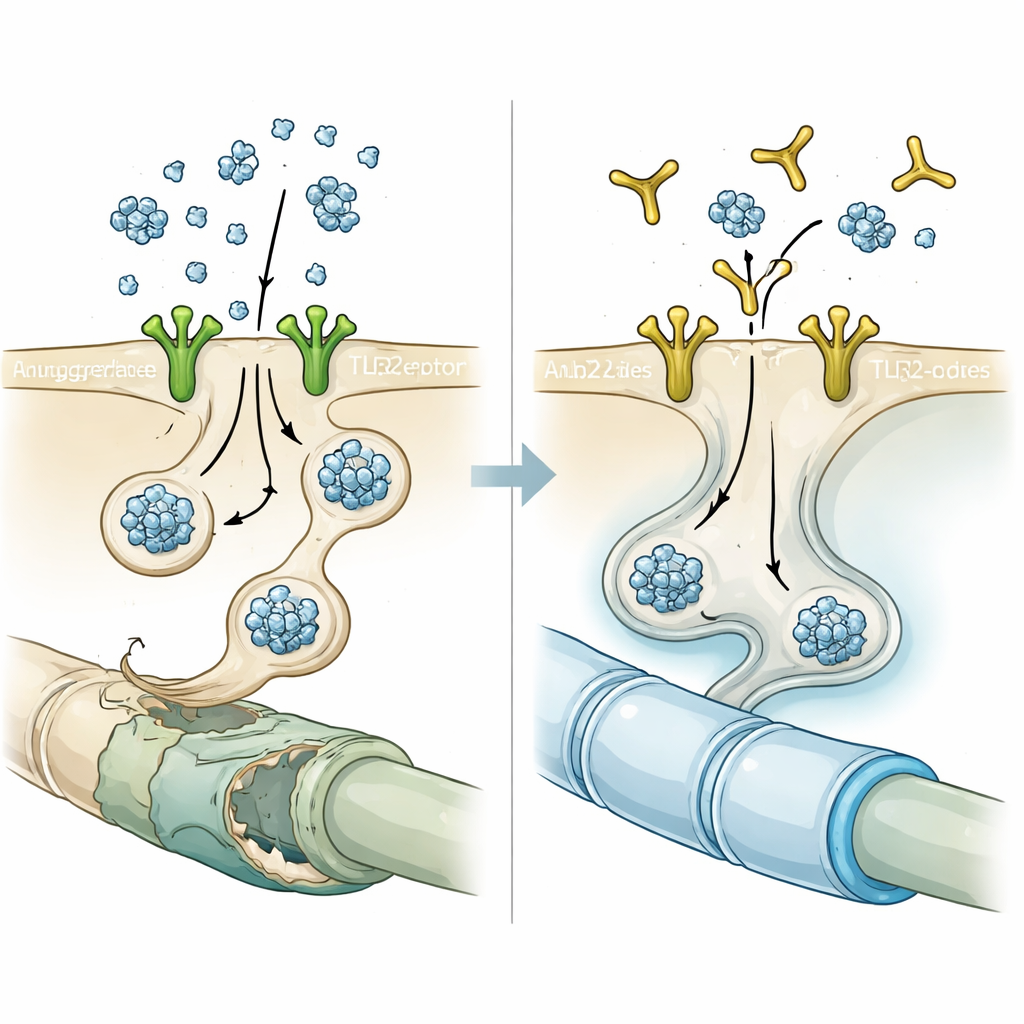
Das Tor mit einem Antikörper blockieren
Anhand dieses Hinweises prüften die Forschenden NM-101, einen Antikörper, der an TLR2 bindet und dessen Aktivierung verhindert. In Zellkulturen reduzierte eine kurze Vorbehandlung der Oligodendrozyten mit NM-101 vor Zugabe von neuronalem Alpha-Synuclein die Zahl und Intensität der einschlussähnlichen Aggregate deutlich. Bei Mäusen, die entweder neuronales Alpha-Synuclein überproduzierten oder Injektionen vorgeformter Alpha-Synuclein-Fibrillen erhielten, senkten wöchentliche NM-101-Infusionen die Menge aggregierten Proteins in der weißen Substanz, dämpften entzündliche Reaktionen von Mikroglia und Astrozyten und verringerten die Aktivierung einer entzündungsfördernden Caspase-1 in Oligodendrozyten. Behandelte Tiere lebten länger und schnitten in motorischen Tests besser ab, was darauf hindeutet, dass die schützenden Effekte des Antikörpers funktionell bedeutsam waren und nicht nur mikroskopische Befunde.
Beschädigte Isolierung retten
Da Oligodendrozyten die Myelinbildner des Gehirns sind, untersuchte das Team, ob die Alpha-Synuclein-Übertragung Myelin schädigt und ob die Blockade von TLR2 helfen kann. Einzelzell-RNA-Sequenzierung von menschlich abgeleiteten Oligodendrozyten, die neuronenkonditioniertem Alpha-Synuclein ausgesetzt waren, zeigte weitreichende Verschiebungen weg von einem reifen, myelinproduzierenden Zustand hin zu einem unreiferen, progenitorähnlichen Profil, wobei viele zentrale Myelin-Gene herunterreguliert wurden. Parallele Genexpressionsstudien an laser-gekapselten Oligodendrozyten von MSA-Patienten und aus dem Mausmodell zeigten ein gemeinsames Muster: verringerte Expression von Genen, die an Bildung und Erhalt von Myelin beteiligt sind. Unter dem Elektronenmikroskop zeigte die weiße Substanz in Alpha-Synuclein-Mäusen dünnere, unregelmäßig organisierte Myelinscheiden. Die NM-101-Behandlung kehrte viele dieser Veränderungen um, verdickte das Myelin, stellte Myelinproteinspiegel wieder her und normalisierte die Expression von Genen, die für die Reifung von Oligodendrozyten erforderlich sind.
Was das für künftige Therapien bedeutet
Die Studie stützt eine klare Erzählung: Bei MSA kann Alpha-Synuclein, das von Neuronen stammt, über TLR2 auf der Oberfläche in Oligodendrozyten gelangen, sich dort anreichern, Entzündungen auslösen, das Entwicklungsprogramm der Zellen entgleisen lassen und die Myelinhülle der neuronalen Verdrahtung erodieren. Durch die Blockade von TLR2 mit einem gezielten Antikörper konnten die Forschenden diese Kette von Ereignissen in Maus- und humanen Zellmodellen unterbrechen, toxische Einschlüsse reduzieren, Entzündungen dämpfen, Myelin reparieren und Überleben sowie Bewegung verbessern. Obwohl NM-101 selbst noch strenge Tests am Menschen benötigt, etabliert die Arbeit die TLR2-abhängige Proteinübertragung als zentralen Treiber der MSA-ähnlichen Pathologie und hebt die Anti-TLR2-Immuntherapie als vielversprechende Strategie hervor, um diese verheerende Erkrankung zu verlangsamen oder zu verhindern.
Zitation: Bae, EJ., Ham, S., Jeong, Y.W. et al. Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models. Nat Commun 17, 2175 (2026). https://doi.org/10.1038/s41467-026-68870-x
Schlüsselwörter: multiple Systematrophie, alpha-Synuclein, Oligodendrozyten, Myelinschaden, Immuntherapie