Clear Sky Science · de
Olig2 wirkt als induzierbare Barriere für die Umwandlung von Astrozyten zu Neuronen in vivo
Hilfezellen des Gehirns in Neuronen verwandeln
Das erwachsene Gehirn besitzt nur eine begrenzte Fähigkeit, verlorene Neuronen zu ersetzen, was bei Erkrankungen wie Schlaganfall, Alzheimer und Rückenmarksverletzungen ein großes Hindernis darstellt. Eine vielversprechende Idee ist, benachbarte "Hilfezellen" — sogenannte Astrozyten — direkt in neue Neuronen umzuwandeln, etwa mithilfe von Gentherapie. Diese Studie stellt eine zentrale Frage: Was verhindert, dass diese Umwandlung im lebenden Gehirn effizient funktioniert — und lassen sich diese Bremsen lösen?
Eine verborgene Bremse gegen zelluläre Formwandlung
Astrozyten versorgen normalerweise Neuronen, erhalten die chemische Balance im Gehirn und reagieren auf Verletzungen. In bestimmten Krankheitszuständen können sie sich etwas wie Stammzellen verhalten, was die Hoffnung weckt, sie könnten vor Ort in Neuronen reprogrammiert werden. Forschende wissen bereits, dass eine Klasse von Genen, die sogenannten proneuralen Transkriptionsfaktoren — etwa Ngn2, Ascl1 und NeuroD1 — Astrozyten Richtung neuronaler Identität treiben kann. Dennoch bleibt die Umwandlung von Astrozyten zu Neuronen in Tieren frustrierend ineffizient. Die Autorinnen und Autoren vermuteten, dass Astrozyten neben bereits vorhandenen Abwehrmechanismen eine neu induzierbare Barriere hochziehen könnten, wenn die Reprogrammierung ausgelöst wird.
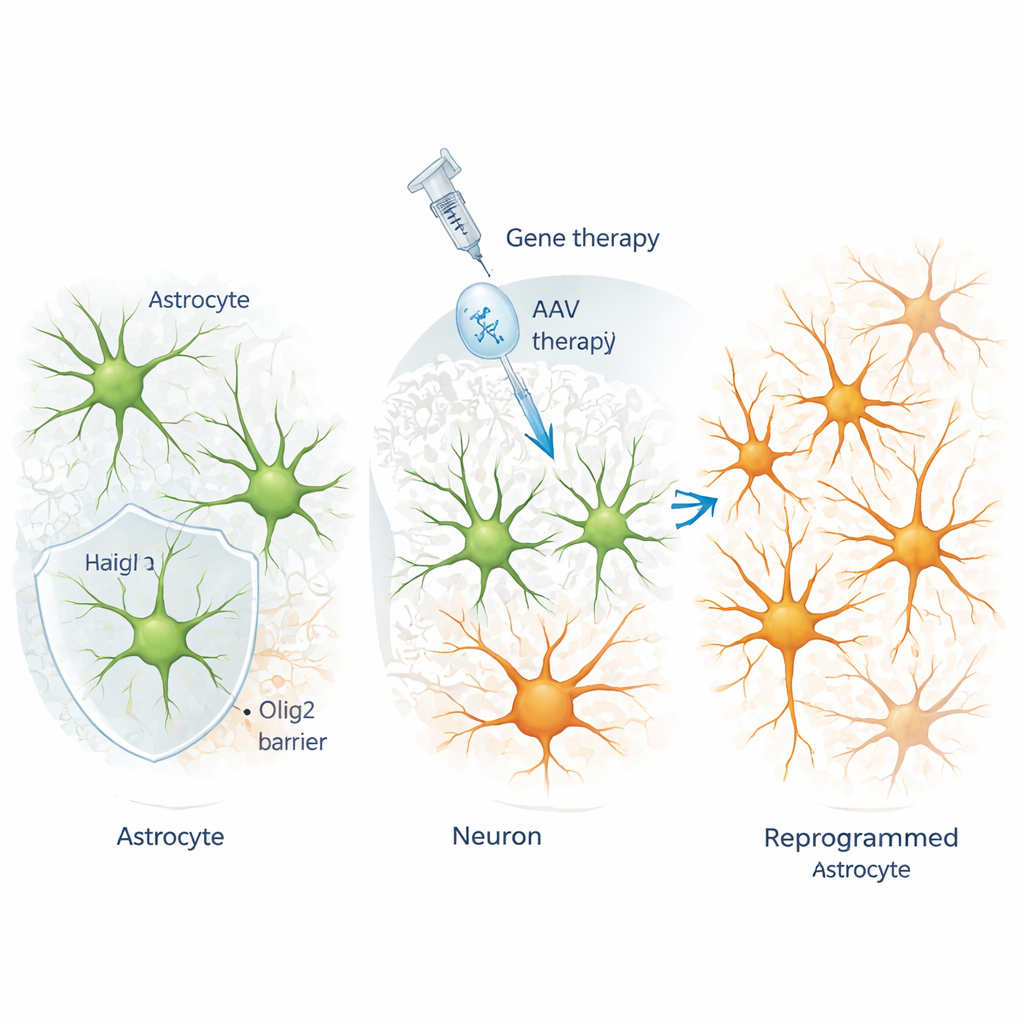
Ein Protein namens Olig2 greift ein, um Veränderungen zu blockieren
In der erwachsenen Maus-Kortex gaben die Forschenden Reprogrammierungsfaktoren in Astrozyten mittels gentechnisch veränderter Viren, die sehr selektiv für diese Zellen sind. Sie entdeckten, dass immer wenn ein basaler Helix–Loop–Helix-(bHLH)-Faktor wie Ngn2, Ascl1 oder NeuroD1 in Astrozyten eingebracht wurde, ein anderer bHLH-Protein, Olig2, dramatisch hochreguliert wurde. Unter normalen Bedingungen findet man Olig2 in Zellen der Oligodendrozyten-Linie, nicht in reifen kortikalen Astrozyten. Sorgfältige Verfolgungsexperimente zeigten, dass die zusätzlich Olig2-positiven Zellen nach der Behandlung nicht durch Proliferation von Oligodendrozytenvorläufern entstanden — stattdessen schalteten die gerade für die Umwandlung anvisierten Astrozyten als Reaktion auf das Reprogrammierungssignal Olig2 an.
Die Entfernung der Bremse verdreifacht die Umwandlung und erzeugt funktionelle Neuronen
Um zu testen, ob Olig2 tatsächlich eine Barriere ist, verwendete das Team kurze Haarnadel-RNAs (shRNAs), um Olig2 gezielt in Astrozyten herunterzuregulieren, die gleichzeitig Ngn2 erhalten hatten. Die Stilllegung von Olig2 reduzierte dessen Proteinspiegel in diesen Zellen nahezu auf null und hatte einen auffälligen Effekt: Der Anteil markierter Astrozyten, die zu Neuronen wurden, stieg im Vergleich zu Ngn2 allein um etwa das Dreifache. Über mehrere Wochen durchliefen viele Zellen eine Zwischenstufe, in der sie typische Astrozytenmarker verloren, bevor sie vollständig neuronale Marker gewannen. Elektrische Aufnahmen aus Hirnschnitten zeigten, dass die umgewandelten Zellen Aktionspotenziale abfeuerten und in etwa der Hälfte der Fälle exzitatorische und inhibitorische synaptische Eingänge erhielten — Merkmale funktioneller Integration in lokale Schaltkreise.
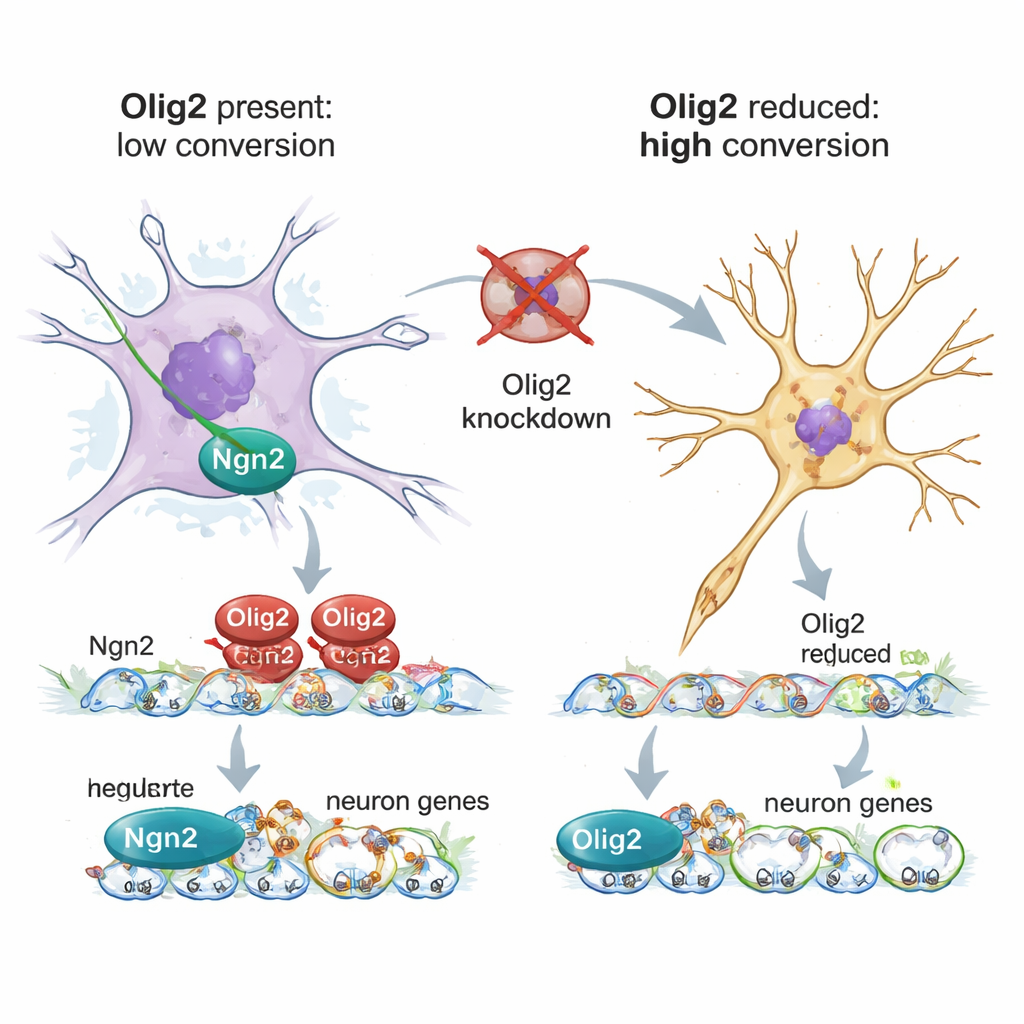
Wie Olig2 den Wechsel zum neuronalen Programm blockiert
Mithilfe der Einzelzell-RNA-Sequenzierung profilierten die Autorinnen und Autoren Tausende einzelner Astrozyten, die Ngn2 ausgesetzt waren, mit oder ohne Olig2-Herunterregulierung. Wenn Olig2 vorhanden war, veränderten Astrozyten ihre Genexpression nur teilweise: Einige Stoffwechsel- und Proteinsynthesewege wurden moduliert, aber Kern-Astrozytengene blieben aktiv und viele neuronale Aufbau-Gene blieben stumm. Als Olig2 reduziert wurde, unterdrückten Astrozyten ihr ausgereiftes Support-Zellprogramm stärker und hochregulierten Gene, die mit neuralen Stammzellen, Neurogenese und Axonwachstum assoziiert sind. Eine ergänzende Methode, CUT&Tag, kartierte, wo Olig2 in der DNA dieser reprogrammierten Astrozyten bindet. Olig2 landete auf regulatorischen Regionen vieler pro-neurogener Gene — einschließlich Ngn2 selbst — konsistent mit einer Rolle als direkter Repressor, der sowohl den Reprogrammierungsfaktor dämpft als auch neuronale Gene abschaltet.
Identitätswechsel der Zellen durch Aufheben einer induzierbaren Abwehr
Insgesamt zeigt die Arbeit, dass Astrozyten eine aktive, induzierbare Abwehr gegen ihre Umwandlung in Neuronen aufbauen: Sobald ein proneuraler Faktor wie Ngn2 eingeführt wird, löst dies Olig2 aus, das wiederum Ngn2 bremst und zentrale neuronale Gene blockiert. Die Deaktivierung von Olig2 löst nicht alle Probleme — die Umwandlungseffizienzen bleiben moderat — verbessert aber deutlich die Ausbeute funktioneller neuer Neuronen und verschiebt Astrozytenstoffwechsel und Genexpression in Richtung eines neuronähnlichen Zustands. Für eine nicht-fachkundige Leserschaft lautet die Quintessenz: Erfolgreiche Hirnreparatur könnte erfordern, nicht nur das Gaspedal mit pro-neuronalen Faktoren zu treten, sondern auch neu entdeckte Bremsen wie Olig2 zu lösen, die Zellen zum Schutz ihrer Identität einsetzen.
Zitation: Lai, C., Hou, K., Li, W. et al. Olig2 acts as an inducible barrier to in vivo astrocyte-to-neuron conversion. Nat Commun 17, 2033 (2026). https://doi.org/10.1038/s41467-026-68869-4
Schlüsselwörter: Umwandlung von Astrozyten zu Neuronen, Zellreprogrammierung, Olig2, Gentherapie, Neuroregeneration