Clear Sky Science · de
Koordinierte Evolution von Genfamilien formt das Genom dimorpher Mucorales
Ein Pilz, zwei Körper
Manche Pilze führen ein Doppelleben und wechseln zwischen einer einzelligen „Hefe“-Gestalt und einer verzweigten „Schimmel“-Gestalt. Diese Formwandlungsfähigkeit hilft ihnen, wechselnde Umgebungen zu überstehen und in manchen Fällen menschliche Gewebe zu befallen. Die hier zusammengefasste Studie zeigt, wie eine Gruppe dieser Pilze, die Mucorales, ihr Genmaterial neu organisiert und nutzt, um beide Lebensweisen innerhalb eines einzigen Genoms zu unterstützen.
Warum formwandelnde Pilze wichtig sind
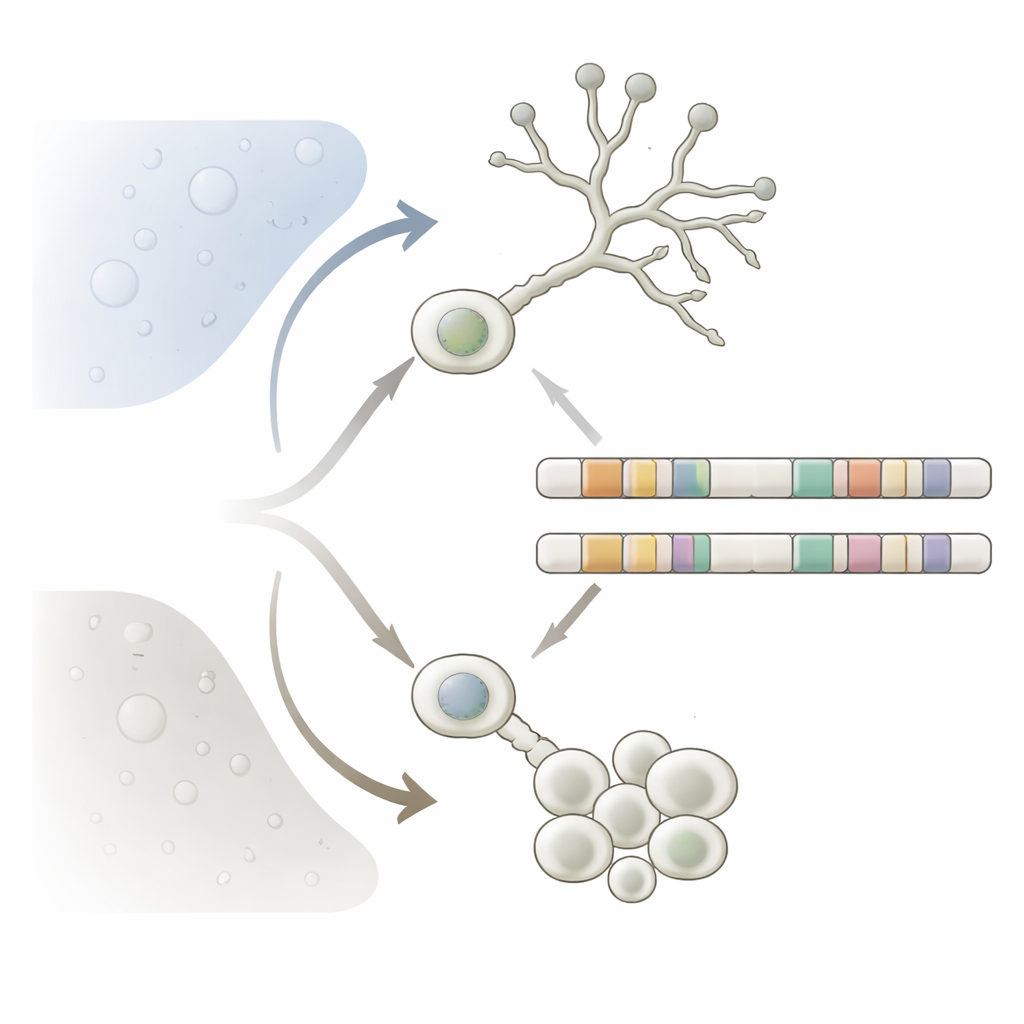
Dimorphe Pilze sind nicht nur ökologisch bedeutsam, sondern auch für die menschliche Gesundheit. Bei Mucorales besteht die Hefegestalt aus isolierten runden Zellen, die niedrige Sauerstoff- und zuckerreiche Bedingungen bevorzugen und sich durch Knospung vermehren. Die Myzelgestalt bildet lange Hyphen, die in sauerstoffreichen Umgebungen gedeihen und Gewebe und Oberflächen eindringen können. Bei mehreren Mucorales-Arten ist nur die filamentöse Gestalt stark infektiös und verursacht Mucormykose, eine schwere Erkrankung bei immungeschwächten Menschen. Zu verstehen, wie diese Pilze die Gestalt wechseln, kann erklären, warum sie so anpassungsfähig sind, weshalb sie gegen manche Arzneimittel resistent sind und welche genetischen Merkmale gefährliche dimorphe Arten von harmlosen Verwandten unterscheiden.
Ein Genom zum Wechseln gebaut
Die Autorinnen und Autoren konzentrierten sich auf den Modellpilz Mucor lusitanicus und verfolgten ihn durch vier Stadien: Hefe, frühes Myzel, die Rückkehr zurück zur Hefe und ausgereiftes Myzel. Durch RNA-Sequenzierung bestimmten sie, welche Gene in jedem Zustand aktiv sind. Sie fanden heraus, dass etwa 70 % aller Gene ihre Aktivität während des Formwechsels ändern — deutlich mehr als bei vielen anderen Pilzen. Hefezellen schalten tendenziell Gene für die Grundstoffwechselprozesse und den Aufbau zellulärer Bausteine ein, während Myzelien Gene bevorzugen, die an interner Signalübertragung und dem Zellskelett beteiligt sind, das das Filamentwachstum trägt. Diese umfassende Umprogrammierung zeigt, dass Dimorphie keine kleine Anpassung, sondern eine Umstrukturierung auf Organismusniveau ist.
Verdoppelte Gene mit geteilten Aufgaben
Eine zentrale Entdeckung ist, dass viele Gene paarweise oder in kleinen Familien vorkommen, deren Kopien sich für eine der beiden Gestalten spezialisiert haben. Das Team betrachtete zuerst ein bekanntes Beispiel neu: zwei Ferrooxidase-Gene und zwei Eisen-Transporter-Gene, die gemeinsam Eisen, ein lebenswichtiges Nährstoffion, aufnehmen. Je ein Mitglied jedes Paares wird in der Hefe genutzt, das andere im Myzel. Das Ausschalten der hefe-spezifischen Kopien schwächte das Hefewachstum stark, ließ das Myzelwachstum jedoch weitgehend intakt; umgekehrt traf dies für die myzel-spezifischen Kopien zu. Bei einer genomweiten Ausweitung dieser Analyse identifizierten die Forschenden 490 solcher „dimorpher Familien“, in denen mindestens eine Kopie hefe-spezifisch und eine andere myzel-spezifisch ist. Insgesamt gehört damit etwa jedes neunte Gen im Genom zu solchen Familien und umfasst viele verschiedene zelluläre Funktionen. Das deutet darauf hin, dass der Pilz statt auf eine universelle Proteinversion für alle Bedingungen auf Zwillingsversionen setzt, die jeweils an die sehr unterschiedlichen Bedingungen des flüssigen, sauerstoffarmen Hefelebens gegenüber dem festen, sauerstoffreichen Myzelleben angepasst sind.
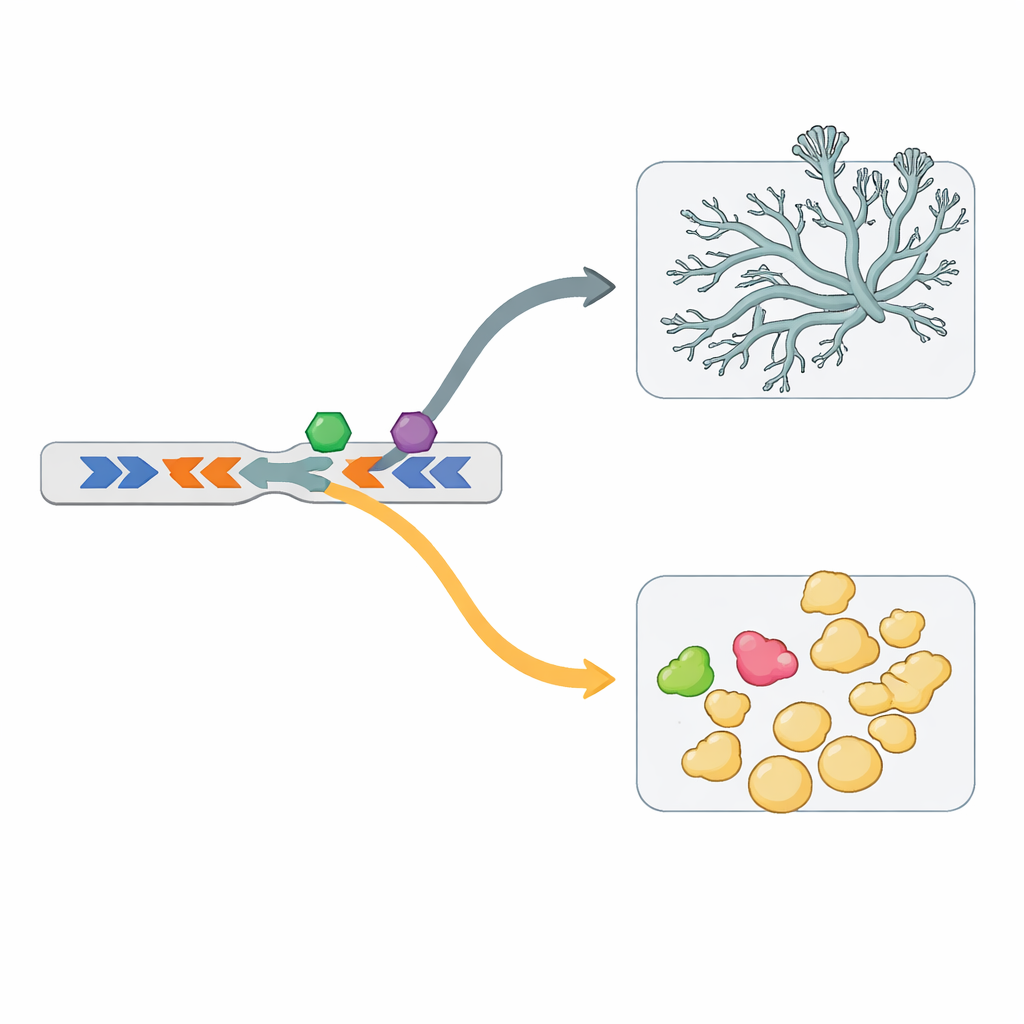
Rück-zu-Rück-Gene und neue Kontrollschalter
Das Genom dupliziert nicht nur Gene, sondern ordnet sie auch in speziellen Konfigurationen an. Viele der Gene für Eisenaufnahme liegen zum Beispiel in „kopf-an-Kopf“-Paaren: zwei Gene, die in entgegengesetzte Richtungen stehen und eine zentrale Kontrollregion teilen. Ein solches Paar ist in der Hefe aktiv, das benachbarte Paar im Myzel. Der experimentelle Austausch dieser gemeinsamen Kontrollregionen kehrte die Aktivitätszeitpunkte der Gene um und bewies damit, dass diese Anordnung als koordinierter Schalter fungiert. Eine Durchmusterung des gesamten Genoms fand über tausend solcher Kopf-an-Kopf-Paare, von denen Hunderte an der Dimorphie beteiligt sind. Die gemeinsamen Kontrollregionen für hefe- und myzelgebundene Paare tragen unterschiedliche DNA-Motive, was darauf hindeutet, dass sie von verschiedenen regulatorischen Faktoren gelesen werden.
Master-Regulatoren und evolutionäre Hinweise
Um diese Regulatoren zu finden, nutzten die Forschenden die gemeinsame Kontroll-DNA der Eisenaufnahme-Gene als Köder, um Proteine herauszufischen, die dort binden. Sie identifizierten zwei zuvor uncharakterisierte Proteine, die sie DFL und DKL nannten, und erzeugten Mutantenstämme ohne jedes dieser Gene. Diese Mutanten zeigten stark gestörte Formwechsel: DKL-Mutanten konnten überhaupt keine Hefe mehr bilden, und beide Mutanten verloren das normale Aktivitätsmuster über Tausende dimorphiebezogener Gene hinweg. Beim Vergleich mit verwandten Arten beobachtete das Team, dass dimorphe Mucorales tendenziell verdoppelte, form-spezifische Genfamilien, Kopf-an-Kopf-Strukturen und das dfl-Gen behalten, während nahe verwandte Pilze, die nicht die Gestalt wechseln, diese Merkmale oft nicht besitzen. Dieses Muster legt nahe, dass sich diese genomischen Eigenschaften gemeinsam als Werkzeugkasten für Dimorphie entwickelt haben und als Marker dienen können, um vorherzusagen, welche Arten wahrscheinlich Formwandler sind.
Was das für Pilzkrankheiten bedeutet
Kurz gesagt zeigt diese Arbeit, dass Mucorales-Pilze ihr Genom um die Herausforderung aufgebaut haben, zwei getrennte Lebensweisen zu beherrschen. Sie lösen dies, indem sie wichtige Gene duplizieren, eine Kopie für die Hefe und die andere für das Myzel feinabstimmen, viele davon in Rücken-an-Rücken-Kontrolleinheiten verdrahten und dedizierte Regulatoren verwenden, um zu koordinieren, welche Version wann genutzt wird. Da die invasive, krankmachende Gestalt oft das Myzel ist und weil einige der betroffenen Gene die Eisenaufnahme und die Medikamentenempfindlichkeit steuern, deuten diese Erkenntnisse auf neue Wege hin, vorherzusagen, welche Pilze gefährlich werden können, und Behandlungsansätze zu entwickeln, die ihre Fähigkeit zum Formwechsel stören.
Zitation: Tahiri, G., Navarro-Mendoza, M.I., Lax, C. et al. Coordinated gene family evolution shapes the genome of dimorphic Mucorales. Nat Commun 17, 2148 (2026). https://doi.org/10.1038/s41467-026-68866-7
Schlüsselwörter: fungale Dimorphie, Mucorales, Genverdopplung, Genomregulation, fungale Pathogenese