Clear Sky Science · de
NKG2D-Aufregulierung macht Tumoren empfindlicher gegenüber kombinierter Anti-PD1- und Anti-VEGF-Therapie und verhindert Hörverlust
Warum diese Forschung für Menschen mit Hörverlust wichtig ist
Manche Menschen erben eine Erkrankung namens NF2-assoziierte Schwannomatose, bei der gutartige Tumoren an den Nerven des Innenohrs wachsen und oft zu schrittweisem, dauerhaftem Hörverlust führen. Aktuelle Behandlungen können Tumoren verkleinern, schädigen aber mitunter das Gehör oder verlieren mit der Zeit an Wirksamkeit. Diese Studie untersucht eine neue Wirkstoffkombination, die in Labormodellen nicht nur das Tumorwachstum verlangsamt, sondern auch das Hören schützt, und damit auf sanftere und länger anhaltende Behandlungsoptionen für Patientinnen und Patienten hinweist.
Die Tumoren hinter dem Schweigen verstehen
Bei der NF2-assoziierten Schwannomatose bilden sich sogenannte vestibuläre Schwannome am Gleichgewichts- und Hörnerv im Schädel. Wenn diese Tumoren wachsen, können sie die empfindlichen Nervenfasern schädigen, die Schallsignale zum Gehirn leiten, und in schweren Fällen auf den Hirnstamm drücken. Chirurgie und Strahlentherapie können Leben retten und Tumoren entfernen oder kontrollieren, bergen aber echte Risiken: Verschlechterung des Gehörs, Schwindel und Schwäche des Gesichtsnervs. Ein Wirkstoff namens Bevacizumab, der ein Wachstumsignal für Blutgefäße (VEGF) blockiert, wird manchmal eingesetzt, um diese Tumoren zu verkleinern und das Hören zu verbessern; nur etwa ein Drittel der Patientinnen und Patienten profitiert jedoch, und der Effekt lässt häufig nach. Das treibt die Suche nach sichereren und dauerhafteren Therapien voran.
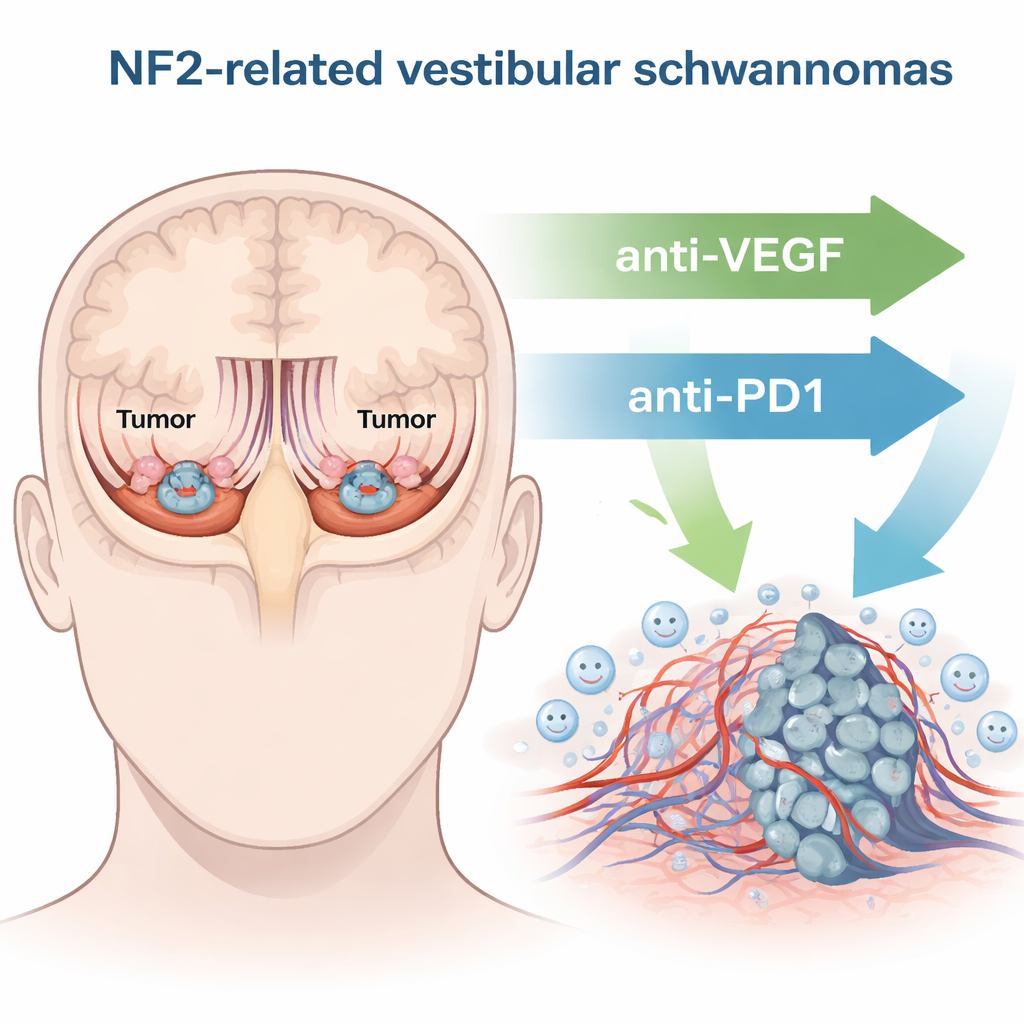
Das Immunsystem als Verbündeten gewinnen
In den letzten zehn Jahren hat die Krebsbehandlung durch Immun-Checkpoint-Inhibitoren einen Wandel erfahren – Wirkstoffe, die die „Bremsen“ der Immunzellen lösen, damit diese Tumore effektiver angreifen können. Eine solche Bremse, PD-1, sitzt auf der Oberfläche von Immunzellen und kann sie ausschalten, wenn sie aktiviert wird. Die Autorinnen und Autoren fragten, ob die Blockade von PD-1 (mittels eines Anti-PD1-Antikörpers) dem Immunsystem helfen könnte, vestibuläre Schwannome zu kontrollieren, und ob eine Kombination mit VEGF-blockierender Therapie noch wirksamer wäre. In Mausmodellen, die menschliche Innenohr- und periphere Nerventumoren gut nachbilden, behandelten sie Tiere mit Anti-VEGF allein, Anti-PD1 allein oder der Kombination und verfolgten anschließend Tumorwachstum, Überleben und Hören.
Die Tumorblutgefäße besser funktionieren lassen, statt sie verschwinden zu lassen
Das Team fand heraus, dass Anti-VEGF mehr bewirkte, als die Tumoren zu „verhungern“. Es remodelte die abnormalen, undichten Blutgefäße zu stabileren, besser funktionierenden Gefäßen. Unter dem Mikroskop zeigten behandelte Tumoren mehr Gefäße, die von Stützzellen bedeckt waren, und einen höheren Anteil an Gefäßen, die tatsächlich Blut führten. Diese „Normalisierung“ verbesserte die Zustellung des Anti-PD1-Antikörpers in den Tumor und erlaubte mehr krebsbekämpfenden Immunzellen – insbesondere CD8-T-Zellen und natürlichen Killerzellen (NK-Zellen) – einzudringen. Bei Mäusen, die die Kombination erhielten, wuchsen die Tumoren langsamer, zeigten weniger teilende Zellen und mehr Zellen mit program- miertem Zelltod, und die Tiere lebten länger als bei einer Einzeltherapie.
Die Abtötungskraft der Immunzellen verstärken
Die Vorteile der Kombination bestanden nicht nur darin, mehr Immunzellen in den Tumor zu bringen; diese Zellen waren auch aggressiver, sobald sie dort angekommen waren. Die Anti-VEGF-Behandlung erhöhte das Vorkommen von Molekülen wie Granzyme B und Perforin, die als molekulare „Geschosse“ des Immunsystems Tumorzellen durchlöchern. Ein zentraler Schalter in diesem Prozess war ein Rezeptor namens NKG2D, der sowohl auf T-Zellen als auch auf NK-Zellen vorkommt. Anti-VEGF steigerte NKG2D und seine Partnermoleküle auf Tumorzellen, wodurch Immunzellen in Laborversuchen wirksamere Killer wurden. Als die Forschenden NKG2D blockierten, nahmen die antitumoralen Effekte der Therapien deutlich ab, was zeigt, dass dieser Weg wesentlich für die Wirkungssteigerung ist. Wichtig: Kleine Proben von menschlichen Tumoren, die langfristig mit Bevacizumab behandelt worden waren, zeigten Genaktivitätsmuster, die zu mehr aktivierten und weniger „erschöpften“ T- und NK-Zellen passten, was darauf hindeutet, dass ein ähnlicher Immunboost auch bei Patientinnen und Patienten auftreten könnte.
Hören schützen und Tumoren kontrollieren
Eine entscheidende Frage war, ob diese immunbasierten Behandlungen das Hören schaden oder helfen würden. Gesunde Mäuse, die nur Anti-PD1 erhielten, behielten normale Hörschwellen, was darauf hindeutet, dass der Wirkstoff kein kurzfristiges Auditivschadenspotenzial hat. Bei tumorbefallenen Mäusen verbesserte Anti-VEGF allein das Hören im Vergleich zu keiner Behandlung, was klinische Erfahrungen widerspiegelt. Anti-PD1 allein und die Kombination aus Anti-PD1 mit Anti-VEGF stellten die Hörschwellen beider nahezu wieder auf Normalniveau her. Als die Forschenden ein realistisches Szenario nachstellten – zunächst Behandlung mit Anti-VEGF und dann entweder Fortsetzung, Abbruch oder Ergänzung durch Anti-PD1 – fanden sie, dass ein Wechsel zu Anti-PD1 das Tumorwachstum noch verlangsamen konnte, der Abbruch von Anti-VEGF jedoch dessen hörschützenden Effekt aufhob. Die Fortführung von Anti-VEGF und die Zugabe von Anti-PD1 ergaben die besten Ergebnisse für Überleben und Hörerhalt.
Was das für Patientinnen und Patienten bedeuten könnte
Für Menschen mit NF2-assoziierter Schwannomatose deutet diese Arbeit auf eine Zukunft hin, in der eine Behandlung mehr leistet, als Tumoren bloß in Schach zu halten – sie könnte auch die Fähigkeit zu hören erhalten. In sorgfältig gestalteten Mausmodellen schuf die Kombination aus einem VEGF-Blocker und einem PD-1-Blocker eine günstigere Umgebung für Immunzellen, verstärkte ihre Tumor-killer-Funktion über NKG2D und schützte das Hören besser als jede Einzeltherapie. Zwar sind klinische Studien nötig, um Sicherheit und Nutzen beim Menschen zu bestätigen, doch die Studie liefert eine klare Roadmap für die Prüfung dieser Wirkstoffkombination als neue, potenziell länger anhaltende Strategie zur Behandlung vestibulärer Schwannome und zur Verhinderung von Hörverlust.
Zitation: Lu, S., Yin, Z., Wu, L. et al. NKG2D upregulation sensitizes tumors to combined anti-PD1 and anti-VEGF therapy and prevents hearing loss. Nat Commun 17, 1148 (2026). https://doi.org/10.1038/s41467-026-68865-8
Schlüsselwörter: vestibuläres Schwannom, NF2, Immuntherapie, Bevacizumab, Hörerhalt