Clear Sky Science · de
Antiparalleles Stapeln von Csu-Pili treibt die 3D-Biofilm‑Assemblierung von Acinetobacter baumannii an
Wie Krankenhauskeime geschützte Städte bauen
Einige der widerstandsfähigsten Krankenhauskeime überleben Antibiotika, indem sie sich in schleimigen, dreidimensionalen Gemeinschaften verstecken, sogenannten Biofilmen. Diese Studie stellt eine einfache, aber zentrale Frage: Wie verknüpfen sich einzelne Bakterien zu solch stabilen, geschichteten Strukturen? Mit Hilfe hochauflösender Elektronenmikroskopie entdeckten die Forschenden ein mikroskopisches „Klettband“ aus haarähnlichen Filamenten, das dem gefährlichen Erreger Acinetobacter baumannii ermöglicht, sich zu schützenden 3D‑Klumpen zu verweben. Das Verständnis dieses verborgenen Gerüsts könnte Wege eröffnen, Biofilme aufzubrechen und vorhandene Medikamente wieder wirksamer zu machen.
Winzige Haare, die Bakterien zusammenhalten
A. baumannii, eine Hauptursache schwer behandelbarer Krankenhausinfektionen, ist mit dünnen Oberflächenhaaren, den Csu‑Pili, übersät. Frühere Arbeiten zeigten, dass diese Pili für die Bildung robuster, kuppelförmiger Biofilme unerlässlich sind, doch blieb unklar, wie sie Zellen tatsächlich zu einer 3D‑Struktur verbinden. Mit mehreren Formen der Elektronenmikroskopie bestätigten die Autorinnen und Autoren zunächst, dass in Flüssigkulturen die Pili größtenteils einzeln von jeder Bakterienzelle abstehen, wie Stacheln an einer Klette. In dichten, auf Oberflächen gewachsenen Kolonien ändert sich das Bild jedoch dramatisch: Viele Pili packen sich dicht zusammen und bilden breite, flache Bänder, die zwischen benachbarten Zellen verlaufen und ein zart wirkendes, aber umfangreiches dreidimensionales Netzwerk erzeugen. 
Flache Leitern aus gepaarten Filamenten
Um zu klären, wie diese Bänder entstehen, reinigte das Team Csu‑Pili und beobachtete ihr Verhalten in Isolation. Innerhalb von Tagen bis Wochen paarten sich einzelne Filamente und verschmolzen zu mehrsträngigen „Superstapeln“, die schließlich ein gelartiges Netzwerk bildeten, das die in echten Biofilmen beobachteten Strukturen eng nachahmte. Hochauflösende Kryo‑Elektronenmikroskopie enthüllte das zugrunde liegende Design. Jeder Pilus ist kein glatter Schlauch, sondern eine zickzackförmige Stange. Liegen zwei Stangen nebeneinander in entgegengesetzter Richtung, berühren sie sich an wiederkehrenden Eckpunkten und bilden stabile laterale Verbindungen. Viele solche antiparallelen Paare können sich dann zu einem sehr dünnen, plattenartigen Stapel anreihen — im Wesentlichen eine mikroskopische Leiter oder ein Band, das nur eine Filamentdicke, aber viele Filamentbreiten hat.
Ein eingebauter Bauplan für 3D‑Wachstum
Die detaillierten Strukturen zeigen, dass diese Stapelfähigkeit fest in der Geometrie der Pili verankert ist. Das Zickzack‑Muster wiederholt sich über sehr kurze Distanzen und schafft viele potenzielle Kontaktpunkte entlang jedes Filaments. Dadurch kann, sobald zwei Pili in der richtigen Orientierung aufeinandertreffen, eine Kette von Verbindungen wie ein Reißverschluss entstehen und das Blatt schnell verlängern. Wichtig ist, dass die Ausrichtung der Stangen sicherstellt, dass Kontakte meist zwischen Pili unterschiedlicher Zellen und nicht innerhalb derselben Zelle gebildet werden, was die Zell‑zu‑Zell‑Verknüpfung natürlich fördert. Die Stapel bleiben flexibel und dehnbar, sodass der wachsende Biofilm physikalischen Belastungen standhalten kann, ohne auseinanderzubrechen. Die Forschenden beobachteten, dass sich bei der Zellteilung neue Tochterzellen oft mit ihren Pili gegenüberliegend anordnen, was die Stapelbildung genau dort begünstigt, wo Zellen zu einem 3D‑Cluster zusammengebunden werden müssen. 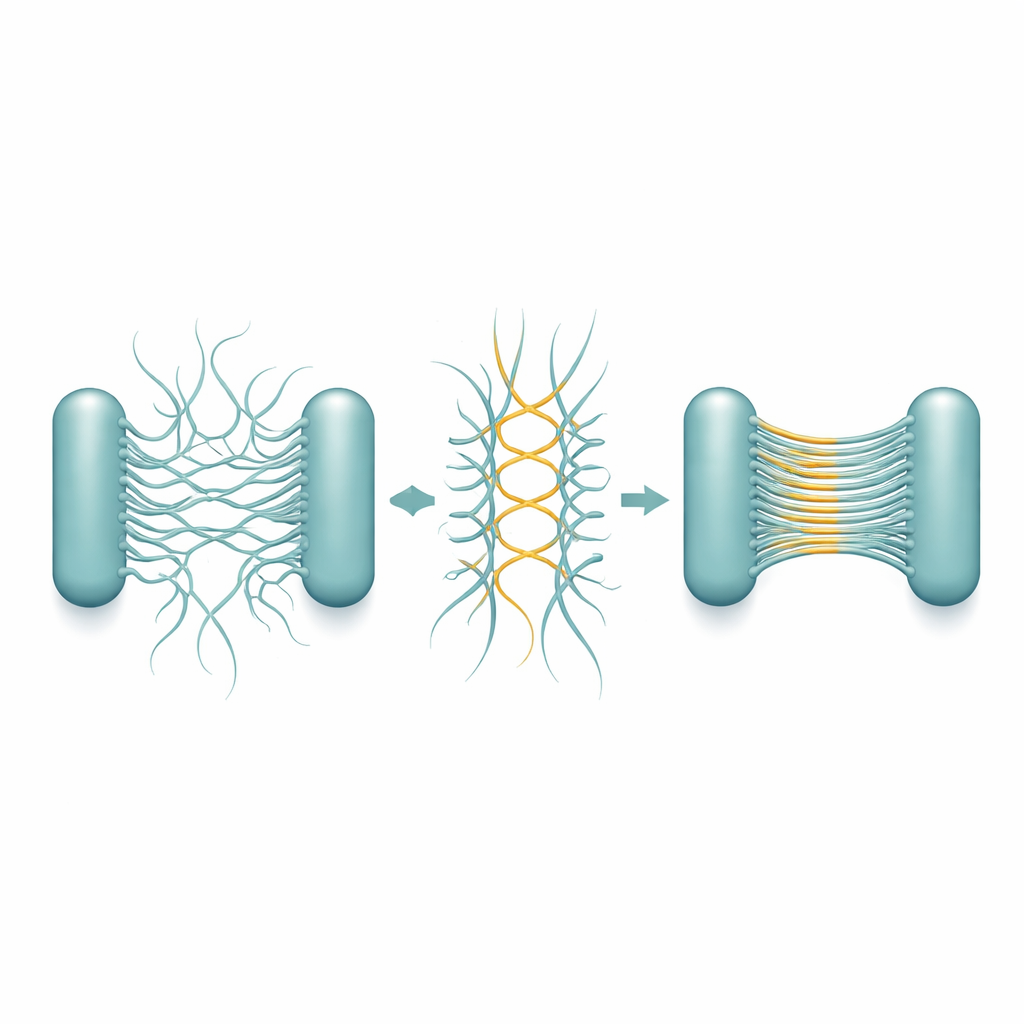
Kleber, Füllstoff und frühe Gerüste
Die Studie untersuchte auch, wie andere Komponenten des Biofilms beitragen. Ein zuckerartiges Polymer namens PNAG und lockere DNA aus zerstörten Zellen reichern sich in ausgereiften Biofilmen an. Mikroskopie zeigte, dass diese Substanzen die engen Zwischenräume zwischen Bakterien ausfüllen und sich um die Pilus‑Stapel wickeln, ähnlich wie Beton um eine Stahlbewehrung gegossen wird. Entfernten die Forschenden jedoch PNAG und DNA, bildeten die Bakterien weiterhin organisierte Flöße, die allein durch Csu‑Pilus‑Stapel zusammengehalten wurden. Das zeigt, dass die Pili das primäre Gerüst aufbauen, während das umgebende Material später die Struktur zementiert und stabilisiert.
Neue Schwachstellen in bakteriellen Festungen
Vereinfacht gesagt erklärt diese Arbeit, wie A. baumannii seine Oberflächenhaare nutzt, um sich in robuste, mehrlagige Klumpen zu verflechten, die für Medikamente und Immunzellen schwer durchdringlich sind. Die Pili wirken zunächst als Haken, um Oberflächen zu greifen, und dann als flexible Bänder, die sich zu flachen Blättern stapeln und benachbarte Zellen in alle Richtungen miteinander verbinden. Zuckerpolymere und DNA füllen anschließend die Zwischenräume und verwandeln dieses Bänderwerk in eine feste Festung. Indem die Studie die genaue Art und Weise aufzeigt, wie Pili aneinanderhaften, benennt sie ein neues Ziel: Wirkstoffe oder Moleküle, die Pilus‑zu‑Pilus‑Kontakte blockieren, könnten das Biofilmgerüst von innen schwächen und hartnäckige bakterielle Infektionen leichter angreifbar machen.
Zitation: Malmi, H., Pakharukova, N., Paul, B. et al. Antiparallel stacking of Csu pili drives Acinetobacter baumannii 3D biofilm assembly. Nat Commun 17, 2508 (2026). https://doi.org/10.1038/s41467-026-68860-z
Schlüsselwörter: Biofilme, Acinetobacter baumannii, Pili, Antibiotikaresistenz, Kryo‑Elektronenmikroskopie