Clear Sky Science · de
Früherkennung abweichender Zellschicksale und Reparatur mithilfe zirkulierender Vorläuferzellen bei Patienten mit heterotoper Ossifikation
Wenn Knochen dort wächst, wo er nicht hingehört
Manchmal beginnt nach schweren Verletzungen oder Gelenkoperationen Knochen in Muskeln und anderem Weichgewebe zu wachsen, wo er nicht hingehört. Diese Erkrankung, heterotope Ossifikation genannt, kann Gelenke blockieren, starke Schmerzen verursachen und alltägliche Bewegungen nahezu unmöglich machen. Ärzte entdecken sie derzeit meist erst, nachdem der fehlgeleitete Knochen bereits Fuß gefasst hat, wenn es zu spät ist, um ihn zu verhindern. Diese Studie stellt eine einfache, aber weitreichende Frage: Könnte eine routinemäßige Blutabnahme Wochen im Voraus warnen, dass dieser verborgene Knochen im Entstehen ist?
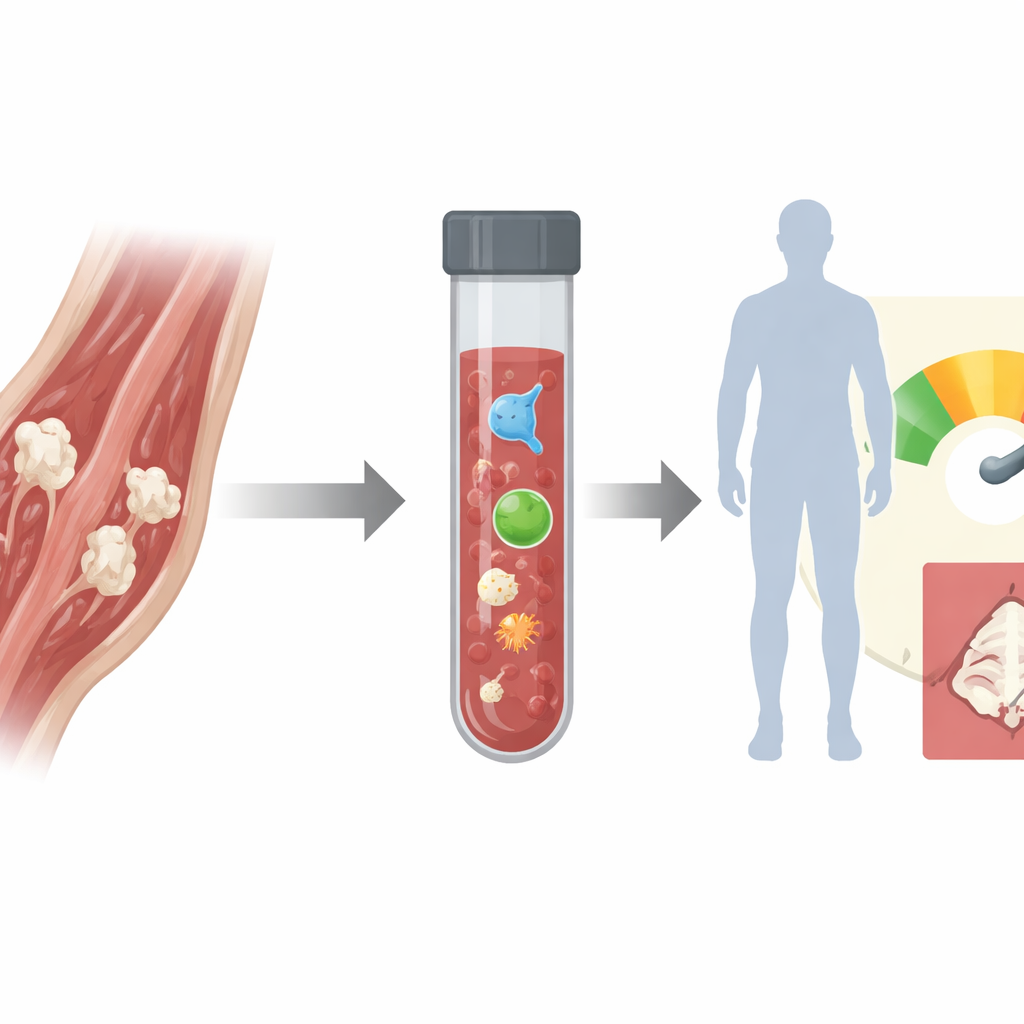
Eine versteckte Gefahr nach Verletzung und Operation
Heterotope Ossifikation ist überraschend häufig nach schweren Verbrennungen, Explosionstraumen im militärischen Kontext, Frakturen und insbesondere nach Hüftgelenksersatz. Die heutigen Mittel — Röntgenaufnahmen, CT-Scans und Knochenszintigraphien — schlagen jedoch erst nach sechs bis acht Wochen an, wenn der neue Knochen bereits gereift ist. Schutzmaßnahmen wie Strahlenbehandlung oder starke entzündungshemmende Medikamente existieren zwar, haben aber ernste Nebenwirkungen und werden oft breit angewendet, weil wir nicht zuverlässig sagen können, wer sie wirklich braucht oder wann man mit der Behandlung beginnen und aufhören sollte. In der Folge erhalten viele Patientinnen und Patienten entweder unnötig riskante Medikamente oder verpassen das enge Zeitfenster, in dem diese Mittel tatsächlich die Entstehung zusätzlichen Knochens verhindern könnten.
Seltene Reparaturzellen im Blut verfolgen
Das Forschungsteam konzentrierte sich auf eine besondere Gruppe von Reparaturzellen, die sogenannten mesenchymalen Vorläuferzellen, die normalerweise beim Wiederaufbau von Knochen und Bindegewebe helfen. Nach bestimmten Verletzungen gelangen winzige Mengen dieser Zellen in den Blutkreislauf. Mithilfe eines mikrofluidischen Geräts — eines Chips, der Zellen in engen Kanälen sortieren kann — fischten die Wissenschaftler diese seltenen zirkulierenden mesenchymalen Vorläuferzellen aus Blutproben von Mäusen und von Patienten, die sich einer Hüftoperation unterzogen. Sie entdeckten, dass diese zirkulierenden Zellen bereits wenige Stunden nach einer Verletzung, die später zu heterotopen Knochen führt, ein charakteristisches Muster aktiver Gene tragen, das sich sowohl von normalen Blutzellen als auch von Blutproben nach Verletzungen unterscheidet, die nicht zur zusätzlichen Knochenbildung führen.
Genmuster in einen Frühwarntest verwandeln
Durch den Vergleich von Blutproben von Patientinnen und Patienten, die später eine heterotope Ossifikation entwickelten, mit denen, die dies nicht taten, und durch die Zuordnung dieser Ergebnisse zu detaillierten Studien an Mäusen, identifizierte das Team eine Gruppe von 32 Genen, die zusammen eine molekulare „Signatur" für schädliche Knochenbildung bilden. Anschließend nutzten sie maschinelle Lernalgorithmen, um ein Vorhersagemodell zu trainieren, das ausschließlich die Aktivitätsniveaus dieser Gene in den zirkulierenden Vorläuferzellen betrachtet. In den menschlichen Proben konnte dieser blutbasierte Test bis zu 90 Prozent der zukünftigen Fälle korrekt identifizieren und zugleich in allen Patienten, die gesund blieben, Fehlalarme vermeiden. Bemerkenswerterweise trat die Gen-Signatur bereits sechs Stunden nach Operation oder Trauma auf — mehr als einen Monat bevor Standardbildgebung neuen Knochen nachweisen kann.
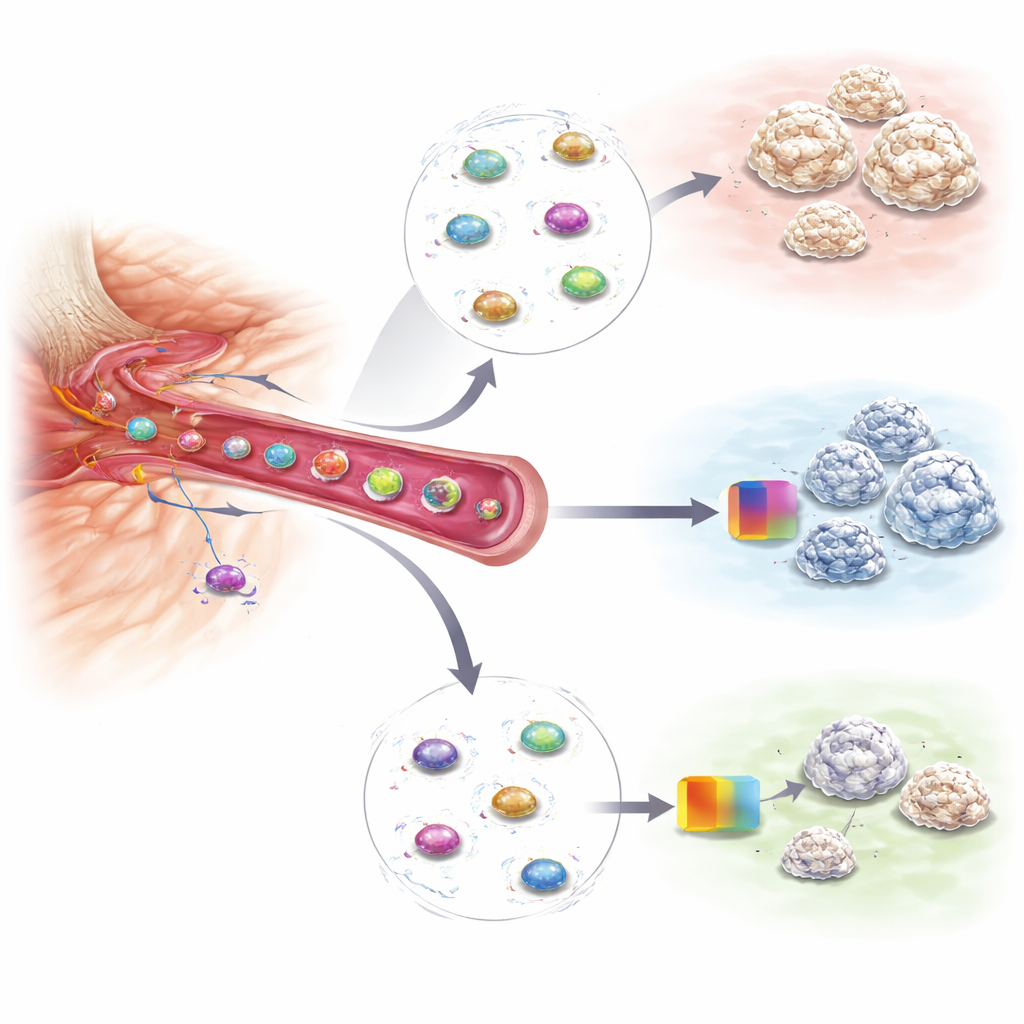
Prüfen, ob Behandlungen tatsächlich wirken
Der gleiche blutbasierte Ansatz erwies sich auch als nützlich zur Überwachung von Therapien. In einem Mausmodell behandelten die Forschenden verletzte Tiere mit einem Medikament, das ein Enzym blockiert, das an der Versteifung der Gewebematrix beteiligt ist und bekanntermaßen heterotope Knochenbildung reduziert. Wenn die Behandlung wirksam war, fiel die Gen-Signatur in den zirkulierenden Vorläuferzellen deutlich ab, und die Tiere entwickelten später deutlich kleinere Herde von zusätzlichem Knochen. Andere Verletzungsarten, die keine heterotope Ossifikation auslösen — etwa Muskelschäden oder Kopfverletzungen — zeigten nicht denselben Anstieg dieser Zellen oder ihres Genmusters, was die Spezifität des Tests unterstreicht. Das deutet darauf hin, dass wiederholte Blutentnahmen sowohl Hochrisiko-Patienten aufspüren als auch nahezu in Echtzeit anzeigen könnten, ob eine vorbeugende Behandlung wirkt.
Was das für Patientinnen und Patienten bedeuten könnte
Insgesamt deuten die Befunde auf eine Zukunft hin, in der ein einfacher Bluttest nach schweren Verletzungen oder Gelenkoperationen eine hochgradig personalisierte Versorgung steuern könnte. Anstatt alle gleich zu behandeln, könnten Ärztinnen und Ärzte Personen identifizieren, deren Reparaturzellen sich in Richtung Knochenbildung am falschen Ort entwickeln, präventive Therapien frühzeitig beginnen und sie beenden, sobald die gefährliche Gen-Signatur verschwindet. Über die heterotope Ossifikation hinaus könnten ähnliche „Liquid Biopsies“ zirkulierender Reparaturzellen Ärzten helfen, andere Erkrankungen zu verfolgen, bei denen die Gewebeheilung fehlgeleitet ist, wie Arthritis oder Fibrose. Für Patientinnen und Patienten könnte das weniger Komplikationen, kürzere Behandlungszeiträume mit riskanten Medikamenten und eine bessere Chance bedeuten, mobil und schmerzfrei zu bleiben.
Zitation: Nunez, J., Holtz, M., Korlakunta, S. et al. Early detection of aberrant cell fate and repair using circulating progenitor cells in patients with heterotopic ossification. Nat Commun 17, 2231 (2026). https://doi.org/10.1038/s41467-026-68857-8
Schlüsselwörter: heterotope Ossifikation, Liquid Biopsy, mesenchymale Vorläuferzellen, Gelenkersatz, Früherkennung