Clear Sky Science · de
Degradation der negativen Elektrode durch zweistufiges Zinkabscheidungsverhalten und dessen Wiederherstellung in Zinkbatterien
Warum Zinkbatterien im Alltag wichtig sind
Elektrizität sicher und kostengünstig zu speichern ist grundlegend — vom Rückhalt für Solarzellen in Häusern bis zur Stabilisierung des Stromnetzes. Zink‑Metall‑Batterien sind dabei attraktive Kandidaten: Zink ist reichlich vorhanden, ungiftig und funktioniert in wasserbasierten Elektrolyten, die deutlich sicherer sind als die brennbaren Flüssigkeiten vieler Lithium‑Batterien. Trotzdem gehen diese vielversprechenden Batterien weiterhin zu schnell in Leistung verloren oder kurzschließen. Dieser Artikel macht einen verborgenen zweistufigen Wachstumsprozess an der Zinkelektrode sichtbar, der diese Schäden verursacht, und stellt eine chemische „Selbstheilungs“‑Strategie vor, die die Lebensdauer deutlich verlängert.
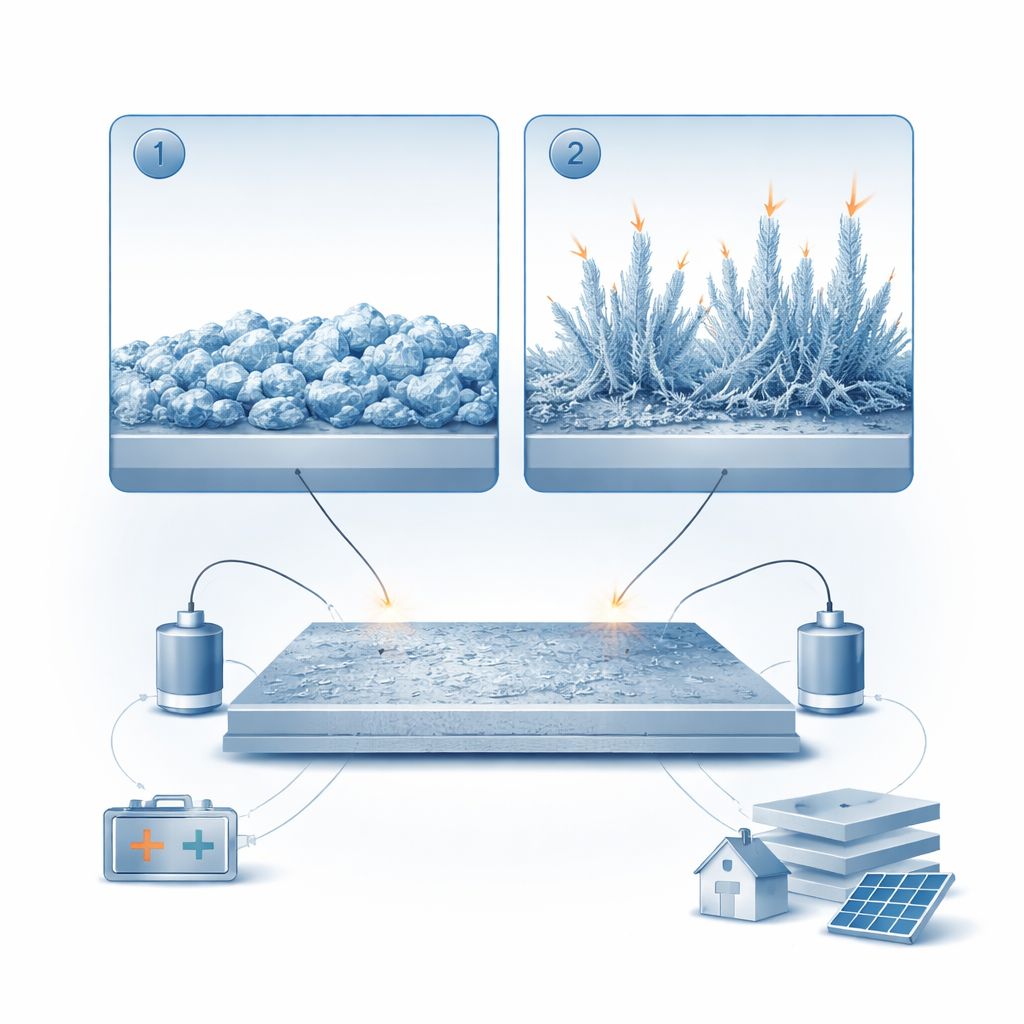
Vom glatten Metall zum Zink‑„Moos“
Die negative Elektrode in diesen Batterien besteht aus Zinkmetall, das beim Laden und Entladen wiederholt abgeschieden (Zink wird hinzugefügt) und aufgelöst (Zink wird entfernt) wird. In einer transparenten Zelle mit Mikroskop beobachteten die Forschenden, wie sich Zink im Laufe der Zeit auf einer Metalloberfläche aufbaut. Sie stellten fest, dass Zink nicht nur auf eine Weise wächst, sondern in zwei klar unterscheidbaren Phasen. Zuerst bildet sich eine relativ dichte, klumpige Kristallstruktur, die eine glänzende, kompakte Schicht ergibt. Mit fortschreitender Abscheidung sprossen dann von scharfen Kanten und Spitzen dünne, fadenartige Strukturen. Diese zweite, „mossige“ Zinkphase füllt den Raum zwischen den Elektroden und verbindet sie schließlich, was interne Kurzschlüsse begünstigt.
Wie mossiges Zink zu „totes“ Zink wird
Das Team kombinierte Direktbildgebung, Elektronenmikroskopie und Computersimulationen, um zu verstehen, warum diese mossige Schicht entsteht. Die scharfen Vorsprünge an den klumpigen Zinkstellen konzentrieren das elektrische Feld — ein Effekt ähnlich Blitzableitern, die elektrische Entladungen bündeln. Diese Feldkonzentration zieht mehr Zinkionen an die Spitzen und fördert so ein schnelles, drahtartiges Wachstum. Beim umgekehrten Prozess, wenn Zink wieder aufgelöst wird, lösen sich die mossigen Filamente zuerst und verlieren dabei den elektrischen Kontakt zum darunterliegenden Metall. Zurück bleibt sogenanntes „totes“ Zink: kleine, elektrisch isolierte Partikel, die nicht mehr an der Batteriereaktion teilnehmen, aber noch aktives Material enthalten. Das führt zu Kapazitätsverlust und zu rauen, instabilen Oberflächen.
Entwurf eines klügeren Elektrolyten
Ausgehend von der Erkenntnis, dass mossiges Wachstum durch lokale Ionenansammlungen an Vorsprüngen verursacht wird, entwickelten die Forschenden einen Elektrolyt‑Zusatzstoff, der sowohl die Bildung von mossigem Zink als auch das entstehende verschwenderische tote Zink adressiert. Sie verwendeten ein Salz namens Acetylcholin‑iodid, das positiv geladene organische Kationen und Iodid‑Anionen in einem Molekül liefert. Empfindliche Massenmessungen und Infrarotspektroskopie zeigten, dass die Kationen stark und selektiv an der Zinkoberfläche adsorbieren und dort eine dünne, positiv geladene Schicht bilden, die den Zink‑Ionen‑Fluss vereinheitlicht. Das fördert eine glatte, flache Zinkabscheidung statt filigranen, fadenförmigen Wachstums und hält die Oberfläche kompakt sowie widerstandsfähiger gegen Korrosion und Wasserstoffbildung.
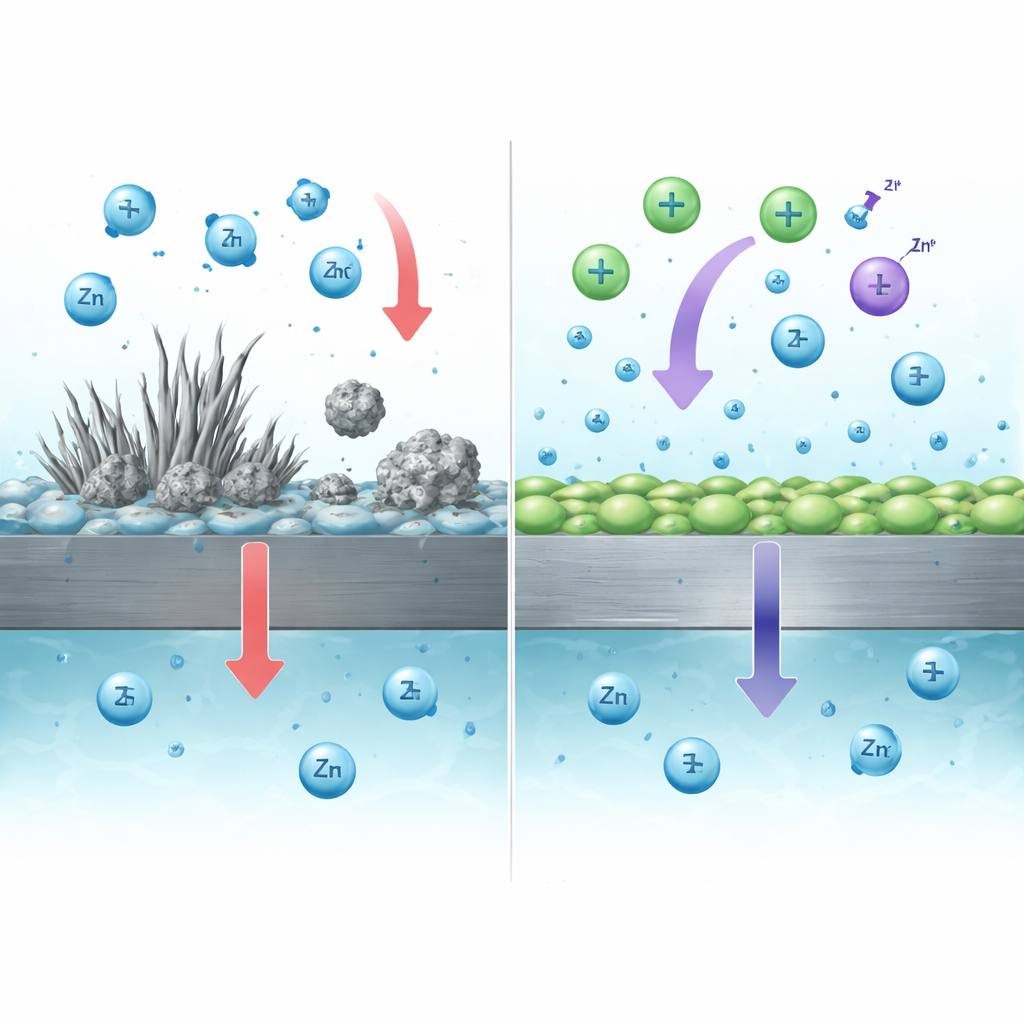
Verlorenes Zink reaktivieren, um die Batterielebensdauer zu verlängern
Der Iodid‑Anteil des Zusatzstoffs übernimmt eine andere, aber ergänzende Funktion. Beim Laden wird Iodid teilweise in eine mild oxidierende Spezies (I3−) umgewandelt, die mit toten Zinkpartikeln und isolierenden Zink‑haltigen Nebenprodukten auf der Oberfläche reagieren kann. Diese Reaktionen wandeln elektrisch isoliertes Zink zurück in gelöste Zinkionen, die in nachfolgenden Zyklen wieder an der Elektrode abgeschieden werden können. Experimente zeigten, dass totes Zink in einer jodhaltigen Lösung nahezu bis zum theoretisch erwarteten Ausmaß auflöste, und Vollzellen mit dem Zwei‑Ionen‑Zusatzstoff mehr Ladung zurückgewannen, als allein durch frisch abgeschiedenes Zink erklärt werden könnte — ein klarer Hinweis darauf, dass zuvor verlorenes Zink innerhalb der Batterie „recycelt“ wurde.
Was das für reale Batterien bedeutet
Durch die Kombination feld‑glättender Kationen mit einem zink‑recycelnden Anion ermöglichte der neue Elektrolyt Zinkelektroden mit einer mittleren Coulomb‑Effizienz von etwa 99,7 % und stabilem Betrieb über mehr als 1400 Stunden bei hohen Strömen und Kapazitäten — Bedingungen, die für netzgebundene Speicher relevant sind. Symmetrische Zinkzellen und praktische Zink‑Iod‑Beutelzellen zeigten geringe Spannungsverluste und behielten je nach Test nach Hunderten bis Zehntausenden von Zyklen mehr als 96 % ihrer Kapazität. Für Laien ist die Kernbotschaft: Die Forschenden haben genau herausgefunden, wie Zinkelektroden degradieren — durch ein zweistufiges mossiges Wachstum, das totes Metall erzeugt — und sie haben ein chemisches Rezept gezeigt, das sowohl diese schädliche Struktur verhindert als auch verlorenes Material wiederbelebt. Dieser duale Ansatz bringt sichere, wasserbasierte Zinkbatterien deutlich näher an einen langlebigen Einsatz in großem Maßstab in Haushalten und Stromnetzen.
Zitation: Gan, H., Liu, D., Zhang, Y. et al. Negative electrode degradation induced by two-stage zinc plating and its recovery in zinc batteries. Nat Commun 17, 2067 (2026). https://doi.org/10.1038/s41467-026-68844-z
Schlüsselwörter: Zinkmetall‑Batterien, Elektrodenabbau, mossiges Zink, Elektrolyt‑Zusätze, Netzspeicher