Clear Sky Science · de
cGAS-IFN-I-Reaktionen durch Entnahme nukleärer DNA aus sterbenden Zellen mittels Nukleocytose
Wie unser Immunsystem DNA von Toten liest
Wenn unsere Zellen bei Infektionen, Krebs oder durch normalen Verschleiß sterben, müssen ihre Überreste beseitigt werden, ohne übermäßige Entzündungen auszulösen. Diese Arbeit enthüllt einen überraschenden Mechanismus: Immunzellen können buchstäblich in die Zellkerne sterbender Zellen hineinbohren, deren DNA herausziehen und sie als Gefahrensignal nutzen. Das Verständnis dieses versteckten Aufräum‑und‑Alarm‑Systems könnte unsere Sicht auf antivirale Medikamente, Autoimmunerkrankungen, Krebstherapien und Arzneimittelnebenwirkungen verändern.
Ein verborgener DNA‑Alarm in Immunzellen
Unsere Zellen besitzen einen Sensor namens cGAS, der DNA an Orten erkennt, an denen sie nicht sein sollte—im Zellplasma statt sicher im Zellkern oder in Mitochondrien. Wenn cGAS auf solche DNA trifft, schaltet es ein starkes Alarmprogramm ein, das Typ‑I‑Interferone produziert, zentrale antivirale und immunregulierende Proteine. Man wusste bereits, dass Viren ihr genetisches Material in Zellen einschleusen und so diesen Weg auslösen können, und dass Fragmente unserer eigenen DNA gelegentlich entweichen und Autoimmunität verursachen. Doch eine grundlegende Frage blieb: Wie gelangt größere Menge eigener DNA, insbesondere aus toten Zellen, jemals zu cGAS, ohne zuvor in den zellulären “Mägen”—den Lysosomen—verdaut zu werden?
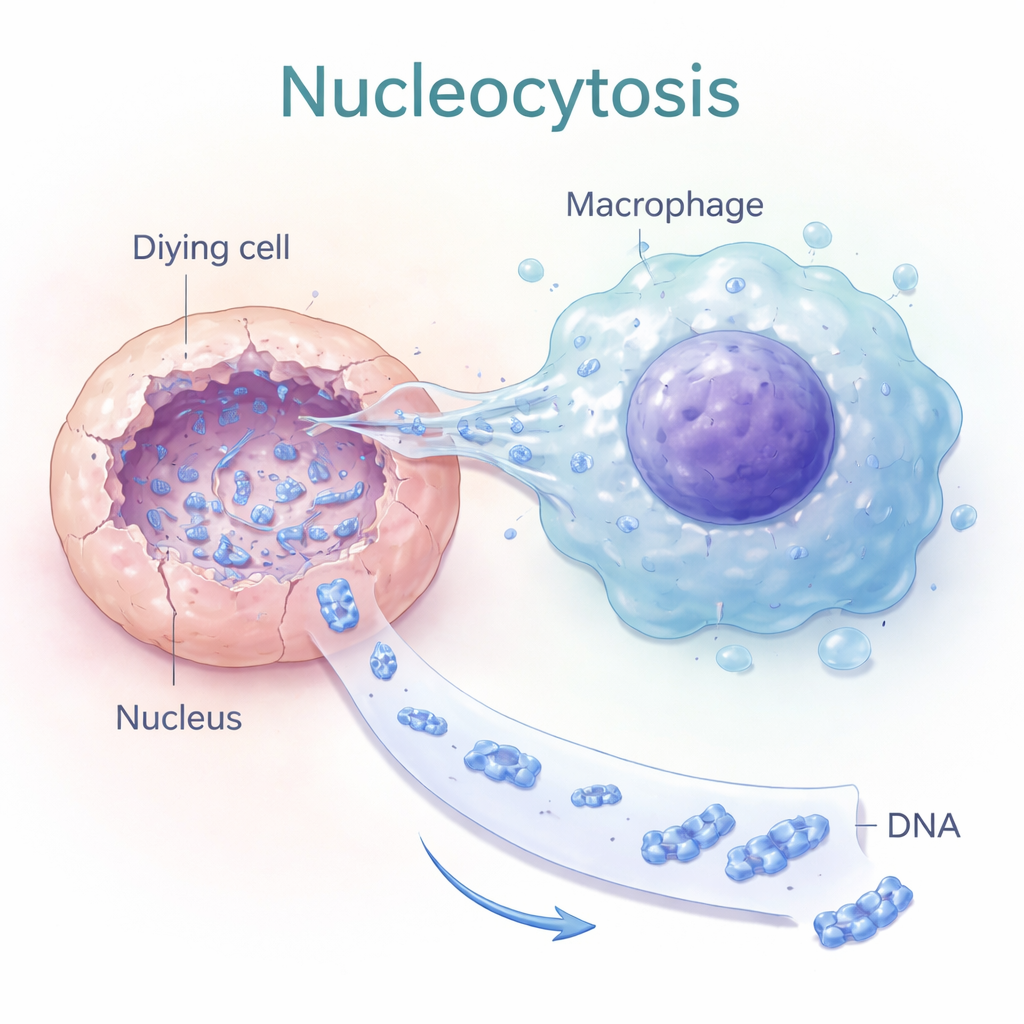
Nukleocytose: Tunnel in sterbende Zellkerne
Die Autoren beschrieben einen Prozess, den sie „Nukleocytose“ nennen, bei dem bestimmte Makrophagen—Immunzellen, die normalerweise Trümmer aufnehmen—etwas viel zielgerichteteres tun. Anstatt eine ganze tote Zelle zu verschlingen, strecken sie dünne, fingerartige Fortsätze direkt in den Kern der sterbenden Zelle. Lebendzellaufnahmen zeigten, dass die DNA‑Intensität im toten Zellkern abnahm, während sie in dem angehefteten Makrophagen zunahm, was auf eine aktive Entnahme nukleärer DNA hinweist. Dieser Transfer hing vom intrazellulären Skelett (Aktin) und von Signalstoffen ab, die die Zellform steuern, was nahelegt, dass Nukleocytose ein zielgerichtetes mechanisches Verhalten und kein passives Austreten ist.
Wenn antivirale Medikamente den DNA‑Alarm aktivieren
Während der COVID‑19‑Pandemie wurden Medikamente wie Hydroxychloroquin breit als antivirale Mittel getestet, doch ihre genauen Wirkungen im Körper blieben unklar. Die Forscher fanden heraus, dass Hydroxychloroquin und mehrere verwandte „kationisch‑amphiphile“ Medikamente den cGAS–STING–Interferon‑Weg stark aktivieren können—aber nur in einer Untergruppe von Makrophagen. Diese Wirkstoffe stören Lysosomen, indem sie deren pH erhöhen und ein Enzym namens PPT1 blockieren, das beim Abbau von Fettsäure‑Markierungen an Proteinen hilft. Die kombinierte Wirkung treibt einige Zellen in eine spezielle Form des Zelltods, bei der ein Protein namens Calreticulin im Zellkern akkumuliert. Makrophagen richten dann bevorzugt Fortsätze auf diese calreticulin‑reichen Kerne aus, entnehmen DNA via Nukleocytose und lösen in nur wenigen Zellen eine intensive Interferonproduktion aus—genug, um ein starkes lokales antivirales Signal zu erzeugen, ohne den ganzen Körper zu überschwemmen.
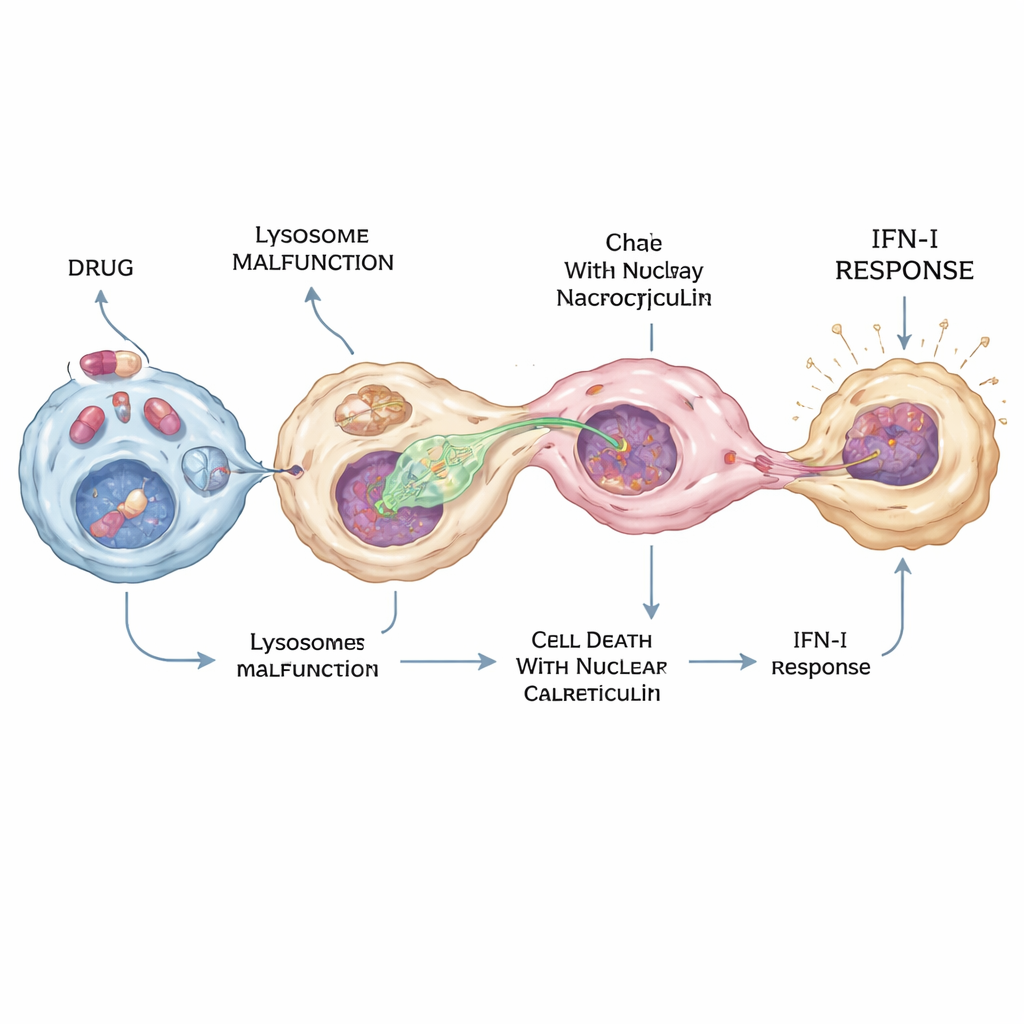
Von lokaler Abwehr zu Krankheit und Nebenwirkungen
Durch Studien an Zellkulturen und in Mauslungen zeigte das Team, dass medikamentenbehandelte Makrophagen eine STING‑abhängige Interferonantwort entfachen können, die weitgehend lokal bleibt—zum Beispiel in der Lunge—statt systemisch zu werden. Das erklärt, warum Medikamente wie Hydroxychloroquin in bestimmten Geweben antivirale oder antitumorale Vorteile zeigen können, aber auch, weshalb sie bei Langzeitanwendung organspezifische Nebenwirkungen wie Augen‑ oder Herztoxizität verursachen können. Derselbe Nukleocytose‑Prozess könnte plausibel zu Autoimmun‑ oder Entzündungskrankheiten beitragen, wann immer tote Zellen und lysosomaler Stress zusammentreffen, weil er einen direkten Weg bietet, über den eigene DNA den cGAS‑Alarm auslösen kann.
Warum das für künftige Behandlungen wichtig ist
Für Nicht‑Spezialisten ist die Kernbotschaft: Immunzellen fressen tote Zellen nicht nur passiv; sie können aktiv die Kerne nach DNA „abgraben“ und diese als Signal zum Hilferuf nutzen. Dieser Nukleocytose‑Weg erklärt, wie unsere eigene DNA fokussiert und lokal mächtige antivirale Abwehrmechanismen aktivieren kann, und macht zugleich deutlich, wie Medikamente, die Lysosomen oder PPT1 stören, unbeabsichtigt diesen Schalter umlegen könnten. Indem man lernt, Nukleocytose gezielt hoch- oder herunterzuregulieren—entweder durch klügere antivirale und Krebstherapien oder durch das Vermeiden unerwünschter Selbst‑DNA‑Signale bei Autoimmunerkrankungen—hoffen Forschende, diesen neu entdeckten Mechanismus für sicherere, präzisere Therapien zu nutzen.
Zitation: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
Schlüsselwörter: nukleocytose, cGAS-STING, Hydroxychloroquin, Typ-I-Interferon, Makrophagen