Clear Sky Science · de
Entwicklung der manganbasierten Photoredox-Katalyse mit niederenergetischem Licht aus hochenergetischer sichtbarer Licht‑Photokatalyse
Weniger Licht, gleiche Chemie
Chemiker verwenden häufig helles, hochenergetisches Licht – etwa intensive blaue oder ultraviolette Lampen – um Reaktionen zu treiben, die komplexe Moleküle aufbauen. Dieses „harte“ Licht kann jedoch Energie verschwenden, empfindliche Molekülteile schädigen und ist schwer anzuwenden in tiefen Geweben oder großen Reaktoren. Diese Studie zeigt, wie einfache, preiswerte Mangansalze direkt im Reaktionsgefäß zusammengesetzt werden können, um mit deutlich sanfterem Rot- und naheinfrarotem Licht zu arbeiten und dennoch leistungsfähige, für Arzneimittel- und Materialforschung wertvolle Bindungsbildungen durchzuführen.
Warum sanfteres Licht wichtig ist
Hochenergetisches Licht ist ein bisschen wie ein Brenner, um eine Kerze zu entzünden: Es erledigt die Arbeit, kann aber auch alles in der Nähe verkohlen. In chemischen Reaktionen führt das zu Überreaktionen, Zerstörung empfindlicher Gruppen und schlechter Kontrolle. Sanfteres Licht – insbesondere Rot und Nahinfrarot, die weniger Energie tragen – dringt tiefer durch Flüssigkeiten und sogar biologische Gewebe und ist generell verträglicher für komplexe, fragile Moleküle. Das Problem ist, dass die meisten bestehenden lichtgetriebenen Katalysatoren auf höherenergetisches Licht abgestimmt sind, und deren Neuentwurf meist langwierige, komplexe Synthesen erfordert. Die Autoren wollten das „Photonenbudget“ solcher Reaktionen senken, ohne die Katalysatoren von Grund auf neu bauen zu müssen.
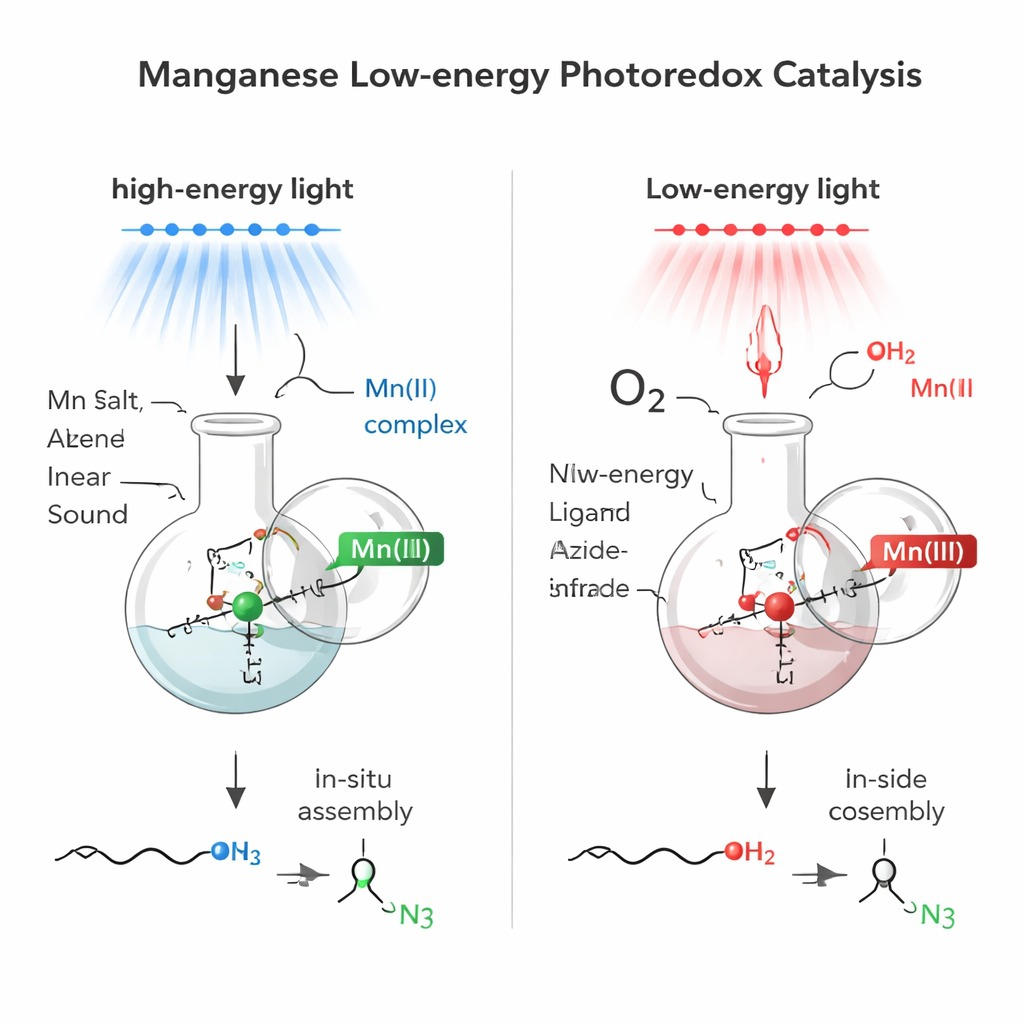
Den Katalysator direkt im Gefäß aufbauen
Anstatt aufwändige Metallkomplexe vorab herzustellen, verwendete das Team eine In-situ-Strategie: Sie mischten handelsübliche Mangansalze mit einem kleinen Hilfsmolekül (einem Liganden) und einer Azidquelle direkt in die Reaktionsmischung. Diese Selbstassemblierung erzeugte ein lichtabsorbierendes System auf Manganbasis. Mit einem Mangan(II)-Salz nahm die Mischung stark blaues Licht auf und konnte kurzlebige „Azido-Radikale“ aus einem gebräuchlichen Reagenz namens TMSN3 erzeugen. Diese reaktiven Fragmente addierten dann über einfache Kohlenstoff–Kohlenstoff-Doppelbindungen (Alkene) und setzten eine Azidgruppe (N3) an das weniger substituierte Ende der Doppelbindung – ein Muster, das als anti-Markownikow-Addition bekannt ist. Bemerkenswerterweise diente einfaches Wasser als Wasserstoffquelle, wodurch der Prozess sowohl einfach als auch atomökonomisch wurde.
Vom Blau ins tiefrote Spektrum
Die Forschenden fragten dann, ob ein eng verwandtes Mangansystem mit deutlich niederenergetischem Licht im tiefroten und nahinfraroten Bereich funktionieren könnte. Durch den Wechsel von Mangan(II) zu Mangan(III) und Feinabstimmung des Reaktionsmediums erzeugten sie eine neue Mischung, die Licht bis in etwa 850 Nanometer absorbierte – also weit ins Nahinfrarot hinein. Unter diesem schonenden Licht erzeugte der Mangan(III)-Komplex weiterhin Azido-Radikale, nun aber in Gegenwart von Luft (als Sauerstoffquelle) und einem einfachen Alkohol wurde in einem Schritt sowohl eine Azid- als auch eine Alkoholgruppe über das Alken eingebracht. Das Ergebnis ist ein β2-Azidoalkohol, ein besonders nützlicher Baustein, weil er zwei vielseitige funktionelle Gruppen – N3 und OH – an benachbarten Kohlenstoffatomen trägt.
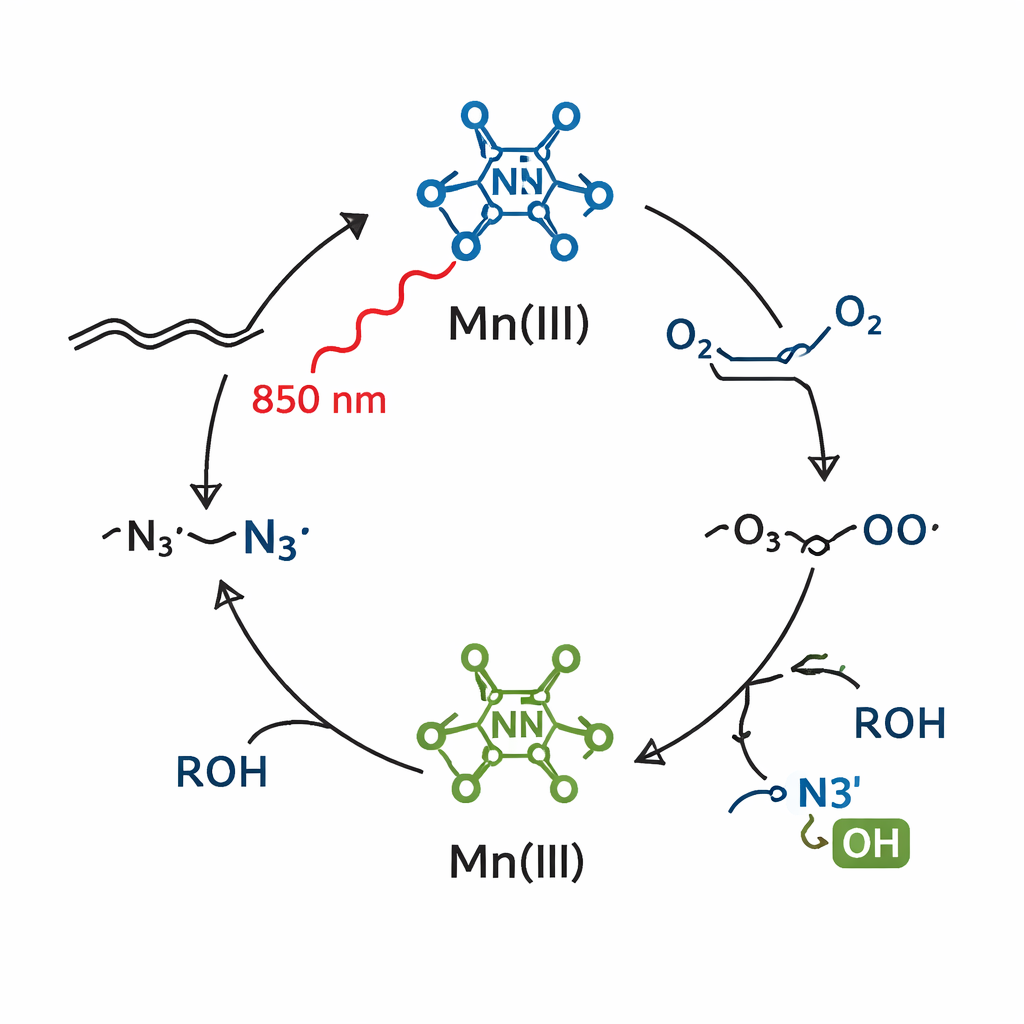
Von einfachen Alkenen zu komplexen, arzneimittelähnlichen Molekülen
Mit beiden Systemen – dem für blaues Licht und dem für niederenergetisches Licht – prüfte das Team eine große Vielfalt an Alkenen. Sie wandelten viele verschiedene Ausgangsmaterialien in Alkylazide oder β2-Azidoalkohole mit mäßigen bis hohen Ausbeuten um, selbst wenn die Moleküle Gruppen trugen, die typischerweise Metallkatalysatoren stören, wie ungeschützte Amine, Alkohole, schwefelhaltige Gruppen und komplexe Ringsysteme. Sie zeigten auch „Late‑Stage‑Funktionalisierung“, indem sie fortgeschrittene, arzneimittelähnliche Moleküle modifizierten und vorhandene Pharmazeutika in neue Derivate mit hinzugefügten Azid- und in einigen Fällen Alkoholgruppen verwandelten. Diese neuen Funktionen können später in andere stickstoffreiche Strukturen überführt oder an biologische Zielmoleküle gekoppelt („geclicked“) werden und erweitern so das Werkzeug für die medizinische Chemie.
Energieeffiziente Chemie mit praktischer Perspektive
Die Arbeit zeigt, dass sich eine hochenergetische blaulichtgetriebene Reaktion in einen niederenergetischen nahinfraroten Prozess „entwickeln“ lässt, allein durch Änderung der Art und Weise, wie ein gängiges Mangansalz in Lösung zusammengesetzt wird. Die in situ aufgebauten Mangansysteme ersparen zeitraubende Katalysatorsynthesen, nutzen ein reichliches und relativ wenig toxisches Metall und können sogar von natürlichem Sonnenlicht angetrieben werden. Für Nicht‑Spezialisten lautet die Kernbotschaft: Wir benötigen nicht immer härteres Licht oder teure seltene Metalle, um anspruchsvolle Chemie zu betreiben. Indem man Katalysatoren entwirft, die sich aus einfachen Bausteinen selbst bilden und auf sanfteres Licht ansprechen, weist dieser Ansatz den Weg zu energieeffizienteren, skalierbaren und biologisch verträglicheren Methoden zur Herstellung der komplexen Moleküle, auf die moderne Medizin und Materialien angewiesen sind.
Zitation: Yang, W., Song, Y., Yu, X. et al. Evolution of manganese low-energy photoredox catalysis from high-energy visible light photocatalysis. Nat Commun 17, 2062 (2026). https://doi.org/10.1038/s41467-026-68837-y
Schlüsselwörter: Photoredox-Katalyse, Mangan-Katalyse, niederenergetisches Licht, Alkenfunktionalisierung, Azido-Radikale