Clear Sky Science · de
Priming versus propagating: unterschiedliche Immunwirkungen von alpha- gegenüber beta‑teilchenemittierenden Radiopharmazeutika in Kombination mit Immun-Checkpoint‑Hemmung bei Mäusen
Strahlung als immunologischer Verbündeter
Krebsärzte versuchen zunehmend, das Immunsystem zur Tumorbekämpfung zu rekrutieren, doch viele Tumoren ignorieren oder widerstehen diesen Medikamenten weiterhin. Diese Studie stellt eine aktuelle Frage: Lassen sich verschiedene Arten zielgerichteter Strahlung nicht nur nutzen, um Tumoren direkt zu verkleinern, sondern auch, um das Immunsystem besser zu instruieren — und verändert die Wahl des radioaktiven Wirkstoffs die Art dieser Instruktion?
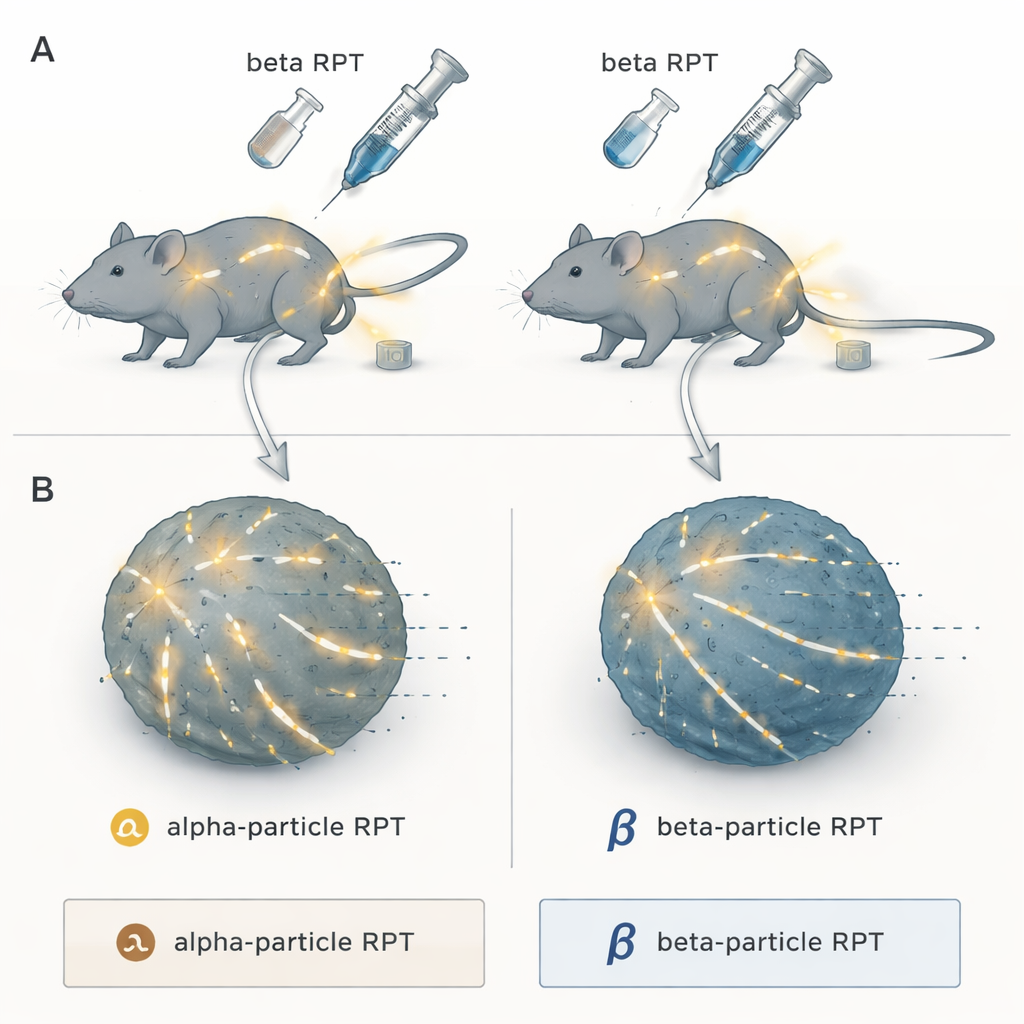
Zwei Varianten präziser Strahlentherapie
Die Forschenden konzentrierten sich auf radiopharmazeutische Therapie, ein „suchen‑und‑zerstören“-Verfahren, bei dem eine radioaktive Nutzlast an ein Molekül gekoppelt wird, das natürlicherweise Tumoren ansteuert. Nach der Injektion zirkuliert es im Körper und liefert Strahlung an Krebsherde, wo immer sie sich verbergen — etwas, das externe Bestrahlung bei weit verstreuter Erkrankung nur schwer leisten kann. Das Team verglich zwei Hauptkategorien: Alpha‑Teilchen‑Emittenten, die extrem dichte Energieschübe über sehr kurze Distanzen freisetzen, und Beta‑Teilchen‑Emittenten, die weniger dichte Strahlung aussenden, die weiter durch Gewebe reicht. Alle waren an denselben tumoranzielenden Träger NM600 gekoppelt, sodass sich nur die Strahlungsart — nicht die Zielgerichtetheit — unterschied.
Kombination von Strahlung mit Immun‑Checkpoint‑Blockern
Allein können Checkpoint‑Inhibitoren wie Anti‑PD‑L1 und Anti‑CTLA4 die Bremsen des Immunsystems lösen, funktionieren aber am besten, wenn der Tumor dem Immunsystem bereits sichtbar ist. In Mausmodellen von Melanom, Prostatakrebs und kolorektalem Krebs verabreichten die Forschenden eine sorgfältig gewählte niedrige Strahlendosis von NM600, entweder alpha‑ oder beta‑basiert, mit oder ohne Kombination von Checkpoint‑Inhibitoren. Sie variierten außerdem das Timing der Immunmedikamente — vor, kurz nach oder deutlich nach der Strahlenbehandlung — um zu untersuchen, wie der Zeitpunkt Ergebnisse wie Tumorwachstum, Überleben und langfristiges immunologisches Gedächtnis beeinflusst.
Wenn Beta‑Strahlung brilliert: Verstärkung einer vorhandenen Antwort
In einem „immun‑heißen“ Modell des kolorektalen Krebses, das bereits auf Immuntherapie reagiert, erzielte das beta‑emittierende NM600 die besten Ergebnisse, insbesondere wenn die Immunmedikamente früh oder zu einem mittleren Zeitpunkt begonnen wurden. Tumoren schrumpften stärker, Mäuse lebten länger, und geheilte Tiere lehnten denselben Krebs oft ab, wenn er Monate später erneut implantiert wurde. Detaillierte immunologische Profile zeigten, dass die Kombination aus beta‑basierter Behandlung und Checkpoint‑Blockade weniger eine neue Antwort erzeugte als eine bereits vorhandene verstärkte: bestehende tumorspezifische Killer‑T‑Zellen expandierten, wurden aktiver und produzierten mehr Angriffssignale. Kurz gesagt: Beta‑Emitter waren hervorragend darin, eine laufende Immunantwort zu propagieren.
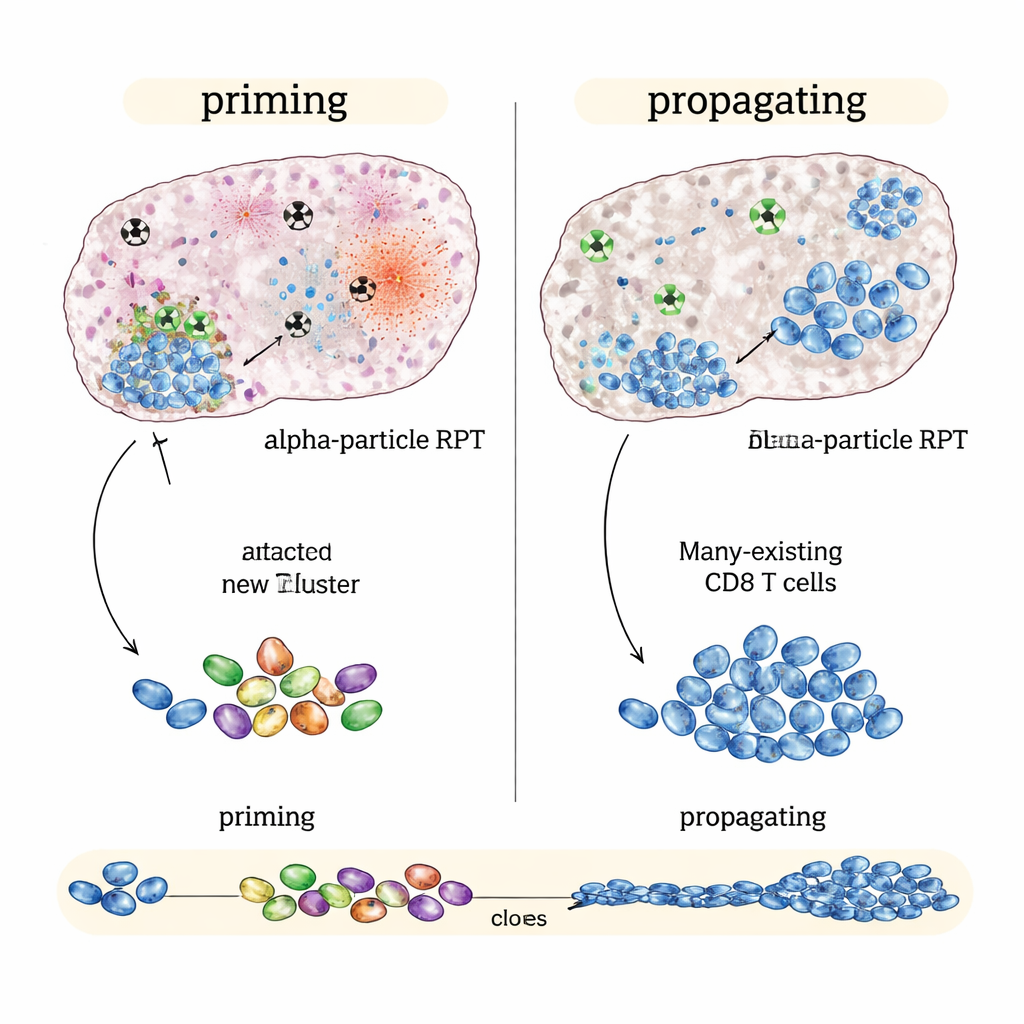
Wenn Alpha‑Strahlung brilliert: Auslösung neuer Immunangriffe
Im Gegensatz dazu zeigte die alpha‑emittierende Variante in „immun‑kalten“ Tumoren wie einem Melanom‑ und einem Prostatakrebsmodell, die kaum auf Checkpoint‑Medikamente alleine reagieren, bei gleicher durchschnittlicher Tumordosis bessere Wirkungen als Beta‑Emitter. Alpha‑basierte Therapie plus Immunmedikamente verlangsamte das Tumorwachstum stärker und verlängerte das Überleben weiter. Einzelzellgenetische Analysen legen eine Erklärung nahe: Alpha‑Strahlung verursachte intensive, lokal begrenzte Schäden, die offenbar starke Alarmsignale im Tumor generierten, während nahegelegene immunologische Strukturen weitgehend verschont blieben. Dieses Muster hing mit breiteren, diverseren T‑Zell‑Antworten zusammen und zeigte Anzeichen dafür, dass neue tumorerkennende Killer‑T‑Zellen gebildet und mit langlebigen Gedächtniszellen verknüpft wurden — Hinweise auf Immun‑Priming statt bloßer Verstärkung.
Warum Typ und Timing der Strahlung wichtig sind
Über die verschiedenen Modelle hinweg schnitt eine frühe oder mittlere Gabe der Checkpoint‑Inhibitoren — etwa zeitgleich mit dem Höhepunkt strahleninduzierter Gefahrensignale — durchweg besser ab als verzögerte Behandlung. Die Arbeit legt eine praktikable Faustregel nahe: Bei Tumoren, die dem Immunsystem bereits sichtbar sind, könnten niederdosisige, beta‑basierte Radiopharmazeutika ideale Partner für Checkpoint‑Inhibitoren sein, weil sie vorhandene Immunität propagieren und stärken. Bei immunresistenteren Tumoren könnten hochwirksame Alpha‑Emitter besser geeignet sein, neue T‑Zell‑Antworten zu primen und einen „kalten“ Tumor „heiß“ zu machen. Für Patientinnen und Patienten heißt das: Nicht alle radioaktiven Wirkstoffe sind austauschbar; die Abstimmung von Isotop und Zeitplan auf die immunologische Persönlichkeit des Tumors könnte Kombinationen aus Strahlen‑ und Immuntherapie wirksamer und dauerhafter machen.
Zitation: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
Schlüsselwörter: radiopharmazeutische Therapie, Alpha vs Beta Strahlung, Immun-Checkpoint-Inhibitoren, Krebsimmuntherapie, Tumormikroumgebung