Clear Sky Science · de
Sicherheit und biologische Aktivität eines bispezifischen T‑Zell‑Rezeptors gegen HIV Gag bei Männern mit HIV: Eine First‑in‑Human‑Studie
Warum diese neue HIV‑Studie wichtig ist
Menschen mit HIV können heute dank moderner Medikamentenkombinationen nahezu normale Lebensspannen erwarten. Diese Medikamente, die antiretrovirale Therapie (ART) genannt werden, entfernen das Virus jedoch nicht; sie halten es lediglich unter Kontrolle. Versteckte Nischen von HIV bleiben im Körper und können eine Infektion wieder neu entfachen, wenn die Behandlung stoppt. Diese Studie prüft eine neue Form präziser Immuntherapie — aufgebaut aus einem im Labor hergestellten T‑Zell‑Rezeptor — die das Immunsystem darauf trainieren soll, diese Verstecke bei Personen, die bereits gut unter ART kontrolliert sind, sicher aufzuspüren.
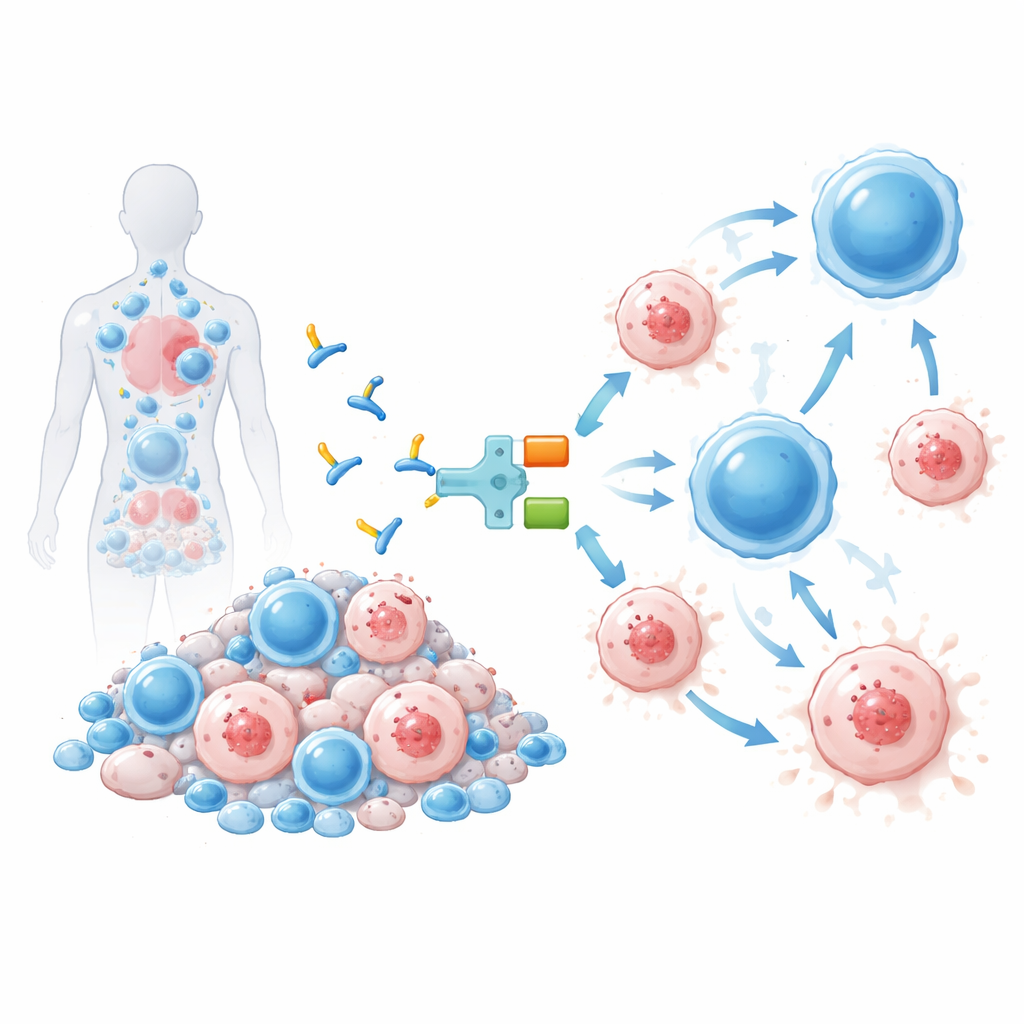
Das versteckte Virus, das nicht verschwindet
Selbst wenn Bluttests „nicht nachweisbar“ anzeigen, bleibt HIV als genetisches Material in langlebigen Zellen zurück, vor allem in einer Art weißer Blutkörperchen, den CD4‑T‑Zellen. Diese Reservoir‑Zellen tragen stilles, aber intaktes Virus, das wieder aktiv werden kann und Menschen dazu zwingt, lebenslang täglich Tabletten einzunehmen. Vollständig jede infizierte Zelle zu beseitigen ist extrem schwierig und ist nur bei wenigen Menschen gelungen, die risikoreiche Knochenmarktransplantationen wegen Krebs durchliefen. Viele Forschende zielen stattdessen auf eine „funktionelle Heilung“ ab: das Reservoir so weit zu verkleinern, dass die körpereigene Abwehr HIV ohne ständige Medikamente kontrollieren kann.
Ein konstruiertes Molekül, um T‑Zellen umzulenken
Die hier getestete Therapie, IMC‑M113V genannt, ist ein kleines Protein, das wie ein molekularer Adapter zwischen infizierten Zellen und dem Immunsystem wirkt. Ein Ende von IMC‑M113V ist ein gentechnisch veränderter T‑Zell‑Rezeptor, der ein kleines HIV‑Fragment aus dem Gag‑Protein erkennt, das im Kontext eines verbreiteten Immunmarkers (HLA‑A*02:01) auf der Oberfläche infizierter Zellen präsentiert wird. Das andere Ende bindet an CD3, eine Struktur, die auf allen T‑Zellen vorhanden ist. Wenn IMC‑M113V beide Seiten gleichzeitig verbindet, bringt es gewöhnliche T‑Zellen in engen Kontakt mit einer HIV‑infizierten Zelle und löst deren Abtötung aus. In Labortests war dieses Molekül extrem empfindlich: Es erkannte bereits wenige Kopien des viralen Fragments auf der Zelloberfläche und eliminierte effektiv Zellen, die mit mehreren häufigen HIV‑Varianten infiziert waren, während es gegen eine Palette gesunder menschlicher Zellen keine nennenswerte Aktivierung zeigte.
Erster Test bei Menschen mit HIV
Um zu prüfen, ob dieser Ansatz beim Menschen sicher ist, führten die Forschenden eine Frühphasenstudie mit zwölf erwachsenen Männern mit HIV im Vereinigten Königreich, in Belgien und in Spanien durch. Alle Teilnehmenden hatten eine gut kontrollierte Infektion unter ART, hohe CD4‑Zahlen und trugen den erforderlichen HLA‑Typ. Jede Person erhielt eine einzelne intravenöse Dosis IMC‑M113V in einer von drei niedrigen Dosisstufen und wurde anschließend einen Monat lang engmaschig überwacht. Der Hauptfokus in dieser Phase lag auf der Sicherheit: es wurden Nebenwirkungen wie Fieber, schwere Entzündungsreaktionen oder neurologische Probleme beobachtet, die bei anderen potenten T‑Zell‑aktivierenden Medikamenten in der Krebsbehandlung auftreten können.
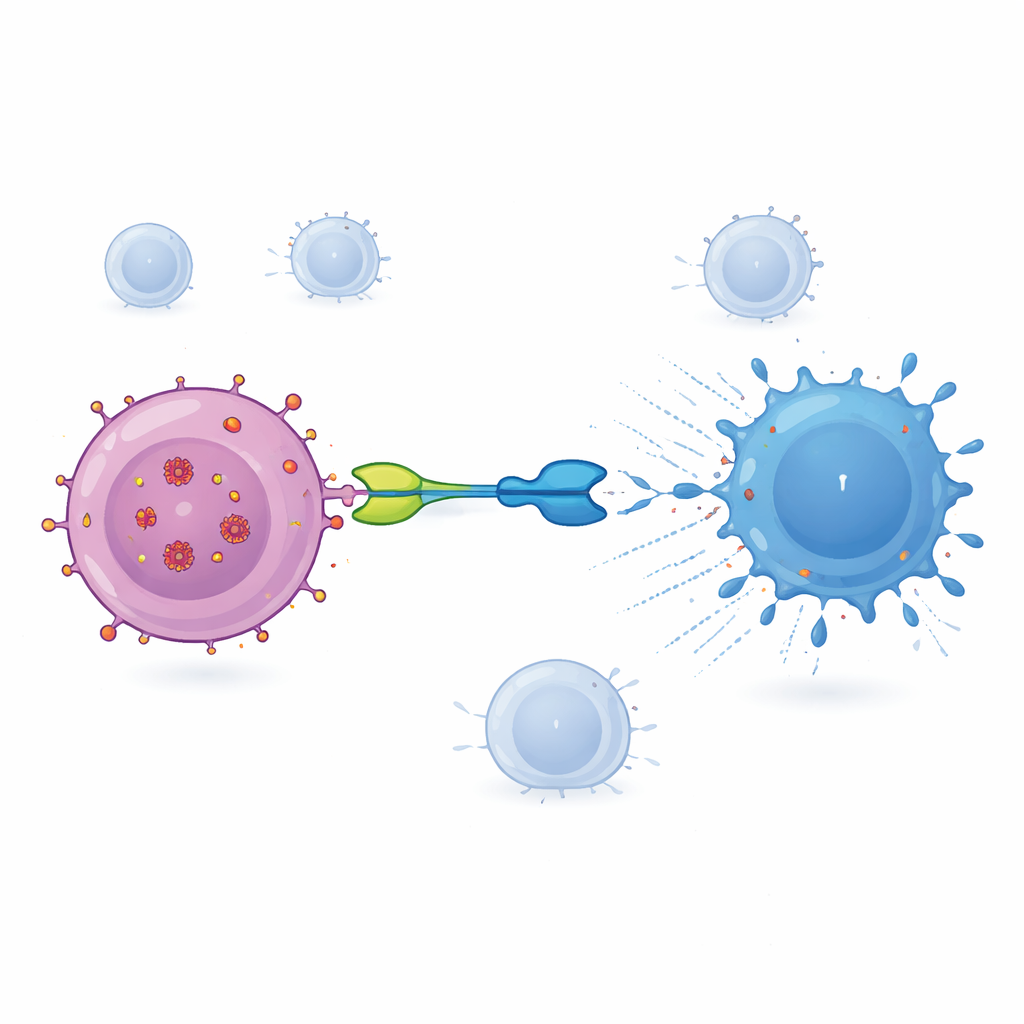
Was die Forschenden in der Klinik beobachteten
Über alle Dosen hinweg wurde IMC‑M113V im Allgemeinen gut vertragen. Die Hälfte der Teilnehmenden berichtete über Nebenwirkungen, überwiegend milde Symptome wie Müdigkeit oder Hautirritation, und niemand entwickelte schwere Komplikationen wie Zytokinfreisetzungssyndrom oder Neurotoxizität. Bluttests zeigten, dass die Wirkstoffspiegel innerhalb von etwa einem Tag anstiegen und wieder abfielen, mit einer Halbwertszeit von ungefähr 15–22 Stunden. Bei der höchsten Dosis (15 Mikrogramm) zeigten mehrere Teilnehmende vorübergehende Anstiege entzündlicher Moleküle, besonders von Interleukin‑6, sowie Hinweise darauf, dass ihre T‑Zellen aktiviert wurden und verstärkt zellabtötende Proteine zu produzieren imstande waren. Diese Immunveränderungen waren am stärksten bei Freiwilligen ausgeprägt, deren Viren Gag‑Varianten trugen, an die IMC‑M113V besonders stark binden kann, was darauf hindeutet, dass das Medikament seine vorgesehenen Ziele im Körper ansprach. Nach einer Einzeldosis gab es jedoch keine messbare Verringerung der Größe des HIV‑Reservoirs im Blut, gemessen an viralem RNA und intakter viraler DNA in CD4‑Zellen.
Was das für die zukünftige HIV‑Behandlung bedeutet
Für eine nicht spezialistische Leserschaft ist die Hauptbotschaft, dass diese Studie einen wichtigen ersten Nachweis des Konzepts liefert: Ein hochspezifisches immunologisches „Brücken“‑Molekül kann Personen mit gut kontrolliertem HIV sicher verabreicht werden und ihre T‑Zellen dazu bringen, Zellen zu erkennen, die das Virus beherbergen. Es heilte HIV nicht und ermöglichte nicht das Absetzen der ART, aber das war nicht das Ziel dieser First‑in‑Human‑Studie. Die Ergebnisse stützen die Erprobung höherer und wiederholter Dosen, möglicherweise in Kombination mit Substanzen, die mehr infizierte Zellen dazu verleiten, sich zu offenbaren, sowie die Ausweitung des Ansatzes auf andere HLA‑Typen über HLA‑A*02:01 hinaus. Wenn künftige Studien bestätigen, dass diese Strategie zuverlässig virale Reservoirs ohne gefährliche Nebenwirkungen verkleinern kann, könnte sie ein zentraler Baustein kombinierter Therapien werden, die eine langfristige, medikamentenfreie Kontrolle von HIV anstreben.
Zitation: Vandekerckhove, L., Fox, J., Mora-Peris, B. et al. Safety and biologic activity of a bispecific T cell receptor targeting HIV Gag in males living with HIV: a first-in-human trial. Nat Commun 17, 2207 (2026). https://doi.org/10.1038/s41467-026-68833-2
Schlüsselwörter: HIV‑Heilung, T‑Zell‑Therapie, viraler Reservoir, bispezifischer Rezeptor, klinische Studie