Clear Sky Science · de
Mechanistische Einblicke in die PCBP1-vermittelte Entfaltung ausgewählter i‑Motiv‑DNA an der G1/S‑Kontrollstelle
DNA‑Faltungen, die wie Verkehrsampeln wirken
In unseren Zellen ist der genetische Code mehr als eine einfache, gerade Leiter aus DNA. Teile davon können sich zu ungewöhnlichen Formen falten, die wie winzige Schalter wirken und steuern helfen, wann Zellen ihre DNA kopieren und sich teilen. Diese Studie konzentriert sich auf eine solche Form, das sogenannte i‑Motiv, und auf ein Protein namens PCBP1, das diese Strukturen erkennen und entfalten kann, genau in dem Moment, in dem sich eine Zelle zur DNA‑Replikation vorbereitet. Das Verständnis dieser Wechselwirkung erklärt, wie Zellen ihr Genom stabil halten und was bei Krebserkrankungen schieflaufen könnte.
Seltsame DNA‑Knoten in cancer‑verknüpften Regionen
Die meisten Menschen lernen, dass DNA die berühmte Doppelhelix bildet, doch bestimmte Abschnitte, die reich an dem Buchstaben C (für Cytosin) sind, können sich zu einem viersträngigen Knoten falten, dem i‑Motiv. Diese Strukturen treten bevorzugt in Kontrollbereichen von Genen auf, die das Zellwachstum steuern, wie cMYC und BCL2. Jahrelang wurde diskutiert, ob i‑Motive überhaupt in lebenden Zellen entstehen, weil sie in sauren Reagenzglasbedingungen leichter nachweisbar sind als in den nahezu neutralen Bedingungen im Körper. Mithilfe spezialisierter Antikörper, die i‑Motive erkennen, haben neuere Arbeiten, einschließlich der vorliegenden Studie, bestätigt, dass sie im Zellkern vorkommen—und oft in der Nähe wichtiger Wachstums‑ und Krebsgene gehäuft auftreten.
Ein Protein, das besondere DNA‑Faltungen erkennt
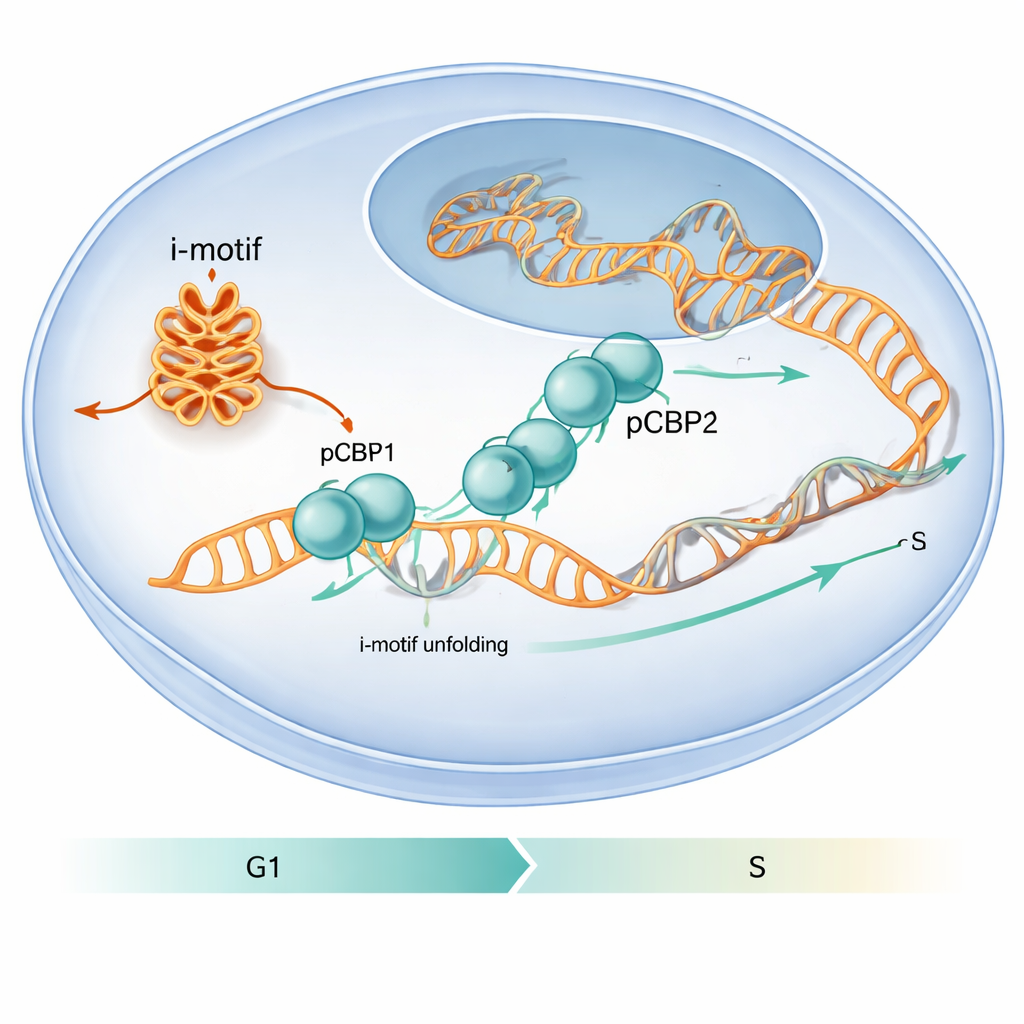
Die Autoren wollten herausfinden, wie Proteine in der Zelle mit diesen ungewöhnlichen DNA‑Faltungen umgehen. Sie konzentrierten sich auf PCBP1, ein Protein, das bereits dafür bekannt ist, C‑reiche DNA‑ und RNA‑Abschnitte zu binden und den Zellzyklus zu beeinflussen. Durch die Analyse vorhandener genomweiter Bindungskarten und gezielter Experimente stellten sie fest, dass PCBP1 häufig an C‑reiche Regionen bindet, die i‑Motive bilden können, insbesondere in der Nähe von Genstartstellen. In Zellversuchen mit humanen Krebszelllinien zeigten Regionen aus den Promotoren von cMYC, BCL2 und der insulinverknüpften ILPR‑Sequenz sowohl starke i‑Motiv‑Signale als auch starke PCBP1‑Besetzung, was darauf hindeutet, dass PCBP1 als spezialisierter Wächter dieser Strukturen fungiert.
Wie PCBP1 den Knoten packt und aufwickelt
In Reagenzglas‑Assays verglichen die Forscher, wie gut PCBP1 gefaltete i‑Motive gegenüber derselben DNA in ungefalteter Form bindet. Sie passten die Säurekonzentration so an, dass die DNA entweder gefaltet blieb oder entspannt wurde, während das Protein stabil blieb. PCBP1 bevorzugte stets das gefaltete i‑Motiv und band es etwa doppelt so stark wie dieselbe Sequenz in ungefalteter Form und nur schwach an nicht verwandte DNA‑Strukturen. Sobald es gebunden war, konnte PCBP1 aktiv das Aufwickeln fördern, sodass der i‑Motiv‑Strang mit seinem komplementären Partner paaren konnte. Allerdings verhielten sich nicht alle i‑Motive gleich: Manche, wie die Struktur im cMYC‑Promotor, wurden schnell entfaltet, während andere, etwa im BCL2, widerstandsfähiger waren und nur langsam aufwanden. Zusätzliche Merkmale wie Haarnadel‑Schleifen in der DNA und das Ausmaß der Protonierung der Cytosine (das Tragen zusätzlicher positiver Ladung) konnten die Entfaltungsaktivität von PCBP1 entweder fördern oder hemmen.
Teamarbeit innerhalb eines einzelnen Proteins
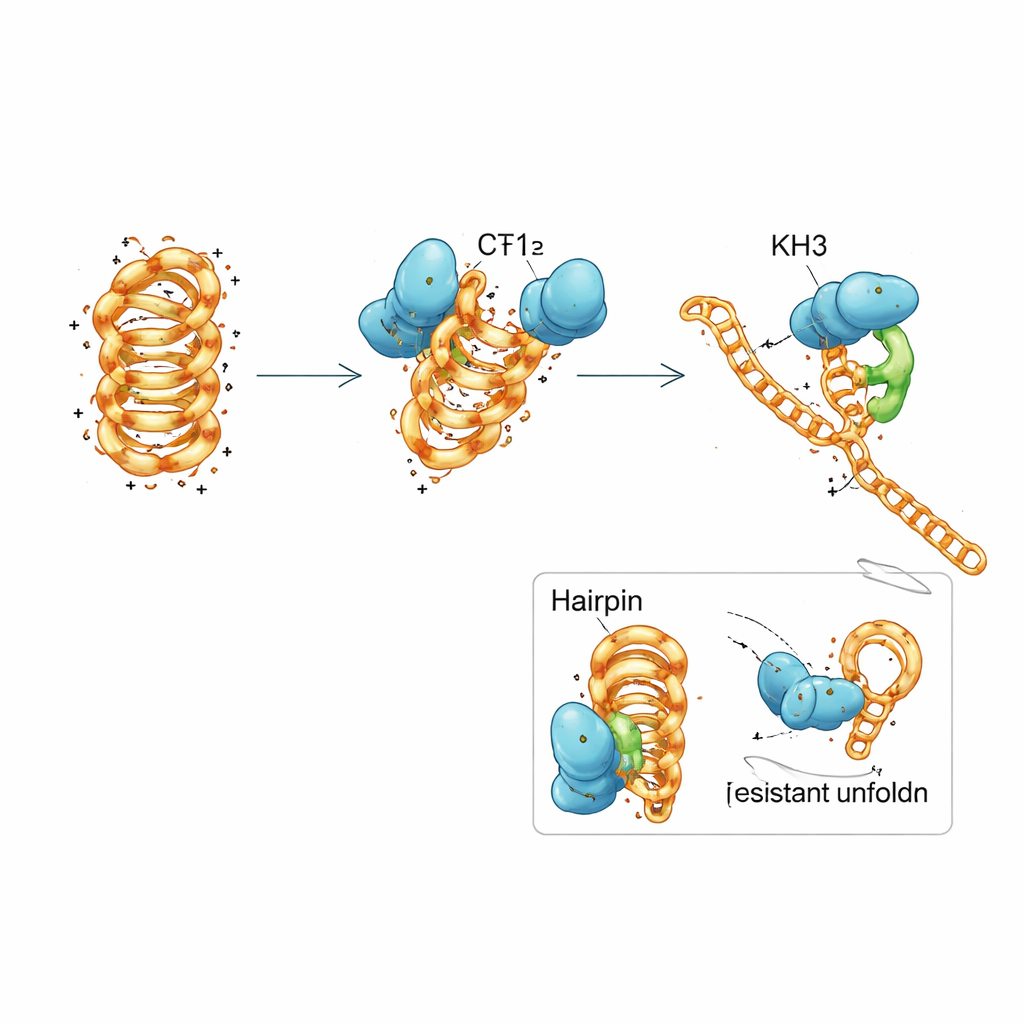
PCBP1 besteht aus drei wiederholten Modulen, den KH‑Domänen, gängigen Motiven, die kurze Abschnitte von Nukleinsäuren greifen. Das Team zerlegte PCBP1 in Teile und entdeckte, dass keine einzelne KH‑Domäne das Verhalten des gesamten Proteins vollständig nachahmen konnte. Die ersten beiden Domänen zusammen konnten sowohl gefaltete als auch ungefaltete DNA erfassen und das i‑Motiv in eine weniger stabile Form drängen, förderten aber nur langsam die vollständige Entfaltung. Die dritte Domäne allein band nur sehr schwach. Wenn alle drei Domänen vorhanden waren und zusammenwirkten, zeigte das Protein wieder seine starke Präferenz für gefaltete i‑Motive und seine effiziente Fähigkeit, sie zu entfalten. Detaillierte biophysikalische Messungen und Computersimulationen deuteten auf einen schrittweisen Mechanismus hin: KH1 und KH2 docken zuerst an flexible Schleifenregionen des i‑Motivs an und stören teilweise ausgewählte Basenpaarungen, was KH3 erlaubt, sich zuzuschalten und die Struktur in einen offenen, replikationsbereiten Zustand zu treiben.
Den Zellzyklus im Zeitplan halten
Die Arbeit zeigt außerdem, dass dieser molekulare Tanz für das Zellverhalten relevant ist. Reduzierten die Forscher PCBP1‑Spiegel in humanen Zellen, traten an bestimmten Genpromotoren mehr i‑Motiv‑Strukturen auf, DNA‑Schadensmarker stiegen und die Zellen blieben an der kritischen G1/S‑Kontrollstelle—dem Moment kurz vor Beginn der DNA‑Replikation—stecken. Unter normalen Bedingungen erreicht die Anwesenheit von PCBP1 an i‑Motiv‑bildenden Regionen rund um diese Kontrollstelle ihren Höhepunkt und nimmt dann ab, sobald die S‑Phase beginnt und die i‑Motive aufgelöst werden. Dieses Timing legt nahe, dass PCBP1 als Betreuer fungiert: Es bindet und entfaltet bestimmte i‑Motive genau im richtigen Moment, damit die DNA‑Replikation reibungslos ablaufen kann und das Genom intakt bleibt. Für eine allgemeine Leserschaft lautet die Botschaft: Ungewöhnliche DNA‑Faltungen können wie temporäre Straßensperren wirken, und PCBP1 ist eines der spezialisierten Werkzeuge der Zelle, um sie zu entfernen und so Fehler zu verhindern, die sonst zur Krebsentstehung beitragen könnten.
Zitation: Sengupta, P., Gillet, N., Obi, I. et al. Mechanistic insights into PCBP1-driven unfolding of selected i-motif DNA at G1/S checkpoint. Nat Commun 17, 1149 (2026). https://doi.org/10.1038/s41467-026-68822-5
Schlüsselwörter: i‑Motiv‑DNA, PCBP1‑Protein, Zellzyklus‑Kontrollstelle, Genomstabilität, DNA‑Sekundärstruktur